电活性生物材料是在电信号作用下能改变其理化特性或者在外界刺激作用下产生电信号的一类生物医学材料。电活性生物材料作为新一代“智能”生物材料,可以将电、电化学和力电信号刺激直接传递给细胞和组织,引起了生物医学领域研究人员的极大关注。此外,生物体的组织和细胞电学性质的研究也正在引起越来越多的关注。与离子物质和大分子的运输相关的电磁场在各种组织(例如心脏、肌肉、神经和皮肤)的许多生物过程中起重要作用,如血管生成、细胞中分裂、细胞信号传导、神经生长、胚胎发育和伤口愈合。
电活性生物材料主要包括压电特性生物材料、导电特性生物材料、半导体特性生物材料和电活性复合生物材料。其中,压电特性生物材料允许通过材料形变传递电刺激,而不需要外部电源,适合作为组织工程支架。导电特性生物材料需要通过外加电源来实现电刺激的控制。此外,导电特性生物材料的最大优点是可以通过调整合成途径和条件以及合成过程中的纳米结构,从而调控其化学、电学和物理性能以满足其生物应用的特定需要。
生物材料新的发展将取决于材料科学领域的进步以及对材料在分子、细胞和组织水平更深入的理解。Hench和Polak在论文《第三代材料》总结了三代生物材料的发展和演变史。
在20世纪60年代和70年代期间,开发出了用于模仿物理损伤组织的第一代生物材料,这类材料特征是生物惰性的不和生物体进行相互作用。随着对材料和生物组织之间界面相互作用机制更深入的理解,第二代生物材料的研究和开发完成了从“生物惰性”到“生物活性”的转变,这类生物活性材料能够与周围生物组织进行有效沟通。20世纪70年代在分子生物学以及90年代在基因组学和蛋白质组学领域的研究进展显著促进了生物医用材料进一步发展。进入21世纪,研究者开发出了结合生物活性和生物可降解性能的第三代生物材料,这类新材料能够激活特定基因,并可以在分子水平刺激组织再生。第三代生物材料涉及微环境分子调控细胞的特定反应,具有很好的前景。
![]()
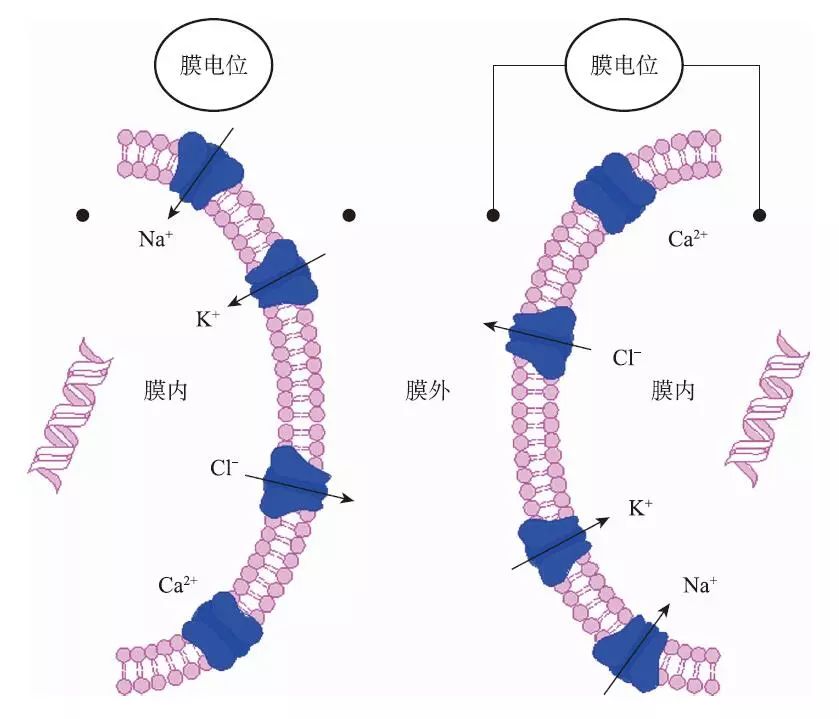
图1 在单细胞水平上生物电信号由离子通道蛋白产生
第三代生物材料在分子和细胞水平的进一步理解为设计材料用于组织修复提供了一个良好的科学基础。
同样地,在细胞和组织电生理行为方面的最新发现启发我们开发新一代生物材料用于组织修复及再生。生物电信号产生于细胞膜的离子通道,在体内的每个细胞都有具有离子通道的细胞膜包围,从而可以产生跨膜电压(图1)。因此,生物体内的所有细胞,不仅仅是兴奋的神经和肌肉细胞,都能产生和接收稳态的生物电信号。在这点上,生物电信号能够形成表观遗传途径来潜在地调节和控制每个细胞的行为。实际上,源于离子通道的生物电信号正越来越多地发现是细胞行为的关键调节因素,来调控细胞数目(细胞增殖和细胞凋亡)、位置(迁移和取向)和类型(细胞分化)。此外,内源性生物电流及电场的作用已经确定在组织再生过程起到重要作用。最近的实验表明,这类生物电信号机制可能比以前认为的具有更为显著的作用。例如,Zhao和他的同事发现,生理电信号强度在角膜和皮肤伤口愈合过程中的细胞迁移具有较强的指导作用[1]。
生物电在生物系统中的极其重要的作用启发我们提出作为用于生物医学应用的下一代生物材料的概念“电活性生物材料”,即第四代生物材料。尤其地,结合人体生物电系统可以为基础研究和临床医学的诊断和治疗提供了较大可能性。设计第四代生物材料实现两个目标:①通过调控细胞生物电信号用于组织再生;②能够监测细胞反应并可以通过生物电信号与宿主组织进行沟通交流。这些生物电信号可以反馈出相关的宿主响应于外部环境的刺激的详细信息,以及这些反馈可以通过电信号指导细胞的行为。
电刺激/调控可以通过基材或媒介进行施加,证实具有很多有益效果,包括刺激体内骨和神经再生。电活性生物材料,如导电聚合物、压电材料和碳基材料已经广泛用作优良新型的支架,有效地提供电刺激信号。在这些生物材料中,导电聚合物如聚吡咯由于其具有良好的电活性、生物相容性已被广泛用于电刺激平台。使用导电聚合物施加电刺激需要外加电源。对比之下,压电材料能够在施加外力下自发产生电信号。因此,由于其具有提供电刺激细胞以促进组织再生的潜在能力,越来越多研究者开始考虑利用压电材料作为电调控平台。最近,碳材料如石墨烯也开始作为很好生物电刺激平台引起了研究者们极大的兴趣。
电活性生物材料可以监控细胞外和细胞内的电生理过程,其对了解细胞内和细胞间的活动以及细胞是如何在庞大网络进行通信是非常重要的。细胞的电信号记录可以揭示细胞的基本行为以及细胞网络响应外部环境刺激的反应。
最近,研究表明半导体硅纳米线(硅纳米线)可以作为场效应晶体管(FET)有效信道用于检测来源于单个活细胞、细胞网络、组织和器官的高分辨率电信号(图2)。例如,硅纳米线生物传感器能够与单个细胞相互作用,并且可以感测到离子通过细胞膜产生的电场电位变化[2]。硅纳米线也可以与细胞内区域接触直接记录细胞内的电信号。除了提高电信号探测细胞的理化和生物微环境,硅纳米线也可以进一步监控新生组织的发育生长过程。例如,Liebe和同事开发了一种具有大孔结构的、柔韧的和独立式的纳米线的电活性支架(NanoES)。这些三维纳米电活性材料可以作为生物相容性细胞外支架促进神经元和心肌细胞的生长,并可以实时监控神经组织构建过程中的局部电生理活动。在另一个研究中,Tian等展示了一种可用注射器注射的网状纳米电活性材料,可以无痕和微创地植入大脑内三维记录脑功能[3]。
![]()
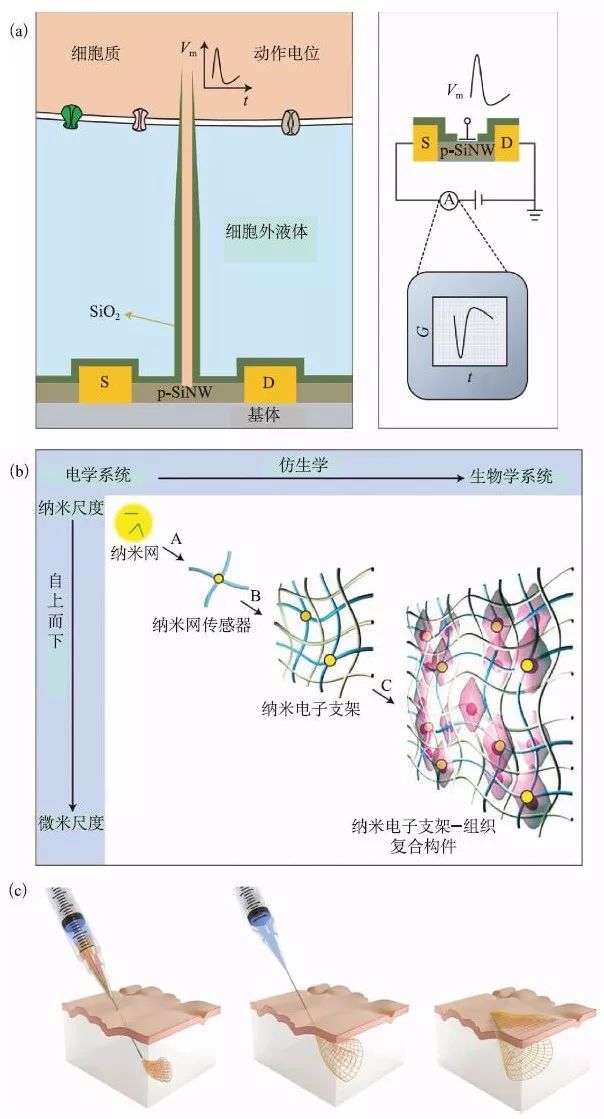
图2 硅纳米线(SiNW)半导体通过记录生物电信号来研究细胞和组织活动
(a) 基于SiNW 的器件用于细胞内跨膜电位检测[2];(b) 三维纳米尺度柔性电子器件培养细胞和组织[3];(c) 可装载在注射器中的网状电子器件注射进入脑组织中[4]
对生物电信号在细胞和分子水平的理解为第四代生物材料的分子设计提供了科学依据。合成生物学方法和材料科学的发展将允许我们合理地设计新一代电活性生物材料,可以刺激调控并在体外和体内记录细胞生物电活动,这将对促进再生医学的发展具有重要意义。我们也期望下一代的生物材料将能够通过细胞和分子生物学的进步得到进一步发展,并且这类电活性生物材料可以结合用于生物传感器、新的药物递送系统和组织支架等领域,以促进应用于临床的医疗器械的快速发展。
[1] Zhao M, Song B, Pu J, et al. Electrical signals control wound healing through phosphatidylinositol-3-OH kinase- [gamma] and PTEN [J]. Nature, 2006, 442(7101): 457-460.
[2] Duan X, Gao R, Xie P, et al. Intracellular recordings of action potentials by an extracellular nanoscale field-effect transistor [J]. Nature Nanotechnology, 2012, 7(3): 174-179.
[3] Tian B, Liu J, Dvir T, et al. Macroporous nanowire nanoelectronic scaffolds for synthetic tissues [J]. Nature Materials, 2012, 11(11): 986-994.
[4] Liu J, Fu T M, Cheng Z, et al. Syringe-injectable electronics [J]. Nature Nanotechnology, 2015, 10(7): 629-636.
![]()
本文摘编自宁成云,毛传斌著《电活性生物材料》第一章引言及第六章部分内容,略有删减改动。
![]()
《电活性生物材料》
作者:宁成云,毛传斌
责任编辑:周涵
北京:科学出版社,2017.12
ISBN:978-7-03-053839-0
《电活性生物材料》是一部综述电活性生物材料及其相关领域最新研究进展的学术专著。本专著对电活性生物材料进行了系统的定义和分类,并结合本课题组最新研究成果及国内外最新研究动态分别从压电特性、导电特性、半导体特性生物材料和电活性复合生物材料等方面,导电活性生物材料的制备、功能特性以及生物学应用等方面前沿研究成果进行系统论述。
(本期编辑:小文)
![]()
一起阅读科学!
科学出版社│微信ID:sciencepress-cspm
专业品质 学术价值
原创好读 科学品味
更多好素材,期待您的来稿
与科学相约 | 科学出版社征稿启事
![]()
点击“阅读原文”可购买本书