研究背景
【ASCO-GI 2019】胃癌免疫治疗临床试验数据的再探索:指引和启示
近日,2019年首场肿瘤学学术盛会——美国临床肿瘤学会消化道肿瘤研讨会(ASCO-GI)在美国旧金山成功举办。在胃癌领域,作为研究热点的免疫治疗,有多项研究在大会报道,如纳武利尤单抗联合andecaliximab对比纳武利尤单抗单药用于复发性胃或胃食管结合部腺癌[1]、帕博利珠单抗联合曲妥珠单抗及化疗用于HER2阳性转移性胃食管腺癌[2]等研究。除了上述临床研究疗效和安全性数据的报道,一些对既往研究的进一步探索性分析也引发了重要关注,其中包括亚洲ATTRACTION-2研究基于患者特征评估纳武利尤单抗疗效的探索性分析,以及欧美CheckMate-032研究中接受纳武利尤单抗患者与真实世界接受标准治疗患者的生存对比,这些探索性分析具有重要的临床启示意义,有助于指导后续研究和临床实践,以下将重点介绍这两项探索性研究。
中国医科大学附属第一医院肿瘤内科主任、教授、博士生导师
辽宁省医学会肿瘤学会主委
中国临床肿瘤学会(CSCO)常务理事
中国医师协会肿瘤医师分会常委
结直肠肿瘤专委会内科治疗专委会主委
中国医药教育协会结直肠肿瘤专委会主委
中国抗癌协会胃癌专委会
肠癌专委会和化疗专委会常委
中国老年医学会肿瘤分会副会长
国务院特殊津贴和全国五一劳动奖章获得者
【摘要8】 ATTRACTION-2研究探索性分析:根据患者基线特征评估纳武利尤单抗的疗效[3]
在这项III期、随机对照、多中心ATTRACTION-2研究中,纳武利尤单抗用于≥二线标准化疗耐药或不能耐受标准化疗的胃癌或胃食管结合部癌。与安慰剂相比,显示出更优的疗效和可管理的安全性。纳武利尤单抗组和安慰剂组的1年总生存(OS)率分别为27.3%和11.6%,2年OS率分别为10.6%和3.2%,死亡风险降低38%(HR=0.62,p<0.0001)[4]。根据基线人口学和疾病特征进行OS亚组分析显示,在所有亚组中,纳武利尤单抗均优于安慰剂。然而,约有一半的患者在接受纳武利尤单抗治疗后仍出现疾病进展。研究者试图进一步探索患者的临床基线特征与纳武利尤单抗疗效的关系。
研究方法
研究采用统计随机森林模型(一种机器学习模型)筛选可能导致纳武利尤单抗早期进展的临床因素。结果变量定义为56天的进展率,协变量为患者的临床特征。初次分析最终确定4个因素,包括低钠血症(低于正常值下限)、高中性粒细胞/淋巴细胞比率(NLR高于第2三分位,即≥4.15)、ECOG PS 评分(0或1分)和雷莫芦单抗治疗史(既往接受或未接受过)。
研究结果
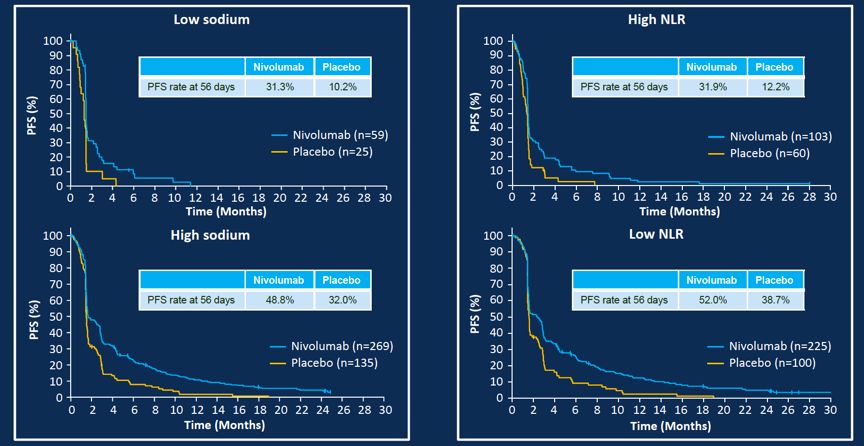
纳武利尤单抗组的330例患者,59例在基线时表现为低钠血症。单因素分析显示,低钠血症是预测早期进展的最强预测因素,如图1所示,低钠血症患者56天的PFS率对比,纳武利尤单抗组和安慰剂组分别为31.3%和10.2%。
图1. 单因素分析纳武利尤单抗组和安慰剂组的PFS
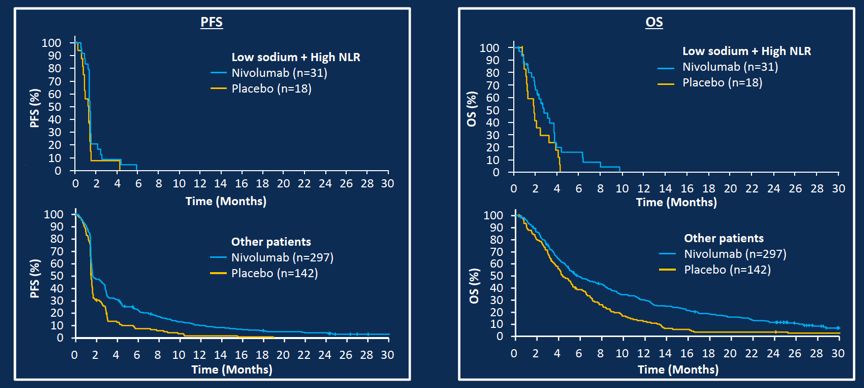
在配对因子分析中,低钠血症和以下任意一个因子组合,都是纳武利尤单抗早期进展的危险因素,包括高NLR(N = 31,9.4%;界值,第2三分位)、中性粒细胞升高(N = 28,8.5%;界值,第2三分位)、PS 1分 (N = 50,15.2%)或既往未使用过雷莫芦单抗(N = 55, 16.7%)。上述任意2个因素配对的患者中,纳武利尤单抗组和安慰剂组的PFS曲线几乎重叠。图2显示,同时存在低钠血症与高NLR两个因素,纳武利尤单抗组和安慰剂组的PFS和OS率只略有差别。
图2.双因素分析纳武利尤单抗组和安慰剂组的PFS和OS
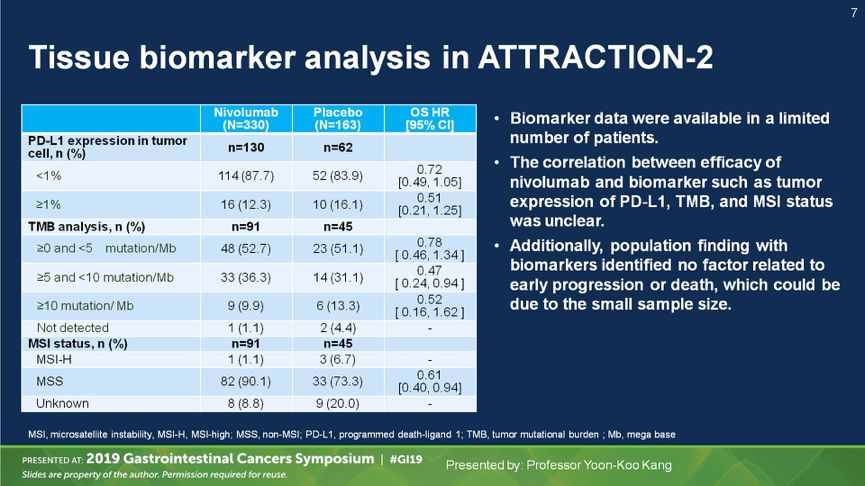
虽然生物标志物的分析仅限于部分人群,样本量偏小,但还是能观察到纳武利尤单抗的获益趋势。纳武利尤单抗在PD-L1表达<1%和≥1%的亚组相比于安慰剂均有改善OS 的趋势,HR分别为0.72和0.51;在各肿瘤突变负荷(TMB)亚组,纳武利尤单抗相比于安慰剂治疗的总生存HR在TMB 0~5、5~10、≥10组分别为0.78、0.47和0.52;微卫星稳定的患者接受纳武利尤单抗治疗总生存的HR为0.61(图3)。
图3.各生物标志物亚组纳武利尤单抗相比于安慰剂治疗的OS HR结果
小结
这一探索性分析的结果提示,低钠血症和高NLR的患者,接受纳武利尤单抗治疗的获益较少,与纳武利尤单抗治疗后的早期进展或死亡相关。纳武利尤单抗在总体状态较差(如低钠血症)和严重炎症状态(高NLR)的胃癌或胃食管结合部癌患者中的疗效可能有所降低。总体而言,本分析有一定的局限性,但为后续仍进一步验证及寻找预后相关临床指标提供了依据。
【摘要128】 模拟治疗比较法显示:纳武利尤单抗用于晚期/转移性胃或胃食管结合部癌优于标准治疗[5]
研究背景及研究方法
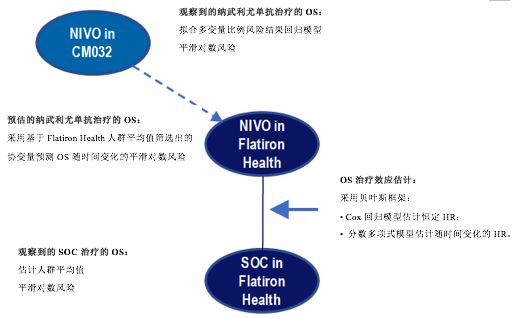
目前,尚无随机对照临床研究在二线或以上化疗耐药后的欧美胃癌/胃食管结合部癌患者中对比纳武利尤单抗与标准治疗的疗效。在基于亚洲人群的ATTRACTION-2研究中,纳武利尤单抗对比标准治疗的OS HR为0.63[6];然而,该亚洲患者结果是否同样适用于美国人群尚未可知。鉴于此,研究者尝试利用CheckMate-032研究(纳武利尤单抗的单臂Ⅰ/Ⅱ期在胃癌的研究)的个体患者数据(数据集1)与Flatiron Health电子健康数据库(数据集2)中接受现有标准治疗的患者数据采用模拟治疗比较法进行对比,旨在既往接受过二线或以上化疗的美国晚期/转移性胃癌或胃食管结合部癌患者中,评估纳武利尤单抗相比于现有标准治疗的生存优势。模拟治疗比较的方法学总结见图4,将Flatiron Health数据库中接受标准治疗的人群所观察到的OS和假设将纳武利尤单抗用于Flatiron Health人群所预估的OS进行比较。
图4.模拟治疗比较法示意图
结果与结论
CheckMate-032研究队列包含42例既往接受过二线或以上治疗的晚期/转移性胃癌或胃食管结合部癌患者。Flatiron Health数据库的3个队列从7566例患者中筛选,最终主要队列、随机队列和后线队列分别纳入36例、34例和118例患者。除Flatiron Health数据库队列患者的年龄更大、PS评分相对更差、血红蛋白水平相对更低外,不同队列患者的基线特征大体均衡。最常用的标准治疗方案包括雷莫芦单抗联合紫杉醇、雷莫芦单抗、FOLFIRI方案。
研究共甄别出6个有可能影响预后的协变量纳入OS回归模型,包括ECOG评分、碱性磷酸酶、血红蛋白、性别、既往手术及肿瘤部位;22个有可能影响治疗效果的因素,经分析,大多对治疗效果无显著影响。
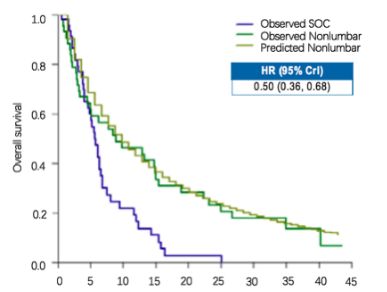
校正Flatiron Health数据库随机队列患者的协变量后,接受纳武利尤单抗治疗患者预估的生存期与CheckMate 032中实际观察到的生存期相似。基于模拟治疗比较法,接受纳武利尤单抗治疗预估的生存期对比Flatiron Health随机队列中观察到的生存期,提示纳武利尤单抗较标准治疗改善总生存(HR = 0.50;95% CI 0.36~0.68)(图5)。这与ATTRACTION-2研究中死亡风险降低37%的结果一致。鉴于尚无研究针对西方人群比较纳武利尤单抗与-标准治疗的随机对照研究,该研究的结果对于临床实践具有重要的启示意义。
图5.接受纳武利尤单抗患者预估的与实际观察到的生存期与接受SOC的生存期比较
目前,免疫治疗药物纳武利尤单抗和帕博利珠单抗已经分别在日本和美国获批用于晚期胃癌治疗,开启了胃癌免疫治疗的新时代。上述两项研究分别探索性分析了ATTRACTION-2研究基线患者特征与疗效的关系,以及采用创新性的方法对比了临床试验和临床实践中晚期胃癌使用纳武利尤单抗与标准治疗的结果,这两项研究为我们提供了重要数据,对后续研究和临床实践具有启示意义。
参考文献
1.SHAH M A, METGES J P, CUNNINGHAM D, et al. A phase II, open-label, randomized study to evaluate the efficacy and safety of andecaliximab combined with nivolumab versus nivolumab alone in subjects with unresectable or recurrent gastric or gastroesophageal junction adenocarcinoma[J]. J Clin Oncol, 2019 (suppl 4; abstr 75).
2.JANJIGIAN Y Y, CHOU J F, SIMMONS M, et al. First-line pembrolizumab (P), trastuzumab (T), capecitabine (C) and oxaliplatin (O) in HER2-positive metastatic esophagogastric adenocarcinoma (mEGA)[J]. J Clin Oncol, 2019 (suppl 4; abstr 62).
3.KANG Y K, SATOH T, CHAO Y, et al. Evaluation of efficacy of nivolumab by baseline factors from ATTRACTION-2[J]. J Clin Oncol, 2019 (suppl 4; abstr 8).
4.SATOH T, CHEN L T, KANG Y K, et al. phase III study of nivolumab (nivo) in previously treated advanced gastric or gastric esophageal junction (G/GEJ) cancer (ATTRACTION-2): Two-years update data[R]. 2018 ESMO Abstract 617PD.
5.CHAU I, AYERS D, GORING S, et al. Comparative effectiveness of nivolumab (NIVO) relative to standard of care (SOC) for advanced/metastatic (adv/met) gastric or gastroesophageal junction cancer (GC/GEJC): A simulated treatment comparison (STC)[J]. J Clin Oncol, 2019 (suppl 4; abstr 128).
6.KANG Y K, BOKU N, SATOH T, et al. Nivolumab in patients with advanced gastric or gastro-oesophageal junction cancer refractory to, or intolerant of, at least two previous chemotherapy regimens (ONO-4538-12, ATTRACTION-2): a randomised, double-blind, placebo-controlled, phase 3 trial[J]. Lancet, 2017, 390(10111): 2461-2471.
NP/IO/3818/03/06/19-03/06/20
41本肿瘤患者指南丛书
点击下方图片即可免费阅读
70个肿瘤相关临床试验招募患者
点击下方图片或识别图片二维码即可查看详情