肺癌治疗新发现!microRNA可作为逆转和预防肺癌耐药性的潜在靶点!
点击上方“转化医学网”订阅我们!
干货 | 靠谱 | 实用
作者:Paris
导语
近日,来自以色列医学癌症中心的研究团队进行的一项新研究发现,一种特殊突变基因的小片段——调节基因表达的非编码基因材料——微小RNA介导了肺癌靶向药物治疗的耐药性。这表明,microRNA可以作为逆转和预防肺癌耐药性的潜在靶点。这是继极光激酶后肺癌靶向治疗的又一大突破。相关论文发表在《nature》子刊《Nature Metabolism》上。

肺癌是全球癌症致死的主要原因之一,某些肺癌的特征在于名为EGFR的蛋白质发生突变。
EGFR基因突变在亚洲非小细胞肺癌(non-small-cell lung cancer, NSCLC)患者中尤为常见,随着EGFR抑制剂的上市,越来越多的患者从中获益,肿瘤控制率得以提高。EGFR抑制剂在EGFR突变型NSCLC中的批准和应用是一项重大临床突破,然而,EGFR酪氨酸激酶抑制剂(tyrosine kinase inhibitors, TKIs)常常在9个月~12个月时产生不完全应答,随后进展为获得性耐药。
发生耐药性的原因之一是肿瘤具有极高的生存能力,它们在最初会屈服于靶向疗法的冲击,但之后能重新连接自身的信号,激活旁逸斜出的生存途径继续存活,逃避靶向药物的击杀——这意味着这些肺癌细胞不再依赖于EGFR的驱动而存活,因此继续用EGFR抑制剂收效甚微。
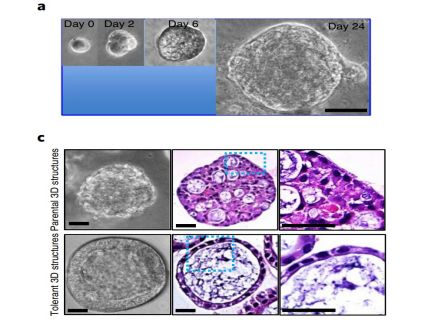
研究发现,EGFR阳性的耐受细胞出现在EGFR阴性药物耐受的细胞中,这表明其存活于最初的药物治疗。研究人员认为,靶向耐药细胞可作为阻断耐药性的新策略。随着奥西替尼在EFGR阳性的NSCLC一线治疗中的成功应用,确定驱动药物耐受性的变化至关重要。然而,对EGFRTKI耐受性的分子机制却未有深刻的见解。
为了解决这一认知空白,研究人员对启动抗癌药物耐受性的信号通路及耐受性如何影响癌症代谢和肿瘤复发进行了探索,单细胞衍生克隆的全转录组分析揭示了奥西替尼耐受性与假性缺氧之间的联系。众所周知,异常调节的代谢途径可导致肿瘤细胞生长,TAC循环的失调可通过激活假性缺氧反应诱导肿瘤发生。进一步的代谢组学和遗传研究表明,奥西替尼的耐药性是由miR-147b介导的VHL和琥珀酸脱氢酶的抑制驱动的,其与TAC循环和假性缺氧途径相关。
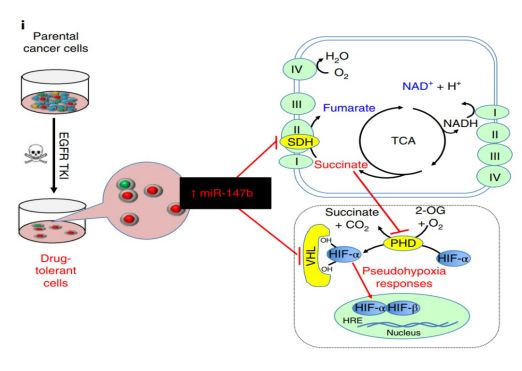
有了以上的理论基础,研究人员进一步用miR-147b抑制剂预处理肺癌患者衍生的3D结构,结果发现,耐药性肿瘤缩小了。miR147-b与三羧酸循环(TAC)的这种联系不仅可对抗肿瘤耐药性,且为预防肿瘤复发提供了有希望的靶标。Slack教授表示,接下来他将测试这一新途径是否可作为临床相关的EGFR突变肺癌小鼠模型的治疗方法。实践是检验真理的唯一标准,希望这一结果能够促进新试验的开展,让具有突变型EGFR的患者可以真正从中获益。
参考文献:
Wen Cai Zhang, Julie M. Wells miR-147b-mediated TCA cycle dysfunction and pseudohypoxia initiate drug tolerance to EGFR inhibitors in lung adenocarcinoma
推荐内容