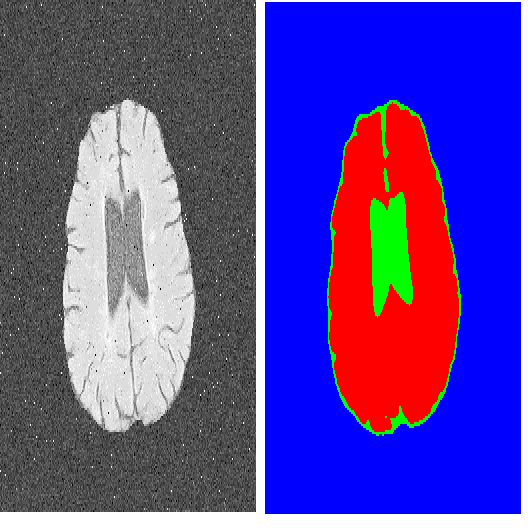
Convolutional Neural Networks (CNNs) work very well for supervised learning problems when the training dataset is representative of the variations expected to be encountered at test time. In medical image segmentation, this premise is violated when there is a mismatch between training and test images in terms of their acquisition details, such as the scanner model or the protocol. Remarkable performance degradation of CNNs in this scenario is well documented in the literature. To address this problem, we design the segmentation CNN as a concatenation of two sub-networks: a relatively shallow image normalization CNN, followed by a deep CNN that segments the normalized image. We train both these sub-networks using a training dataset, consisting of annotated images from a particular scanner and protocol setting. Now, at test time, we adapt the image normalization sub-network for \emph{each test image}, guided by an implicit prior on the predicted segmentation labels. We employ an independently trained denoising autoencoder (DAE) in order to model such an implicit prior on plausible anatomical segmentation labels. We validate the proposed idea on multi-center Magnetic Resonance imaging datasets of three anatomies: brain, heart and prostate. The proposed test-time adaptation consistently provides performance improvement, demonstrating the promise and generality of the approach. Being agnostic to the architecture of the deep CNN, the second sub-network, the proposed design can be utilized with any segmentation network to increase robustness to variations in imaging scanners and protocols. Our code is available at: \url{https://github.com/neerakara/test-time-adaptable-neural-networks-for-domain-generalization}.
翻译:当培训数据集代表了测试时预期会遇到的变异时, Convolution 神经网络(CNNNs)在监管学习问题方面非常出色。在医疗图像分割中,当培训和测试图像在获取细节方面出现不匹配时,例如扫描模型或协议,这一前提就被违反。CNN在这种情景中的显著性能退化在文献中有大量记载。为了解决这一问题,我们设计了CNN作为两个子网络的组合:一个相对浅薄的图像正常化CNN,随后是一条深度的CNN,其中分解了正常图像。我们用一个培训数据集来培训这两个子网络,由特定扫描仪和协议设置的附加图像组成。现在,我们在测试时,在预测分解标签的隐含之前,我们调整了图像的图像正常化子网络。我们设计了一个经过独立训练的自动解析器(DAE),用来在直观的解剖分解标签上进行隐含的模拟。我们校验了多点内部网络中的拟议想法: 持续磁力测试总图像结构的升级。我们展示了多点的智能结构的升级。