BRAF抑制剂单药治疗
【2018 SIMOS】BRAF抑制剂专场: BRAF抑制剂研究进展及安全性防控
2018年10月25~28日,第一届上海国际肿瘤内科学论坛(SIMOS)在国际都市上海市隆重召开,该会议汇聚了国内肿瘤领域的顶级专家,学术气息浓烈,本次论坛主题为“传递新知—抗肿瘤药物的规范应用及管理”。BRAF抑制剂作为重要的肿瘤靶向药物之一,在黑色素瘤(Melanoma)等肿瘤的治疗中具有不可替代的地位,故本次SIMOS特设了“BRAF抑制剂专场”,探讨BRAF抑制剂的相关问题。
浙江大学医学院附属邵逸夫医院潘宏铭教授、复旦大学附属肿瘤医院印季良教授、复旦大学附属肿瘤医院罗志国教授担任本次大会主席,来自中国人民解放军第八一医院的王锋教授、吉林大学第一医院的兰世杰教授、北京大学肿瘤医院的李永恒教授针对BRAF抑制剂的不同话题进行了精彩讲解。
大会主席:印季良教授、潘宏铭教授、罗志国教授
黑色素瘤的BRAF抑制剂治疗现状及进展
讲者:中国人民解放军第八一医院 王锋教授
中国人民解放军第八一医院 王锋教授
在黑色素瘤(Melanoma)的治疗方面,以达卡巴嗪为基础的联合化疗方案作为晚期黑色素瘤的金标准方案接近40年之久,但有效率<10%。近年来,恶性黑色素瘤的驱动基因的研究取得了显著进展,而BRAF基因是其中最为重要的驱动基因。因此BRAF抑制剂对恶性黑色素瘤的治疗具有关键的地位。接下来,将从4方面阐述BRAF抑制剂在恶性黑色素瘤中的治疗现状及进展。
目前应用于黑色素瘤单药治疗的BRAF抑制剂主要有三种,分别为维莫非尼(Vemurafenib)、达拉菲尼(Dabrafenib)以及Encorafenib(LGX818)。
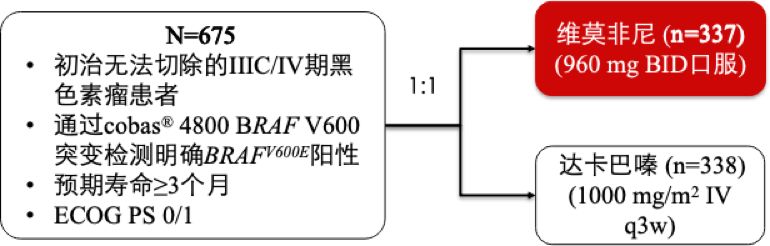
维莫非尼单药治疗黑色素瘤方面,BRIM-3是一项多中心、III期临床研究共纳入675例初治的晚期黑色素瘤患者,分别接受维莫非尼(n=337例)、达卡巴嗪(n=338)治疗。结果显示:
维莫非尼的起效时间更快,仅1.5月便可起效;
在总体有效率(ORR)方面,达卡巴嗪组仅为9%,而维莫非尼组的ORR可高达57%,提高达6倍之多;
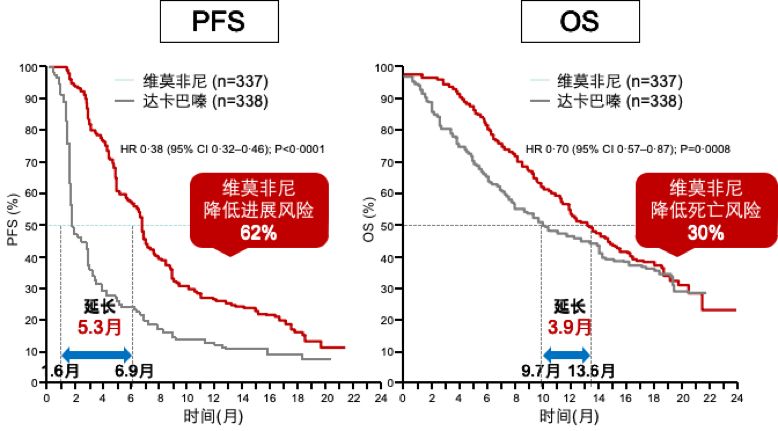
在无进展生存期(PFS)方面,达卡巴嗪组仅为1.6月,而维莫非尼组可达6.9月;总体生存期(OS)方面亦是维莫非尼组更具优势,分别为9.7月vs 13.6月。
BRIM-3 研究设计
BRIM-3 研究PFS/OS结果
在达拉菲尼单药治疗黑色素瘤方面,一项研究共纳入250例晚期黑色素瘤患者,按照3:1比例分别接受达拉菲尼组、达卡巴嗪组进行治疗。在PFS方面,分别为5.1月(达拉菲尼)vs 2.7月(达卡巴嗪),ORR同样是达拉菲尼占据绝对优势,分别为50% vs 6%。
综上,BRAF抑制剂单药治疗晚期黑色素瘤具有显著的疗效,相比较于达卡巴嗪等其他药物均可获得近期疗效及生存期的获益。
BRAF抑制剂联合MEK抑制剂治疗
BRAF抑制剂的联合治疗可进一步提升黑色素瘤的疗效。通常,达拉菲尼/维莫非尼/Encorafenib的联合对象主要有曲美替尼、考比替尼及Binimetinib。国际大型临床试验主要有以下三项基于白种人群的试验,以及一项基于亚洲人群的试验。
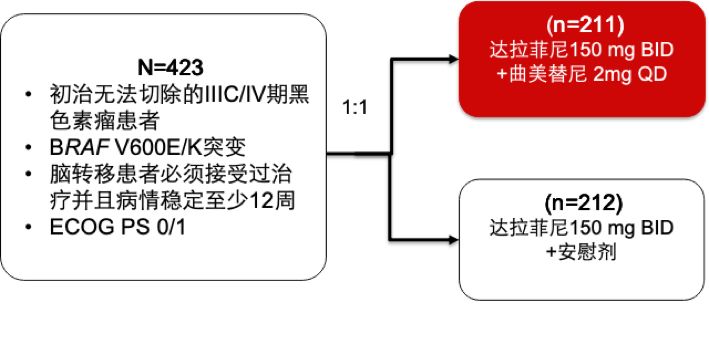
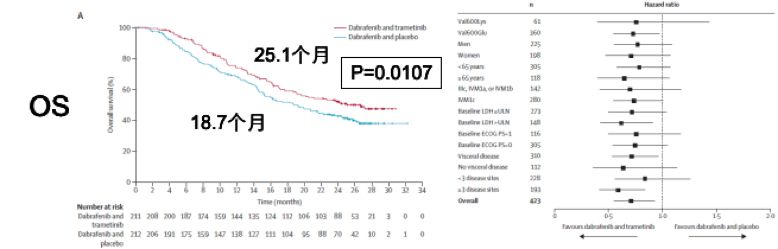
COMBI-D:一项临床研究共纳入423例晚期黑色素瘤患者,分别接受达拉菲尼+曲美替尼(联合组,n=211)、达拉菲尼+安慰剂(单药组,n=212)治疗。结果显示:
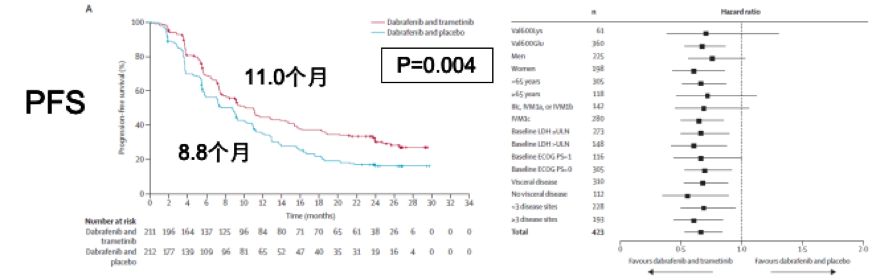
无论是PFS或OS均是联合组明显占优,PFS分别为11月vs 8.8月,OS分别为25.1月vs 18.7月;
总体有效率方面,联合组vs 单药组分别为69% vs 53%。
达拉菲尼+曲美替尼联合治疗研究设计
达拉菲尼+曲美替尼联合治疗PFS结果及亚组分析
达拉菲尼+曲美替尼联合治疗OS结果及亚组分析
Co-BRIM:一项研究纳入495例晚期黑色素瘤患者,分别接受维莫非尼+考比替尼(联合组,n=247)、维莫非尼+安慰剂(单药组,n=248)治疗。结果显示:
PFS分别为12.3月(联合组)vs 7.2月(单药组),OS分别为22.3月vs 17.4月,亦是联合组占优;
ORR方面,分别为70% (联合组)vs 50%(单药组)。
COLUMBUS:在Encorafenib联合Binimetinib方面,一项研究共纳入577例初治或一线免疫治疗失败的晚期黑色素瘤患者,分为三组进行治疗(Encorafenib联合Binimetinib、Encorafenib单药及维莫非尼单药)。结果显示:
Encorafenib联合Binimetinib组vs 维莫非尼单药的PFS分别为14.9月vs 7.3月;OS分别为33.6月vs 16.9月;
在ORR方面,Encorafenib联合Binimetinib、Encorafenib单药及维莫非尼单药分别为62% vs 52% vs 41%。
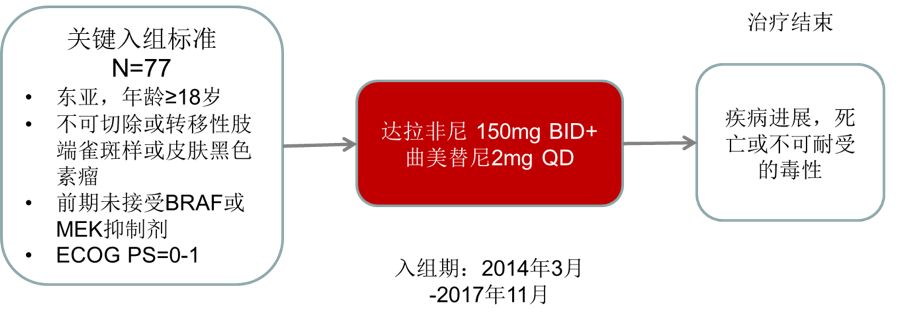
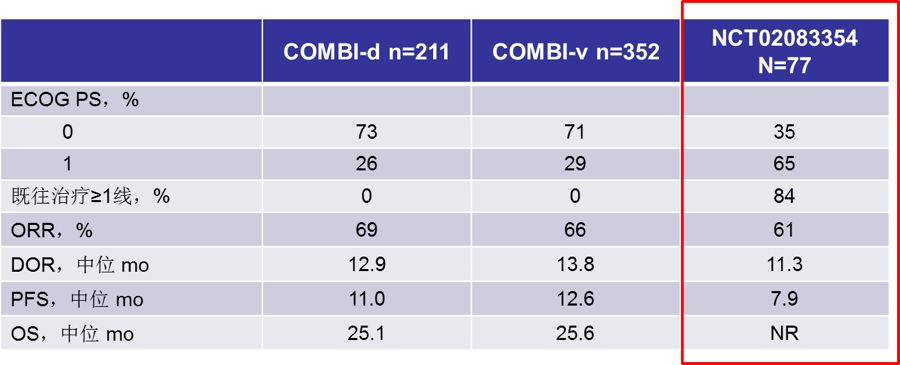
NCT02083354:首项基于亚洲人群的BRAF抑制剂联合MEK抑制剂研究。该研究未能得到如在白种人群中实现的疗效提升。这项研究共纳入77例未经BRAF或MEK抑制剂治疗的晚期黑色素瘤患者,进行达拉菲尼+曲美替尼治疗至疾病进展或死亡。结果显示:
达拉菲尼+曲美替尼的PFS为7.9月,明显劣于西方患者中的11.0-12.6个月;OS还未达到仍在随访中;
ORR达到61%,与西方患者中的66-69%类似。
达拉菲尼+曲美替尼东亚研究设计
达拉菲尼+曲美替尼东西方疗效数据比较
综上,BRAF抑制剂联合MEK抑制剂治疗相较于单药治疗,在西方患者中可显著改善疗效、延长黑色素瘤患者的PFS和OS。但在亚洲患者中却未能得到同样优异的疗效提升。因此适合中国黑色素瘤患者的治疗方案仍需探索。
BRAF抑制剂联合免疫检查点抑制剂
BRAF抑制剂、免疫检查点抑制剂在黑色素瘤治疗中均被证实有效,相关研究显示:维莫非尼+PD-L1抑制剂Atezolizumab,其总体有效率(ORR)可达76%。与此类似,达拉菲尼+Pembrolizumab+trametinib方案的ORR可达67%、而考比替尼+Atezolizumab的ORR亦达45%。综上,BRAF抑制剂联合免疫检查点抑制剂可改善疗效,是未来研究方向。
新辅助治疗
在一项单中心、开放随机、II期临床试验(Combi-Neo)中,分为2组,其中一组接受达拉菲尼+曲美替尼(8周),然后手术,术后再给予达拉菲尼+曲美替尼(至多44周)的新辅助治疗。另一组则接受即刻手术,然后给予标准辅助治疗。结果显示:无论是无事件生存期(EFS)、无远处转移生存期(DMFS)或疾病控制率(DCR),新辅助治疗方案均占优,EFS分别为19.7月vs 2.9月、DMFS分比为未达到vs 7.7月。综上,新辅助治疗方案较之于标准治疗方案而言,疗效更佳。
BRAF抑制剂治疗实体瘤的进展
讲者:吉林大学第一医院 兰世杰教授
吉林大学第一医院 兰世杰教授
除外黑色素瘤,BRAF抑制剂在其他实体瘤中亦有治疗作用。接下来,将从两大方面阐述BRAF抑制剂在实体瘤中的应用。
实体瘤中BRAF突变
2002年,Nature杂志报道了BRAF基因突变存在于多种实体瘤中,因此BRAF成为多种实体瘤的治疗靶点。在BRAF突变率方面,首当其冲的则为黑色素瘤,突变率>50%;其次则为甲状腺癌,BRAF突变率为50%-70%左右,结直肠肿瘤的BRAF突变率约10%,肺癌及其他实体瘤的BRAF突变率相对较低。在BRAF突变类型方面,最常见的为V600E突变,占所有BRAF突变率的98%。
常见实体瘤中BRAF抑制剂治疗进展
1、非小细胞肺癌(NSCLC)BRAF抑制剂进展
非小细胞肺癌(NSCLC)中BRAF突变率并不高(<5%),更常见于吸烟的NSCLC患者,以V600E突变为主,且与其他突变具有互斥性。
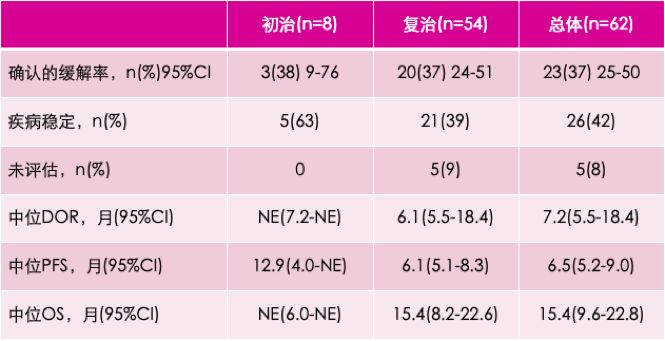
在VE-BASKET研究中,最初纳入20例BRAF突变的NSCLC患者,采用维莫非尼单药治疗。结果显示:总体有效率(ORR)达42%,中位PFS为7.3月,中位OS尚未达到,12月OS为66%。随后,VE-BASKET研究对NSCLC患者进行了扩展,共纳入62例BRAF突变的NSCLC患者(8例初治、52例复治),结果显示:维莫非尼治疗的总体中位PFS达6.5月,总体中位OS达15.4月,其中初治NSCLC患者的中位PFS达12.9月,中位OS尚未达到。
VE-BASKET研究结果
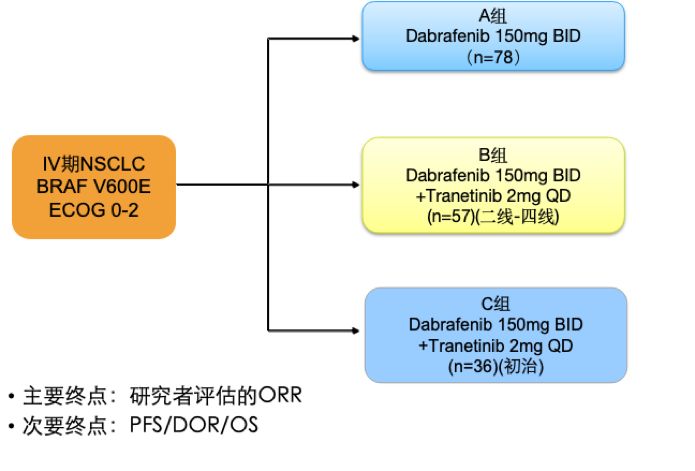
此外,在BRF113928研究中采用达拉菲尼+曲美替尼对36例初治、57例经治BRAF突变的NSCLC患者进行治疗,另采用达拉菲尼单药治疗78例NSCLC患者。结果显示:
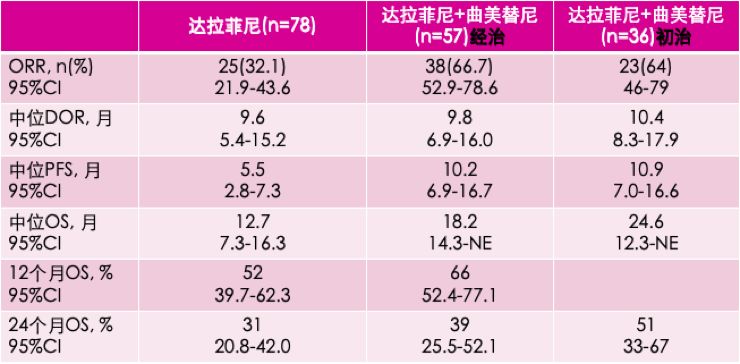
达拉菲尼单药组的ORR为32%,而达拉菲尼+曲美替尼联合组ORR分别为64%(初治)、67%(经治)。
生存情况方面,单药组的中位PFS仅为5.5月,而达拉菲尼+曲美替尼联合组的中位PFS分别达10.9月(初治)、10.2月(经治);中位OS也由单药组的12.7月,提升至联合组的24.6月(初治)及18.2月(经治)。
正是基于BRF113928研究的良好结果,美国FDA批准了达拉菲尼+曲美替尼联合方案用于BRAF突变的NSCLC治疗。
BRF113928研究设计
BRF113928研究结果
2、结直肠癌(CRC)中BRAF抑制剂进展
早期及晚期结直肠癌(CRC)中BRAF突变率约10%,绝大多数为V600E突变,更多见于右侧结直肠癌,远处淋巴结转移及肺转移发生率高。与黑色素瘤不同,BRAF抑制剂单药治疗的CRC疗效欠佳,这主要与BRAF抑制剂导致PI3K/Akt信号通路加强及肿瘤增殖相关。
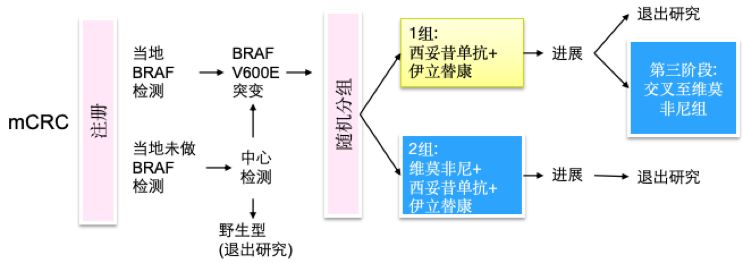
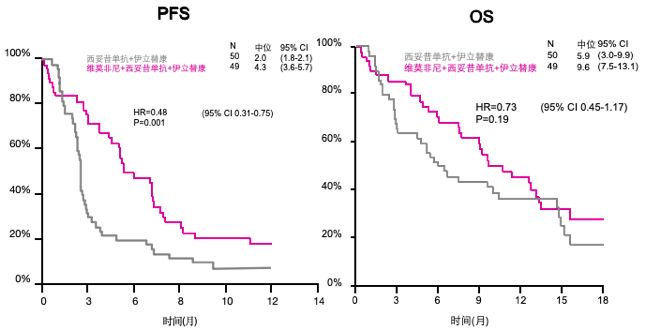
在临床进展方面,SWOG1406研究纳入99例BRAF V600E突变的转移性结直肠癌(mCRC)患者,分别接受西妥昔单抗+伊立替康、维莫非尼+西妥昔单抗+伊立替康治疗。结果显示:维莫非尼+西妥昔单抗+伊立替康组在PFS、OS及DCR等方面均有显著优势,中位PFS分别为4.3月vs 2.0月,中位OS分别为9.6月vs 5.9月,DCR分别为67% vs 22%。
SWOG1406研究设计
SWOG1406研究 PFS/OS结果
3、甲状腺癌中BRAF抑制剂进展
在乳头状甲状腺癌(PTC)中,约45%患者存在BRAF突变,以V600E突变常见。研究表明,存在BRAF突变的PTC患者肿瘤侵袭性更强,死亡率更高。
在治疗进展方面,一项多中心、开放标签、II期临床试验纳入51例BRAF V600突变的PTC患者(其中26例未接受过TKI治疗,另25例接受过TKI治疗),纳入后均接受维莫非尼单药治疗。结果显示:对于未接受过TKI治疗的PTC患者而言,维莫非尼单药治疗的疗效更佳,ORR为42.3%,明显高于接受过TKI治疗PTC患者的27.3%,并且在DCR、PFS及OS等都具有显著优势。
4、脑胶质瘤中BRAF抑制剂进展
胶质瘤中BRAF突变亦是以V600E突变为主,BRAF V600E突变与低级别胶质瘤的更好预后相关。临床进展方面,VE-BASKET研究中纳入24例BRAF V600E突变的神经胶质瘤患者,采用维莫非尼单药治疗的ORR可达25%,其中CR为4.2%,PR 达20.8%。可见,维莫非尼对于BRAF突变的神经胶质瘤亦具有一定的疗效。
BRAF抑制剂联合放疗的安全性管理
讲者:北京大学肿瘤医院 李永恒教授
北京大学肿瘤医院 李永恒教授
研究表明,BRAF抑制剂具有放疗增敏作用,可阻断MAPK/Erk信号通路,进而使更多的细胞停留在G1期,而G1期细胞对于放疗更为敏感。因此BRAF抑制剂联合放疗可增强放疗的治疗作用。但BRAF抑制剂联合放疗亦存在安全性方面的弊端,主要表现为:皮肤毒性、粘膜毒性、肺毒性及颅内神经毒性。接下来,将较为详细地阐述此四方面的毒性,并讲解BRAF抑制剂毒性预防的ECOG指南。
皮肤毒性
BRAF抑制剂联合放疗产生的皮肤毒性存在“增强”和“记忆”效应,“增强”效应即为导致皮肤毒性出现的时间提前(有时可在放疗第3天时便出现)且程度加重;而“记忆”效应则为放疗结束7天后再次应用BRAF抑制剂时,可引起皮肤毒性的加重。
皮肤毒性的严重程度与BRAF抑制剂使用时机存在较大相关性。研究显示:若BRAF抑制剂与放疗同期应用时,3级皮肤毒性发生率明显增加;相反,若BRAF抑制剂与放疗为非同期应用时,3级皮肤毒性很少发生。此外,尤其值得注意的是,当全脑照射治疗(WBRT)时同期应用BRAF抑制剂,其2级皮肤毒性达34%,3级皮肤毒性达6%;而非同期应用BRAF抑制剂2级和3级皮肤毒性分别为7%和0%,差异非常明显。故而,WBRT时应尽量避免同期应用BRAF抑制剂。此外,皮肤毒性的程度与皮肤所接受的剂量相关,而与处方剂量、BRAF抑制剂应用剂量无关。
皮肤毒性的预防及治疗方面,可应用护肤脂、局部糖皮质激素、水杨酸、磺胺嘧啶银等药物进行处理。一般而言,皮肤毒性的处理难度并不大,大部分皮肤毒性能在7天左右缓解。
粘膜毒性
BRAF抑制剂联合放疗可导致粘膜毒性发生率的增加,最常见发生于口腔、食道及胃肠道等部位。其中,最应当警惕的是胃肠道粘膜毒性,尤其是可能导致胃肠道穿孔。因此,在BRAF抑制剂应用时,应尽量避免胃肠道的照射。
在粘膜毒性预防及处理方面,主要可采用支持性治疗(如肠外营养)、糖皮质激素(如泼尼松)等进行治疗;若程度较重时,应停用BRAF抑制剂。
肺毒性
BRAF抑制剂联合化疗导致的肺毒性,最应当引起关注的为“放射性肺炎”,并且部分放射性肺炎可能存在“记忆”效应,即BRAF抑制剂联合放疗期间放射性肺炎不明显,但在后续化疗期间,放射性肺炎会显著加重导致咳嗽、呼吸困难等症状。在治疗上,放射性肺炎的处理主要为全身应用糖皮质激素,可根据情况联合抗生素。
颅内神经毒性
在颅内神经毒性方面,立体定向放疗(SRS)联合BRAF抑制剂发生颅内神经毒性局部控制率较好,并且研究显示BRAF抑制剂并不会增加SRS的颅内神经毒性发生率。因此,原则上应尽量避免全脑放疗(WBRT),而应倾向于SRS。
常见的颅内神经毒性有脑出血、脑坏死。研究显示,BRAF抑制剂联合放疗可增加脑出血发生率,但此类脑出血时间对患者的总体生存(OS)并无显著影响。在脑坏死方面,研究表明,BRAF抑制剂联合放疗并未增加脑坏死的发生率。
BRAF抑制剂联合放疗的ECOG共识
在BRAF抑制剂联合放疗方面,目前ECOG存在以下共识:
即便出现皮肤毒性,仍推荐在放疗期间继续应用BRAF抑制剂;
考虑到黑色素瘤的疾病进展快及易转移,应尽量不中断BRAF抑制剂的全身治疗;
目前尚无联合放疗的BRAF抑制剂优先选择。但ECOG共识在放疗联合的BRAF抑制剂方面推荐了维莫非尼/达拉菲尼。
在本次“BRAF专场会”接近尾声之时,来自浙江省肿瘤医院的方美玉教授、复旦大学附属肿瘤医院的陆雪官教授、吴向华教授及张哲教授针对BRAF抑制剂的研究进展、临床应用价值及前景等多项话题进行了精彩讨论及交流,将本次BRAF专场会再次引入高潮,并使会议内容得到升华。
小结
随着临床研究的不断深入,BRAF抑制剂在黑色素瘤等肿瘤治疗中的应用愈发成熟。以维莫非尼/达拉菲尼/Encorafenib为代表的BRAF抑制剂,无论是单药或联合治疗,均可显著改善黑色素瘤患者的近期疗效及远期生存。此外,BRAF突变及BRAF抑制剂的应用将在更多的实体瘤领域得到发掘和深耕,BRAF抑制剂联合放疗的安全性管控应规范化。
41本肿瘤患者指南丛书
点击下方图片即可免费阅读
70个肿瘤相关临床试验招募患者
点击下方图片或识别图片二维码即可查看详情