强强联手!新组合用药有望“创造”靶点,实现对癌症“围追堵截”
点击上方“转化医学网”订阅我们!
干货 | 靠谱 | 实用

作者:Ruthy
随着社会科技的发展,癌症治疗观念正在发生根本性的改变。其中通过设计合适的治疗药物,使其根据肿瘤细胞上的分子靶点对肿瘤细胞进行精准打击的“生物导弹”——靶向治疗俨然成为了肿瘤研究的热点。但是这种治疗方式的适应症有限,仅针对具有特殊靶点的癌症,使得靶点问题成了阻碍其广泛应用的一大难题。

近日,马里兰大学医学院的研究人员发现了一种破坏癌细胞的新途径,同时确定了可“践行”该途径的一种全新的药物组合(聚腺苷二磷酸核糖聚合酶(PARP)抑制剂+DNA甲基转移酶(DNMT)抑制剂),并证实该组合用药有望对癌症“围追堵截”!
PARP抑制剂——BRCA基因突变肿瘤的克星
细胞在长期进化过程中形成了复杂的DNA损伤反应防御机制,这是维护基因组稳定性的重要途径,该机制一旦缺陷便可导致包括肿瘤在内的多种疾病的发生。因此,DNA损伤反应通路也成为了新的抗肿瘤药物靶点。其中,BRCA是负责修复体内DNA错误的重要蛋白,一旦突变失效,DNA修复能力就会大大减弱,细胞将会更容易积累突变。突变的累积使得细胞为了保持DNA稳定更加依赖另一种DNA修复蛋白——PARP,而PARP抑制剂就成了处理BRCA突变癌细胞的重要“清洁工”。
PARP抑制剂可通过协同致死效应抑制肿瘤细胞的DNA损伤修复,进而杀伤肿瘤细胞,这是一种安全而有效的新型治疗方式。目前已研发出许多选择性和敏感性均较好的PARP抑制剂,且大部分已进入临床试验阶段,其功能与疗效在诸多靶向药中名列前茅,已经成为了BRCA基因突变肿瘤的克星。但PARP抑制剂对靶点要求精准,BRCA突变又只存在于乳腺癌和卵巢癌中,这就导致PARP抑制剂单药应用严重受限。难道这等好疗效当真无法惠及其他癌种?
DNMT抑制剂——为癌症创造新“靶点”
其实想让PARP抑制剂对其他癌种发挥作用说难也不难,只要让其他癌种也出现BRCA突变就可以了。但是,精确诱导基因突变的困难暂且不提,基因突变产生的严重后果也让人不敢轻易尝试这种方案。这是否意味着无计可施了呢?
PARP抑制剂与DNMT抑制剂在癌症中产生协同效应
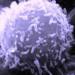
PARP抑制剂针对的是PARP蛋白,细胞会对PARP蛋白产生严重依赖是因为BRCA基因突变导致的DNA修复能力减弱,那么,若有其他方法能引发DNA修复能力减弱,是否就可以在没有BRCA基因突变的前提下使PARP抑制剂发挥作用呢?研究人员使用了DNMT抑制剂,其可通过抑制DNA异常甲基化的发生,进而激活沉默的抑癌基因来防治癌症,但这类化合物在体内结合DNA缺乏选择性,易产生严重的毒副作用,而这毒副作用之一就是诱导细胞出现DNA修复缺陷。这些表型与BRCA突变引发的表型相似同时与BRCA突变无关。他们指出,这种表型让BRCA突变阴性的肿瘤出现了新“靶点”,使得肿瘤细胞对PARP抑制剂敏感,响应PARP抑制剂的致死作用,阻断DNA缺陷的修复,进而强力杀伤肿瘤细胞。同时,他们指出这种组合用药与放疗结合还可得到意想不到的协同作用,真正实现对肿瘤的“围追堵截”!
这项研究确认了一种对抗肿瘤的全新方式,结合了当前市场上现有的药物得到了令人振奋的实验结果,为多种癌症的治疗注入了强心剂。同时也论证了将研究成果转化为临床患者受益的重要性,让患者真正受益将是广大癌症患者最大的福音!
参考文献:
Rachel Abbotts, et al.DNA methyltransferase inhibitors induce a BRCAness phenotype that sensitizes NSCLC to PARP inhibitor and ionizing radiation.PNAS .