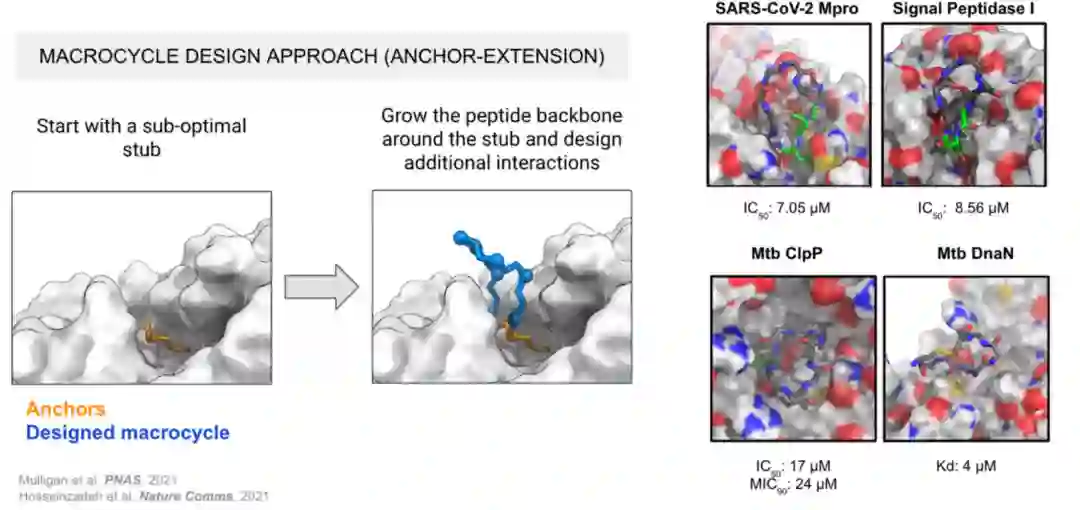
一、背景 多肽/环肽药物在近年吸引了不少药物科学家的眼球,环肽结合了分子量小,靶向结合力强等特点,是介于大分子和小分子药物中间的理想药物形式。目前已经有不少的研究表明,环肽对于体外循环的靶点具有良好的可设计性。
但其口服生物利用度一直是环肽/多肽药物研发的制高点,如何克服透膜性,是扩展环肽药物靶向胞内靶点的关键。本次David baker实验室的透膜环肽研究是领域一次重要突破,其验证了**“减少”环肽的极性基团**来提高其透膜性能力的概念,通过大量的实验验证提供了29条具透膜特性的环肽序列和结构。
二、算法
设计方法主要分为了2个主要的策略:
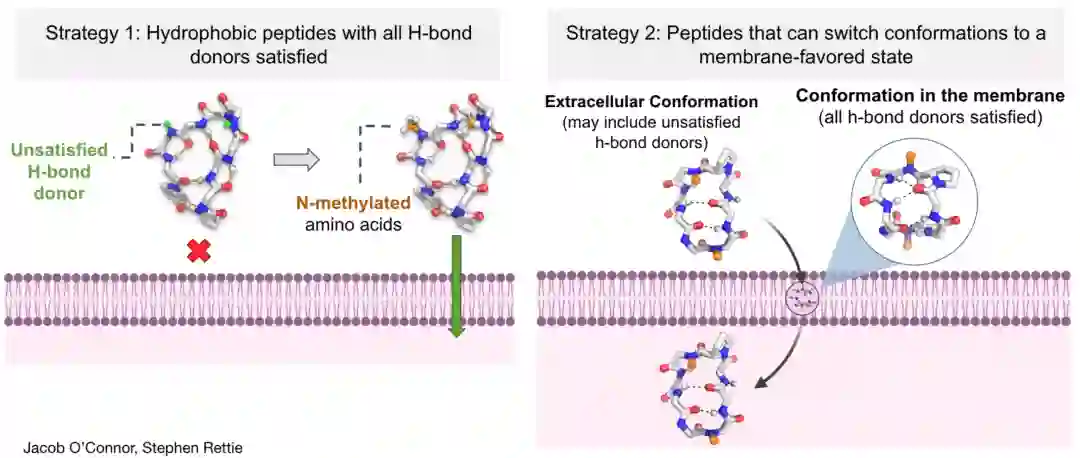
策略1:尽可能减少暴露的极性基团,增加疏水性
generalized kinematic closure (genKIC) 采样6-12个长度的多聚甘氨酸主链,把有2对以上主链氢键形成的构象取出; 1. 在有内部氢键相互作用的主链集合上,引入为L-pro,D-pro和AIB为刚性结构支撑位点,强化环肽的结构刚性; 1. (与之前环肽生成算法最大的不同点)消除暴露极性基团,在Rosetta设计序列阶段将主链上存在不饱和NH的氨基酸替换为主链甲基化的氨基酸类型,并且侧链序列设计空间只允许非极性残基; 1. 筛选<5个主链甲基化残基以及内部存在2个或以上氢键配对的序列进行下一步验证conformational energy landscape,把折叠态即为势能面最低点的序列筛选出来。 1. 根据ABOXY的rama二面角进行聚类。
策略2:基于变构透膜的方式设计
通过设计存在两种构象状态的多肽,使其在透膜过程中可以通过变构状态,将原本不饱和的极性基团自发形成氢键。从而形成可以透膜的“疏水态”。
3种设计方法: 1. 将策略1种生成的大量多肽进行大批量验证conformational energy landscape, 将存在2个或以上低能折叠态的序列选出。*(两个状态的能量差值在5 kcal/mol以内) 1. 对于折叠态大于5 kcal/mol的case,使用Rosetta multi-state的设计方法同时优化两个状态的序列,使得这些序列结构的能量相似。 1. 从晶体结构出发,引入不稳定的突变,并重复方法1的过程。
三、实验
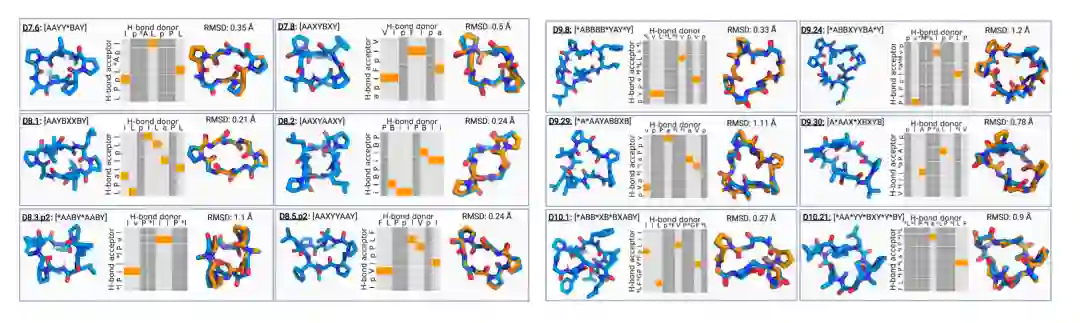
通过化学合成法和高效液相色谱进行纯化,经过NMR解析这些被选中的环肽的序列结构与设计几乎一致(RMSD<1.0)。
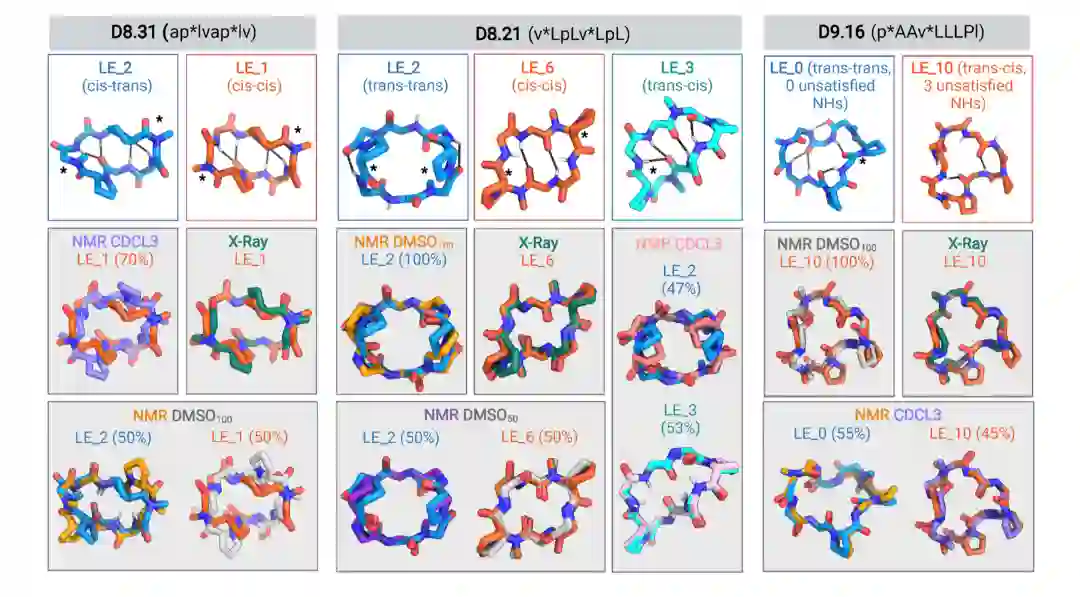
基于变构效应的透膜环肽同样,分别在溶液和DMSO中都折叠成了目标的状态:
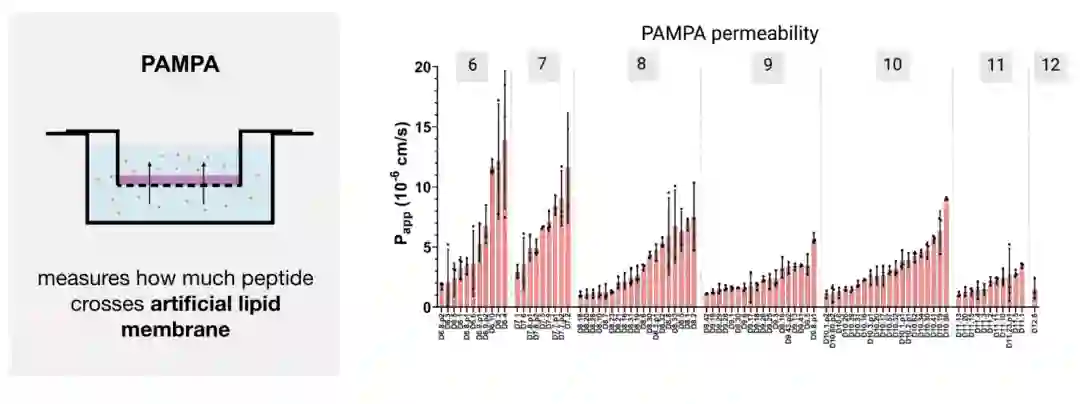
通过进一步实验检测环肽分子的透膜能力,作者使用了一种基于人工膜自由扩散的检测方法(PAMPAs),实验结果显示长度为6-8个氨基酸的多肽具有良好的透膜特性(>10E-6 cm/s)。表明最大化环肽内部的氢键饱和度,有利于环肽进行透膜!但透膜性和环肽的长度存在trade-off。
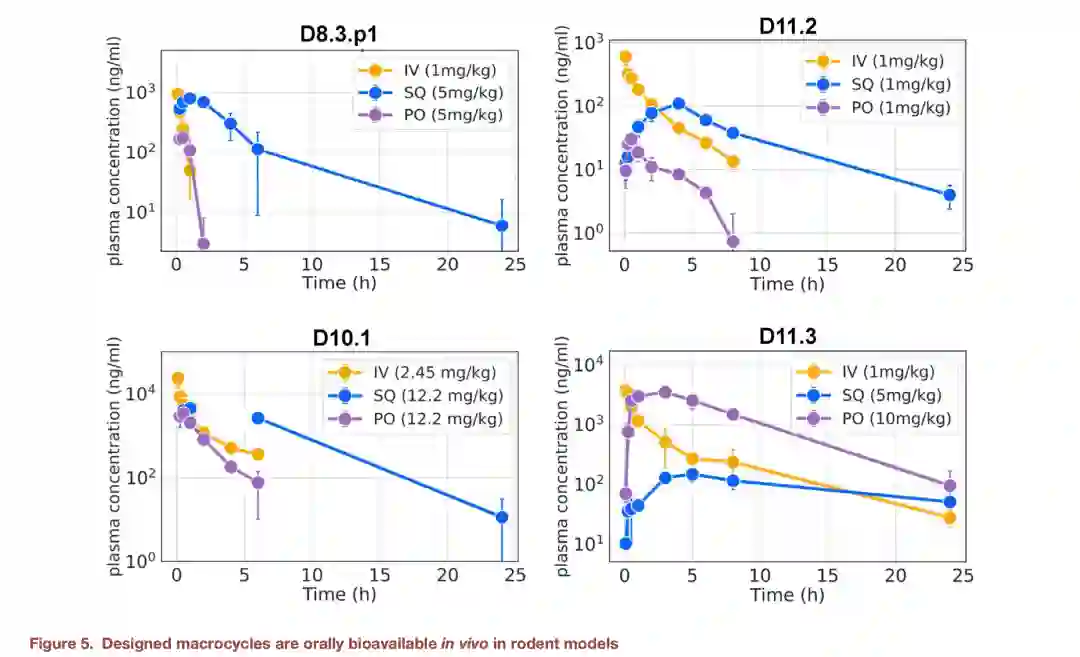
口服利用度测试:所有四种设计的环肽其口服生物利用度比大多数其他天然口服吸收肽更高(7.5% and 11%)。更加值得注意的是D11.3的利用度高达40%,并且其半衰期达到了5.58个小时,是良好的药物候选序列。
点评
本次研究很好地验证了减少极性基团来增加透膜性的概念,为后续进行功能化残基的移植提供了许多高精度的支架模板。但是环肽采样方法上并没有特别重大的改进。笔者认为变构环肽的设计算法还有很大的提升空间,可以在采样阶段就进一步考虑变构效应的影响。 参考文献: Bhardwaj G, O’Connor J, Rettie S, et al. Accurate de novo design of membrane-traversing macrocycles[J]. Cell, 2022.