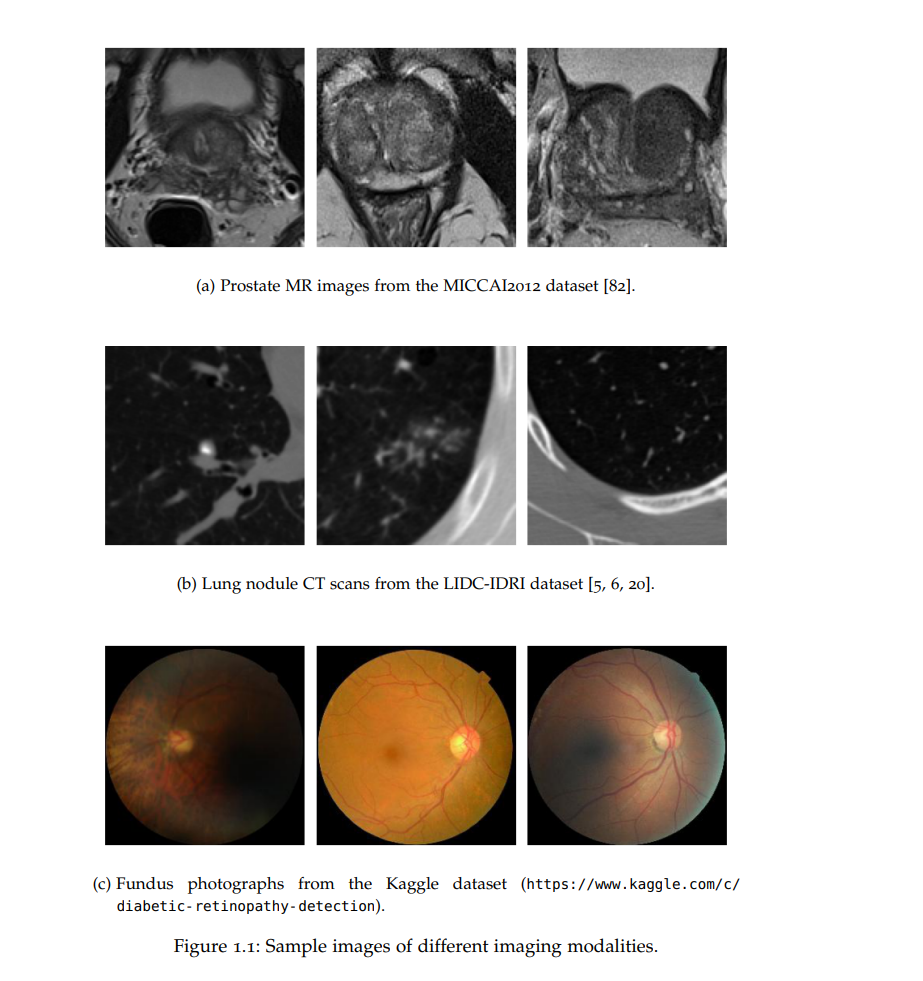
**本文共分为4个独立章节,分别研究面向医学图像分割与重建的不确定性量化方法、面向生存分析的鲁棒深度模型和新的灰盒对抗防御算法。**该论文结合了理论和实证结果,包含了医疗健康中的两个应用,即医学图像分析和生存分析。**在第3章和Hu et al.[54]中,提出了一种新的医学图像分割的监督不确定性量化方法。利用多级标注的可变性作为"基础真相"偶然不确定性的来源,并将其视为监督学习问题中的目标。**我们将这种基本事实的不确定性与概率U-Net[69]相结合,并在LIDC-IDRI肺结节CT数据集[5,6,20]和MICCAI2012前列腺MRI数据集[82]上进行测试。我们发现,我们能够改进预测的不确定性估计。我们还发现可以提高样本精度和样本多样性。**在第4章和Hu、Pezzotti和Welling[53]中,我们提出了一种新方法,可以准确评估医学图像重建模型的预测精度。**首先,通过将预测误差分解为随机误差和系统误差,证明当前方法估计的预测不确定性与预测误差不高度相关,并表明前者等价于随机误差的方差。目前的方法通过修改模型结构和训练损失来联合估计真实目标和数据的不确定性,从而不必要地损害了性能。分别估计它们而不进行修改可以提高性能。接下来,建议分两步估计目标标签和预测误差的大小。在一个大规模的MRI重建数据集[127]上展示了所提出方法,取得了比最先进的不确定性估计方法更好的结果。
**在第5章和Hu等人的[51]中,我们提出了一种基于transformer的鲁棒生存模型,该模型估计了患者特异性生存分布。**我们的贡献是双重的。首先,到我们发表[51]为止,深度生存模型使用全连接或循环神经网络,我们是第一个将Transformer[120]应用于生存分析的人。此外,我们使用序数回归来优化随时间推移的生存概率,并惩罚随机的不协调对。其次,许多生存模型仅使用排序指标进行评估,如一致性指数[45]。本文还建议使用绝对误差指标,来评估对被观察对象的精确持续时间预测。在两个公开的真实世界数据集上展示了所提出的模型,表明所提出模型的平均绝对误差结果明显优于当前模型,同时,在一致性指数下确定最佳模型是具有挑战性的。
在第6章和Hu, Nalisnick, and Welling[52]中,我们提出了一种新的灰盒对抗防御算法,该算法可能用于一些安全敏感的应用。在对抗样本的文献中,白盒和黑盒攻击受到了最多的关注。假定敌手对防御者的模型有完全(白色)或没有(黑色)访问权限。在本章中,我们关注同样实用的灰框场景,攻击者只掌握部分信息。我们的防御假设除了私钥之外的一切都将被攻击者使用。该框架使用离散化的Baker映射[34]进行图像去噪和加密。对使用各种梯度制作的对抗性图像(如FGSM [39], PGD[86])进行的广泛测试表明,所提出的防御在CIFAR-10和CIFAR-100上取得了比最先进的灰盒防御在自然和对抗性精度方面都更好的结果。