利用放射同位素标记的红细胞来源的外泌体模拟物进行体内非侵入性成像
外泌体是天然的纳米尺寸的膜囊泡,由于它们作为药物递送载体的潜力而引起了研究人员的兴趣。虽然外泌体是有效的药物载体,但它们的产生和体内生物分布仍未完全阐明。来自Kyungpook大学的研究人员分析了来自红细胞(RBC)的外泌体模拟物(exosome mimetics,EMs)的产生以及用于体内成像的放射性同位素标记RBC-EM。来自RBC的工程化EM通过一步法大规模生产,并通过密度梯度离心进一步纯化。 RBC-EMs用锝-99m(99mTc)标记。非侵入性成像,是在小鼠中注射99mTc(游离)或99mTc-RBC-EM,并通过γ相机成像分析它们的生物分布。然后处死动物,收集器官用于进一步的生物分布分析。 RBC-EM具有与RBC外泌体类似的特征,但就粒子数而言具有高于普通外泌体130倍的产率。 99mTc-RBC-Ems在两小时内的放射化学纯度几乎为100%,3小时降至97%。放射性标记不影响RBC-EM的大小和形态。与游离99mTc相比,99mTc-RBC-EMs在小鼠体内成像显示肝脏和脾脏中的摄取更高,并且甲状腺中没有摄取。离体成像也证实了体内的这些发现。此外,荧光成像证实了同位素成像结果。免疫荧光成像显示,RBC-EMs的肝摄取由库普弗细胞(驻留肝的巨噬细胞)显著介导。这些结果证明了用于新型RBC-EM的简单而大规模的生产方法,其可以用99mTc有效地标记,并且通过同位素成像在体内可行地监测。 RBC-EM可用作体内药物递送载体。
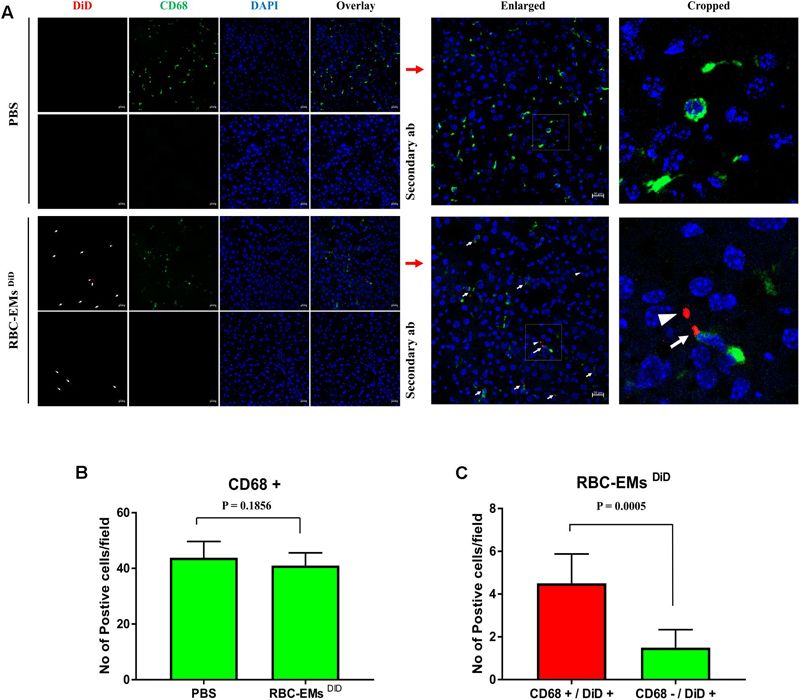
图:小鼠肝脏中RBC-EMs的荧光标记细胞的可视化。
(A)RBC-EMs DiD(红色)和CD68(绿色)在所述小鼠肝脏中的代表性共聚焦图像。(B)对来自PBS和RBC-EMsDiD注射的小鼠的肝脏的共聚焦图像中的CD68细胞的定量计数并以条形图表示。
(C)对从小鼠的肝脏中具有或不具有CD68(绿色)的RBC-EMsDiD(红色)的细胞共聚焦图像的定量进行计数并以条形图表示。
参考文献:
Gangadaran P, Hong CM, Oh JM, Rajendran RL, Kalimuthu S, Son SH,Gopal A, Zhu L, Baek SH, Jeong SY, Lee SW, Lee J, Ahn BC. (2018) In vivo Non-invasive Imaging of Radio-Labeled Exosome-Mimetics Derived From Red Blood Cells in Mice. Front Pharmacol 9:817.
科研学习班了解一下~ ~(点击详细了解):
不做实验,不写meta分析,用这个方法轻轻松松发多篇SCI论文
回复“外泌体” 阅读外泌体最新科研进展及动态
回复“EV” 阅读 2016-2018年This Week in Extracellular Vesicles
回复“盘点” 阅读 外泌体领域十大前沿进展盘点