PNAS又一重磅!揭秘CAR-T疗法及副作用路径!有望治疗实体瘤!
点击上方“转化医学网”订阅我们!
干货 | 靠谱 | 实用
导 读
CAR-T疗法近些年来大热,虽然它目前只能治疗血液系统的疾病,但这并不妨碍人们在其他领域对它的探索。发表在PNAS上的一篇研究揭示了CAR-T及其副作用的机制。这将有助于我们开展对实体瘤的治疗。
CAR-T细胞疗法是一种新型的免疫治疗形式,它将患者自体的免疫T细胞提出后经过基因改造再重新回输至患者体内,经改造后的免疫T细胞可有效的针对性杀死癌细胞。目前该疗法已经由FDA于2017批准,用于治疗血液系统的肿瘤,如儿童白血病和某些淋巴瘤。
而2月12日发表在《PNAS》,题目为“Intensity and duration of TCR signaling is limited by p38 phosphorylation of ZAP-70T293 and destabilization of the signalosome”的研究揭秘了CAR-T疗法能够快速靶向癌细胞并将其杀死的关键机制,并解释了该疗法为什么会导致严重的副作用。
机体内适应性免疫应答是由T细胞增殖、分化并被激活后发挥效应。其中生理性T细胞的活化主要是通过T细胞受体(TCR)和抗原递呈细胞提供的肽/ MHC复合物共同诱导形成的。
Walter和Eliza Hall医学研究所的Misty Jenkins 博士及其团队通过研究CAR-T细胞如何与癌细胞相互作用中发现了酪氨酸激酶ZAP-70对T细胞抗原受体(TCR)信号的启动具有至关重要的作用。
由TCR信号激活的丝氨酸激酶p38,则直接反过来磷酸化其上游的络氨酸激酶ZAP-70。这一负反馈就会降低TCR信号复合物的大小和寿命,限制了T细胞的免疫反应,破坏了其稳定性。
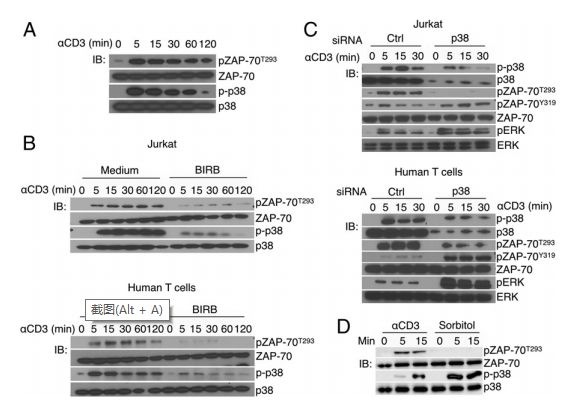
p38在体外和TCR激活的T细胞中磷酸化ZAP-70
Misty Jenkins博士说:“我们发现CAR-T细胞受体具有快速识别和鉴别那些在免疫系统中仍未被检测到的肿瘤细胞,并立即杀死它们。之前我们就已经证明细胞因子的产生与免疫细胞锁定在癌细胞上的时间有关,细胞接触的时间越长,产生的细胞因子就越多,从而导致炎症的程度越来越高。”
目前Misty Jenkins博士和她的团队正在集中研究如何用CAR-T疗法治疗脑癌。脑癌拥有较差的存活率,并对传统治疗,化疗等有抵抗性,而手术切除也会带来大量的附加伤害。CAR-T治疗或许能为脑癌的治疗提供新的思路。
同时,Misty Jenkins博士在2017年获得了脑癌基金会及儿童基金会的资助,支持她继续开展免疫疗法治疗脑癌患儿。
参考文献:
1.Cancer killing clue could lead to safer and more powerful immunotherapies.
2.Maria Letizia Giardino Torchia el al., "Intensity and duration of TCR signaling is limited by p38 phosphorylation of ZAP-70T293 and destabilization of the signalosome," PNAS (2018).
转化医学领域核心门户
识别图中二维码,点击关注
投稿、应聘医学编辑:
微信:vipmed360
商务合作
微信:zhyxkf
END
转折点——生物医药招聘第一平台