黄媚娟教授点评:对FDA获批的F1CDx采用单基因伴随诊断进行临床和分析性验证
一个标志物要获批用于伴随诊断(CDx),必须对靶向治疗和免疫治疗的疗效具有非常好的预测价值,因此,任何一个用于检测这些标志物的新的检测手段需要经过严格的分析性和临床验证。基于NGS的全面基因组分析(CGP)平台FoundationOne CDx (F1CDx) ,在开发时就严格遵循FDA CDx适应症的规定。在2018年10月份召开的ESMO大会上,Foundation Medicine详实地公布了采用单基因伴随诊断检测方法,从临床和分析性验证两方面评估F1CDx平台。
方法
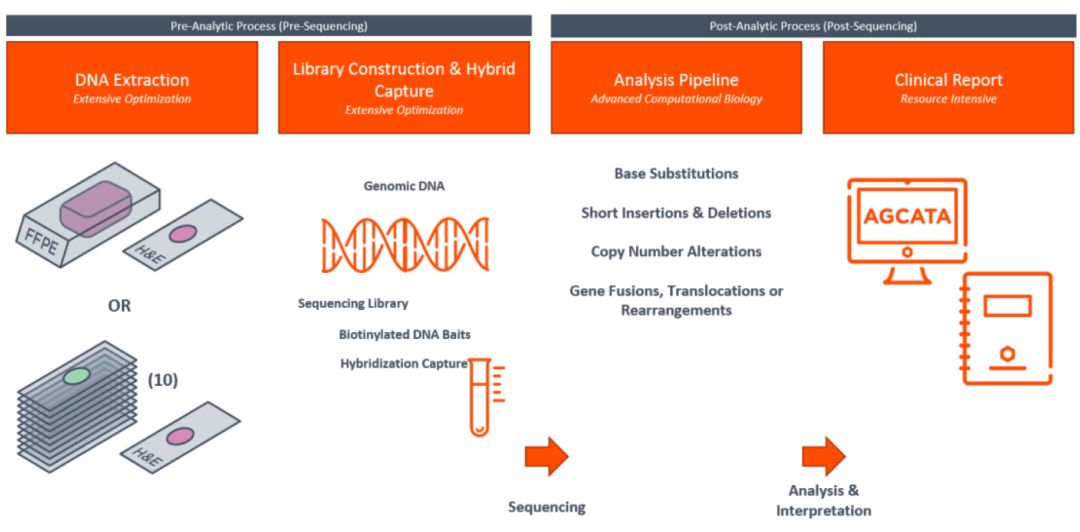
提取FFPE肿瘤组织的DNA,构建全基因组文库,采用Illumina HiSeq 4000平台进行测序。对324个测序基因数据进行分析,旨在发现碱基置换、插入或缺失、拷贝数变异、基因重排、微卫星不稳定性(MSI)和肿瘤突变负荷(TMB)。
图1. FoundationOne CDx(F1CDx)分析流程
结果
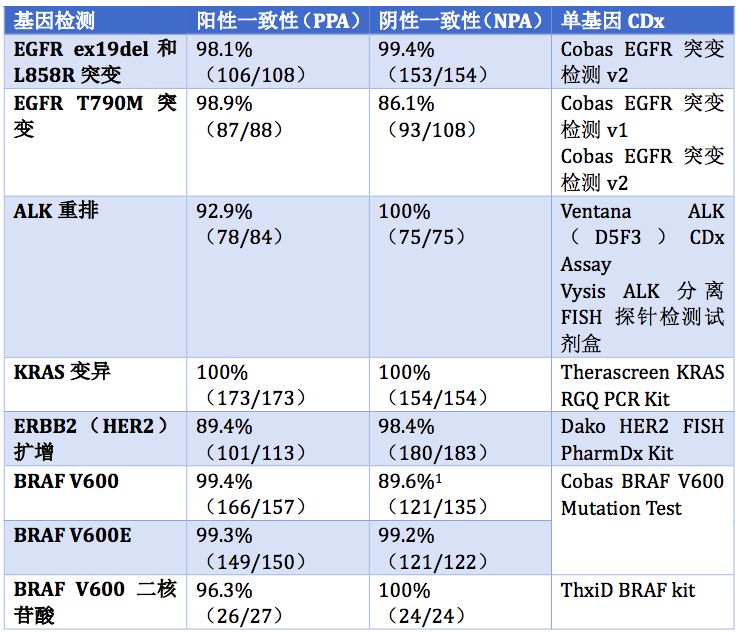
对F1CDx与单基因伴随诊断进行非劣效性验证,单基因伴随诊断包括EGFR cobas检测、BRAF突变检测、FISH和IHC检测ALK重排、FISH法检测ERBB2扩增和其他。评估两个检测方法的阳性一致性(PPA)和阴性一致性(NPA),总结见下表1。
表1. 对FDA获批的F1CDx采用单基因伴随诊断进行临床验证
备注:1. BRAF V600K和V600E二核苷酸检测的敏感性在cobas 检测中显著更低,尤其是在F1CDx可以检测MAF最低40%的二核苷酸变异时,因此导致两种检测方法之间NPA值较低。
2、F1CDx检测所有基因变异形式的分析敏感性(LoD)
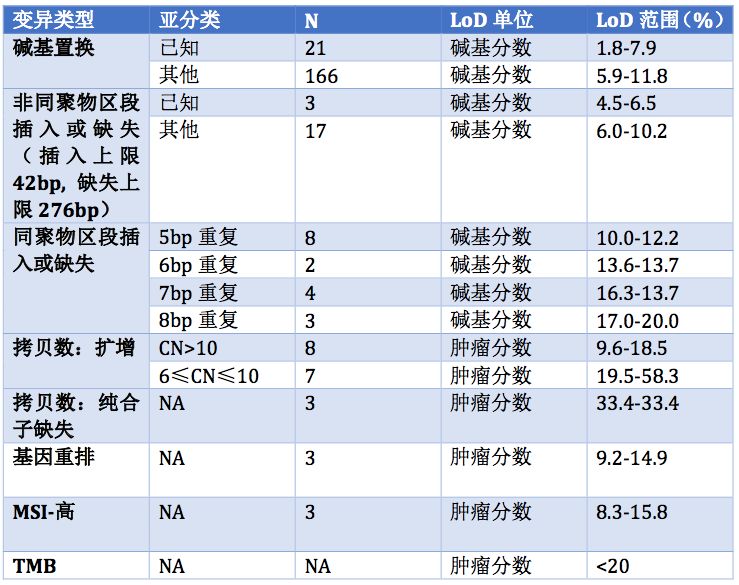
下表2显示了F1CDx检测所有基因变异形式的分析敏感性(LoD)。
表2. F1CDx检测所有基因变异形式的分析敏感性(LoD)
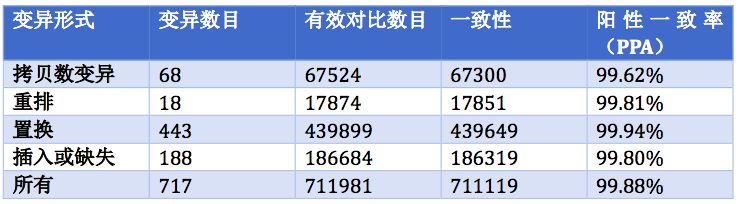
3、F1CDx的分析精准性(不同检测方法和不同批试剂的可重复性)
表3. F1CDx的分析精准性
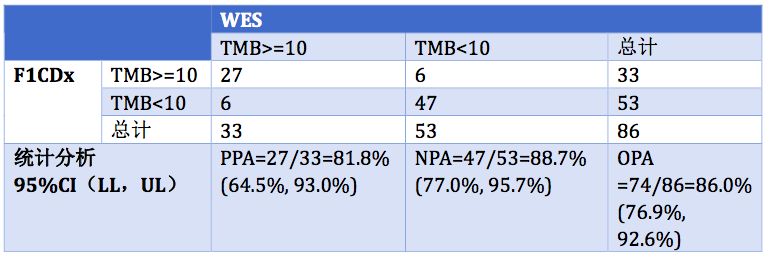
4、以TMB 10mut/Mb作为cutoff值,F1CDx与全外显子测序的分析一致性
86例标本同时接受了F1CDx和全外显子检测,其中全外显子检测覆盖的编码外显子大小为34.7Mb。
表4. 以TMB 10mut/Mb作为cutoff值,F1CDx与全外显子测序的分析一致性
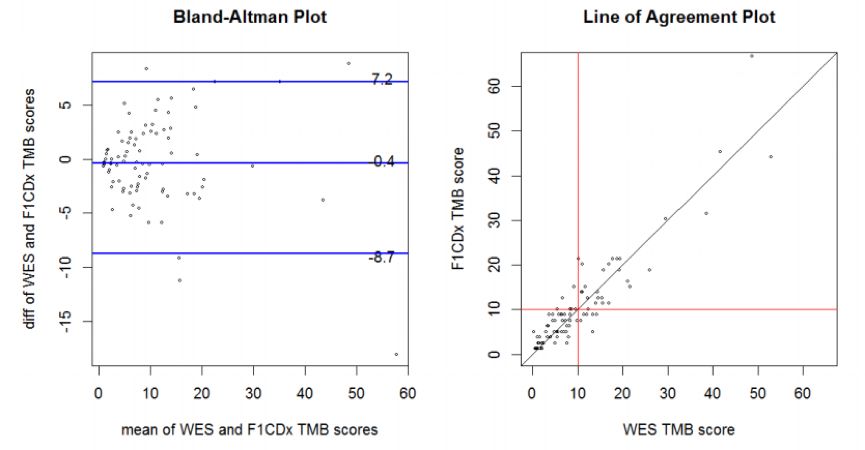
图2. F1CDx TMB评分与全外显子测序TMB评分的分析一致性
5、接受F1CDx检测的肿瘤类型分类
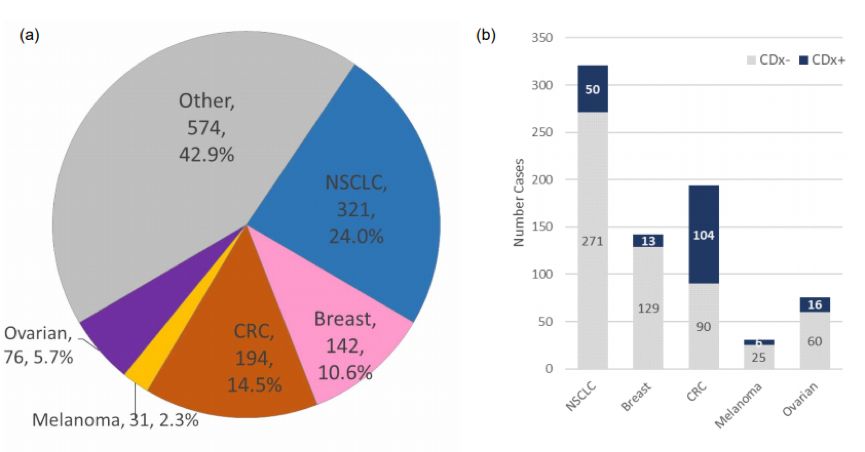
接受F1CDx临床检测的患者,57%属于有CDx的肿瘤,其中NSCLC最常见,占24%,不同瘤种占比分布见下图3。不同瘤种患者中,拥有CDx变异的患者比例分布为:NSCLC(15.6%)、乳腺癌(9.2%)、结肠癌(53.6%)、黑色素瘤(19.3%)、卵巢癌(21.1%)。在结肠癌患者中,46.4%携带CDx变异的患者适合接受治疗。在乳腺癌患者中,CDx变异患者比例较低的原因可能是患者接受了FISH或IHC检测,因此未送检F1CDx检测。
图3. (a)接受F1CDx检测的肿瘤类型分类;(b)CDx阳性的患者数量
6、所有瘤种的常见变异基因
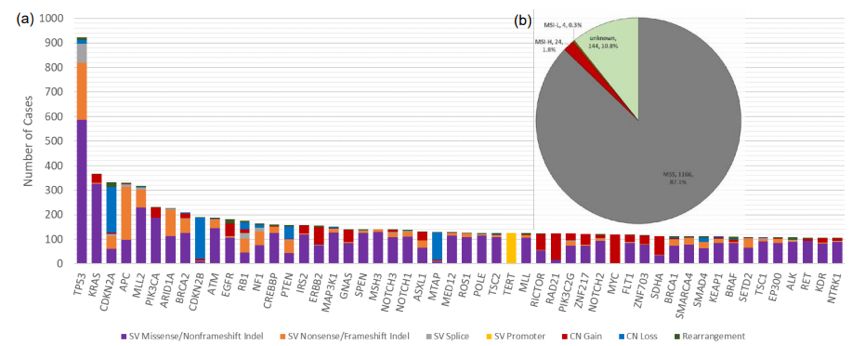
在所有瘤种的变异基因中,最常见的为TP53和CDKN2A变异,KRAS和APC变异在结直肠癌中更常见,见图4A;对MSI-H的24例患者进行单独分析,10例为结直肠癌,3例为子宫内膜癌。
图4. 所有瘤种的常见变异基因分布
7、TMB评分分布
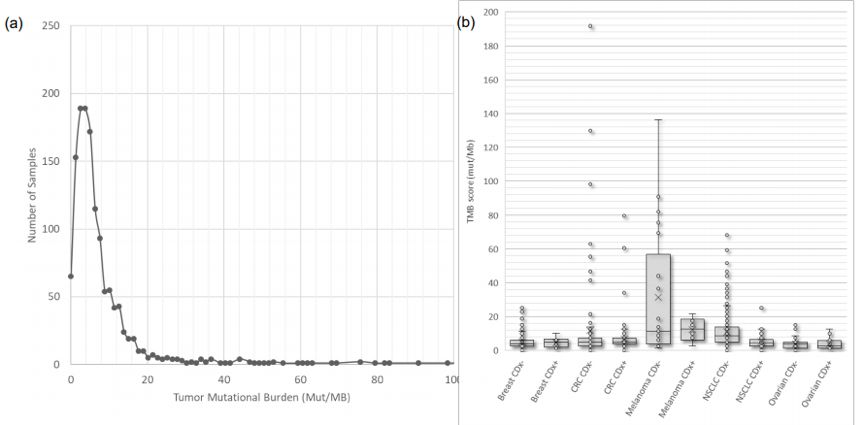
大多数治疗中,TMB为3-4mut/Mb,仅少数患者为高TMB,不同患者的TMB评分分布见下图5A;CDx阳性的不同瘤种患者的TMB评分分布见下图B。相比于CDx阳性的患者,仅在NSCLC患者中观察到CDx阴性患者的TMB显著更高。
图5. (a)所有患者中的TMB分布;(b) CDx阳性的不同瘤种患者的TMB评分
结论
Foundation Medicine研发了第一个基于NGS的全面伴随诊断检测平台——F1CDx,在实体瘤中进行了广泛的临床和分析性验证,并获得FDA批准用于伴随诊断。F1CDx平台目前已经在5个瘤种,8个伴随诊断适应症,包含17个靶向药物的伴随诊断方法中进行了临床验证。F1CDx在不同瘤种中的分析性平台已经建立。此外,研究还发现采用F1CDx检测和全外显子检测的TMB评分高度相关。最初验证的1338例临床患者覆盖不同的疾病类型,包含不同的CDx变异形式,以及MSI-H和TMB高的患者,这一研究证实F1CDx检测结果可以指导患者治疗。
专家点评
博士,博导
华西医院胸部肿瘤科副主任
四川省肿瘤学会副理事长
四川省肿瘤学会肺癌专委会主任委员
中国医药生物技术协会纳米技术分会常务委员
CSCO(中国临床肿瘤协会)中青年委员会委员
CSCO 非小细胞肺癌专委会委员
四川省靶向治疗专委会常委
四川省免疫学会肿瘤免疫专业委员
IASLC(国际肺癌协作组)成员
国家自然基金评审专家,科技部评审专家
肺癌靶向治疗已经走过10余年历程,临床应用已经非常成熟了,随着越来越多治疗靶点的发现和靶向治疗药物的应用,我们已经走进精准肿瘤治疗时代。靶向治疗,顾名思义,需要有精准的靶点,即携带某种基因变异的肿瘤患者才能接受这类治疗。目前获批的靶向治疗药物,在获得FDA批准上市时,通常都同时获批了相应的伴随诊断平台,如EGFR突变的Cobas 检测,ALK重排的FISH分离探针等。但随着越来越多治疗靶点的发现以及靶向药物的应用,传统的单基因检测模式已经不能很好满足临床需求,国内外指南均推荐应用多基因检测平台,同时覆盖多个已经获批的伴随诊断,从而实现高效检测。F1CDx是FDA和CMS批准的首个经过临床验证的NGS伴随诊断(CDx),这一平台在获批之前经过了严格的临床和分析性验证,证实了F1CDx平台的检测效能,可以作为临床多基因检测的首选之一。
Clinical and analytical validation of an FDA approved comprehensive genomic profiling (CGP) assay incorporating multiple companion diagnostics for targeted and immunotherapies. 2018 ESMO, 79P.
41本肿瘤患者指南丛书
点击下方图片即可免费阅读
70个肿瘤相关临床试验招募患者
点击下方图片或识别图片二维码即可查看详情