专家点评
【1458】【病例点评】一个RAS野生mCRC病例引申的问题:一线维持跨线整体治疗策略
上期回顾:
【病例讨论】一个RAS野生mCRC病例引申的问题:一线维持跨线整体治疗策略
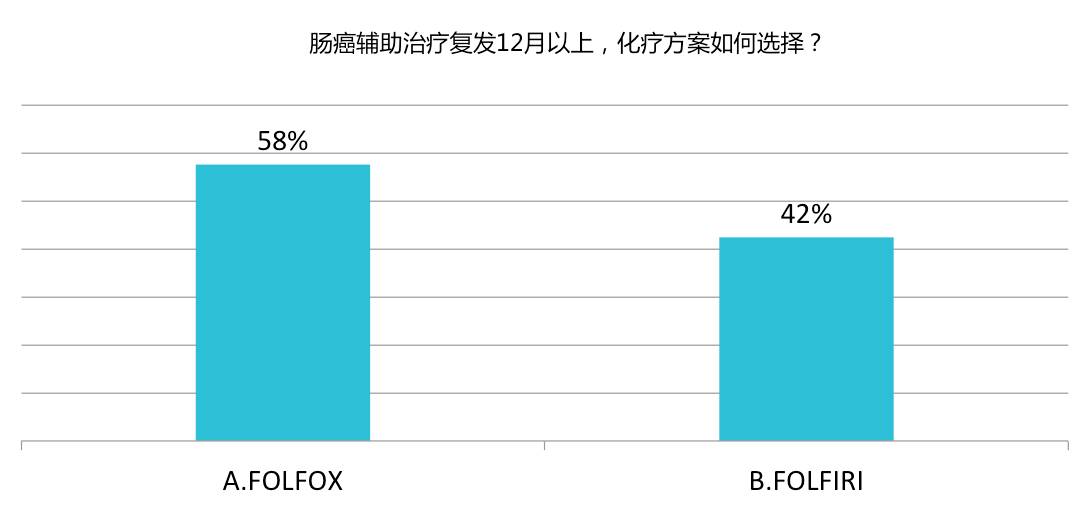
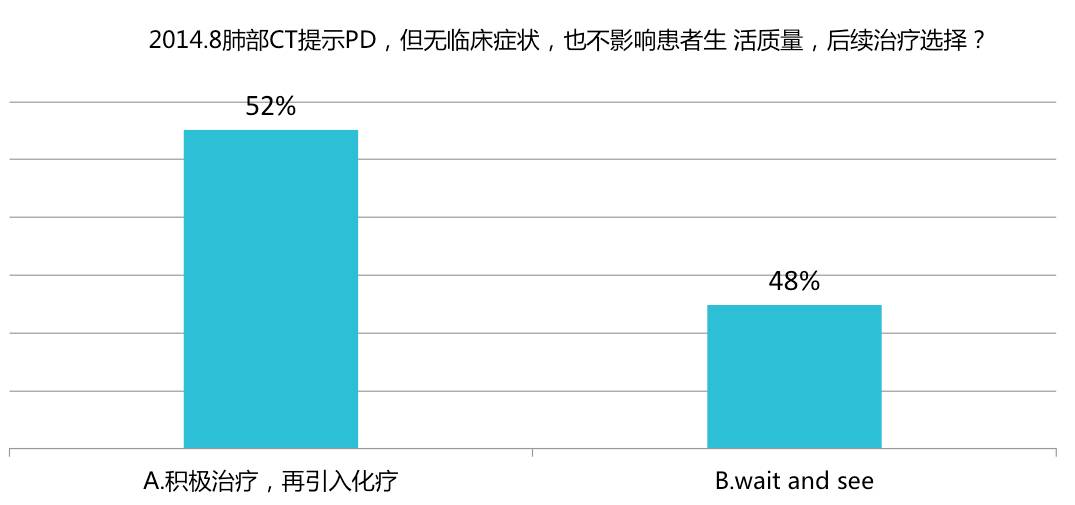
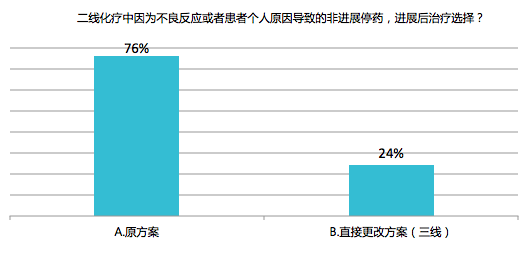
投票结果:
北京肿瘤医院消化内科副主任
主任医师 医学博士 硕士生导师
中国医师协会外科分会MDT专委会常委
中国抗癌协会大肠癌专业委员会青委会副主任委员
CSCO青年专家委员会委员
中华医学会肿瘤分会青年委员
中国抗癌协会化疗专业委员会青年委员
《中国结直肠疾病电子杂志》编委
《Annals of Oncology》胃肠道肿瘤中文版编委
1. 患者双肺多发转移(至少多于6枚),原则上属于不可切除的发展相对缓慢的转移性结肠癌;患者治疗原则以控制疾病为主,延长生存时间,同时保持生活质量,该患者采取了联合化疗与维持治疗的结合方式,最终获得了较长的生存与较好的生活质量,整体治疗是成功的。
2. 患者病史描述提到了骨扫描颈椎与左骶髂关节代谢活跃,后期未描述是否排除骨转移
3. 患者如排除骨转移与锁骨上淋巴结转移,仅有双肺转移,目前病灶数目可能>6个,尽管不属于寡转移定义,但依旧属于在化疗基础上,可进行局部治疗的范畴;该患者后期随访提示生物学行为相对较好,同时该患者肺转移可考虑给予SBRT、射频消融等治疗,或许对生存的改善能提供进一步的益处。当然,局部治疗时机的选择是非常关键的。
专家点评
中国医师协会肿瘤分会青委
中国医师协会康复分会中西医结合康复专委会委员
浙江省医学会肿瘤分会委员
浙江省医学会精准医学分会委员
浙江省抗癌协会肿瘤内科专业委员会青委
浙江省数理医学学会数理医学平台副主任委员
浙江省肿瘤防治联盟结直肠癌专委会副主任委员
医生对恶性肿瘤的诊治应该从接诊的那刻起就贯穿全程管理的理念,以期获得最大的生存获益和最佳的生活质量,其中很重要的一个任务就是降低治疗对生活质量的影响。而要达成这个目标,应该落实以下几个原则:
1.要有全局性观念;2.要关注各类细节;3.要考虑各种因素;4.要有前瞻性思维;5.诊治实施过程中应严格按计划实施;6.视病情变化及治疗毒性进行相应调整。mCRC的治疗是一项系统工程,具体说来,全程管理要遵循以下路径:进行特征评估和患者意愿评估→与患方一起确定治疗目标→结合医生的经验、循证证据和医院的实际情况选择治疗的手段→制定切实可行的治疗计划→根据计划斟酌治疗的细节→严格按计划落实治疗→定期进行疗效评估,随时进行毒性评估,还需要评估疗效和毒性变化对患者依从性和心理的影响→根据疗效、毒性、依从性和疾病状态等调整治疗。这个路径不论在初始治疗期还是后线治疗期间均应遵从。
以目标为导向的治疗是mCRC全程管理的主线。在全程管理过程中,医者需要考量无数的问题,比如:不同目标实施中的考量因素有哪些、患者肿瘤的生物学行为如何、能否达成R0切除或NED、各线治疗方案如何规划、初始治疗方案及靶向药物如何选择、如何进行毒性的全程管控(减毒治疗模式)、系统(全身)治疗与局部治疗如何有序安排等等,这些因素的考虑都是个体化诊治的需要。其中,内科治疗过程中如何降低毒性是重要的一个内容。
mCRC的临床研究发展大致遵循了两个目标:一是引入新药、新方法等如何提高治疗疗效;二是通过治疗方法的改进和基于分子检测等如何降低毒性。根据现有的循证医学主要证据(Ⅲ期临床研究),减轻毒性的策略无非有以下几种:1.维持治疗策略(诱导维持再引入);2.间歇治疗策略;3.单药序贯治疗策略;4.个体化治疗剂量策略。在实践过程中,还有不少医生选择依据毒性加强支持治疗、根据毒性减低药物治疗剂量、疗前相关基因检测(DPD酶、UGT1A1等)指导药物剂量选择、节拍化疗策略等。这些策略的实施在一定程度上使患者能在维持疗效的前提下尽可能的降低毒性,保持有效治疗的持续性。作为患者治疗的实施者,医生总希望诊治实施过程的每一步都有高级别的循证医学证据支持,但遗憾的是临床问题太多,而证据太有限。因此,在治疗实施过程中,根据现有证据提供的理念实施治疗和将患者纳入MDT管理是非常重要的。
本例系年轻老年右半结肠癌女性患者、RAS和BRAF基因野生、有一定症状、不可切除、体力状况较好,初始治疗时选择标准的FOLFIRI+BEV方案达到了较好的缓解,并获得较长的PFS,虽然该方案如何维持治疗无证据,但在实际治疗中引用了OPTIMOX 1研究的理念,有效降低了毒性。在其后的后线治疗中,面对同样的情况,也引入了该理念,达到较好的治疗依从性。当然,在初始治疗时选择CAPOX联合贝伐单抗的方案会更符合循证医学证据。
专家点评
主任医师 硕士生导师 教授
温州医科大学附属第一医院 放化疗科
浙江省医学会肿瘤学分会委员
此病例中,根据患者①手术病理:右半结肠溃疡型中分化腺癌,淋巴结2/20只癌转移;②2013年1月胸部CT及气管镜下活检病理提示两肺多发转移,因此其“右半结肠癌手术化疗后双肺转移,rpT3N1bM1a,ⅣA期”诊断是明确的。那么对于该患者的转移性结直肠癌(mCRC)来说,其一线二线三线四线的治疗方案该如何选择呢?
一线治疗:
CALGB/SWOG 80405 研究显示,对于 KRAS 野生型转移性结直肠癌(mCRC),一线 FOLFOX 或 FOLFIRI 方案联合贝伐珠单抗(Bev)或西妥昔单抗(Cet)在 OS 和 PFS 方面均无显著差异。后续的回顾性分析发现,右半结肠肿瘤患者一线接受 BEV 治疗相比 Cet 显示出更好的生存获益(24.2月与16.7月),这主要与左右半结肠的胚胎起源不同导致二者的分子生物学特征上差异有关。其他如FIRE-3等研究均证实了Bev在右半结肠获益显著高于Cet。而V308试验则比较了一线FOLFOX序贯二线FOLFIRI与一线FOLFIRI序贯二线FOLFOX的疗效差别,两组的一线治疗缓解率(RR,54% vs 56%)、中位总生存期(mOS,20.6月 vs 21.5月)均无统计学意义的差异,而二线的RR(4% vs 15%)与mPFS(2.5月vs4.2月)则以后者为高。因此从二线治疗的疗效考虑,以先用FOLFIRI序贯FOLFOX为佳。综上所述,该患者的一线治疗方案为FOLFIRI+Bev是最佳的选择。
维持治疗:
基于药物的毒性作用及患者的耐受情况,目前的维持治疗模式主要有维持治疗、间歇治疗、持续治疗。其中通过对比不同模式的疗效及毒性,维持治疗得到各大指南的一致推荐。目前不可切除的mCRC后续的维持治疗多推荐低毒的化疗联合靶向治疗,Stop and Go、CAIRO3等研究表明,Bev联合卡培他滨维持证据最为明确。
二线治疗:
患者于2014-8-13CT两肺病灶进展,应该进行二线治疗。首个跨线治疗的多中心随机对照TML研究证实了Bev跨线治疗可为mCRC患者带来确切的PFS和OS获益。因此方案可为FOLFOX+Bev。
三线治疗:
BOND1研究入组了CPT-11治疗失败的患者(包括二线、三线患者),随机分为Cet单药组和CPT-11+Cet 组,结果显示CPT-11+Cet 组较Cet单药组有更好的疗效:RR 22.9% vs 10.8%,TTP 4.1月vs 1.5月。而EPIC试验则入组了一线L-OHP+5FU治疗失败的患者,随机分为CPT-11单药组和CPT-11+Cet 组,提示Cet明显提高了RR和PFS,OS无统计学差别。这两项研究均表明,KRAS 野生型mCRC的三线治疗可采用CPT-11+Cet。
四线治疗:
对于既往标准治疗均失败的难治性KRAS 野生型mCRC,除最佳支持治疗(BSC)外,其四线治疗或许可以尝试Cet单药靶向治疗(KRAS野生型)。目前的一些临床研究如CORRECT、CONCUR研究提示瑞戈非尼+BSC可延长患者OS和PFS,也不失为一个选择。
该患者的治疗过程中,个人认为有一小小不足之处:该患者有明显脊背疼痛症状,骨扫描提示下段颈椎代谢活跃,不能排除转移可能,应加做颈椎MR评估病情,必要时行病理明确。下段颈椎为承重骨,如有转移,要进行局部放疗。当然,在肿瘤的整体治疗中,患者的意愿、经济条件等都应作为我们医者选择治疗方案时应当考虑的因素。
19个肿瘤相关临床试验招募患者
点击下方图片即可查看详情