基本病史
美例秀秀|双靶联合,让乳腺癌无处遁形

第26例
现任中山大学附属肿瘤医院淋巴瘤首席专家
中华医学会肿瘤分会候任主任委员、肿瘤学分会淋巴瘤学组组长
中国抗癌协会化疗专业委员会常委
中国临床肿瘤学会(CSCO)中国抗淋巴瘤联盟副主席
CSCO执行委员会常委
中国老年肿瘤专业委员会副主任委员
中国南方肿瘤临床协作组织(CSWOG)主任委员
广东省抗癌协会肿瘤化疗专业委员会主任委员
广东省医学会肿瘤分会主任委员
国家自然基金评审专家、国家新药评审专家、国家医疗事故鉴定委员会委员,也是美国临床肿瘤协会(ASCO)、美国癌症研究协会(AACR)、美国血液肿瘤协会(ASH)和欧洲肿瘤学会(ESMO)会员,任多家中外期刊的副主编和编委。主要从事恶性肿瘤化学治疗、内分泌治疗和靶向治疗的临床研究和应用性研究。主持包括“863”计划、国家自然科学基金、广东省自然科学基金重点项目等多项科研基金和多项Ⅰ、Ⅱ、Ⅲ期多中心临床研究,已在专业杂志发表论文100多篇
中山大学肿瘤防治中心内科
主治医师、医学博士
2004—2012年就读北京协和医学院(清华大学医学部)八年制临床医学专业
擅长常见恶性肿瘤的诊治和内科治疗(化疗和靶向治疗)
患者女性,45岁,月经规律,孕1产1。2015年4月15日因“发现无痛性右腋窝肿块3日”就诊。既往体健,否认慢性病史、传染病史。
查体:一般状况良好,右锁骨上淋巴结可触及肿大,质硬,大小约1.5cm×1cm,右腋窝可触及多发肿大淋巴结,质硬,部分融合,最大直径约4cm。双乳视诊、触诊未见明显异常,乳头无溢脓溢液,余查体未见明显异常。
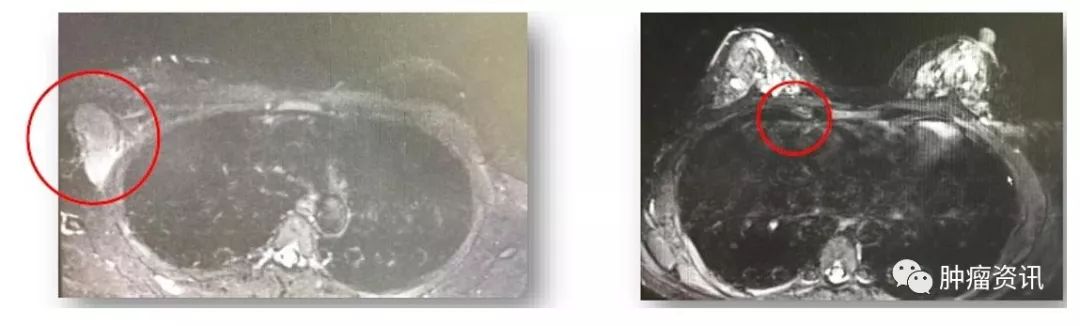
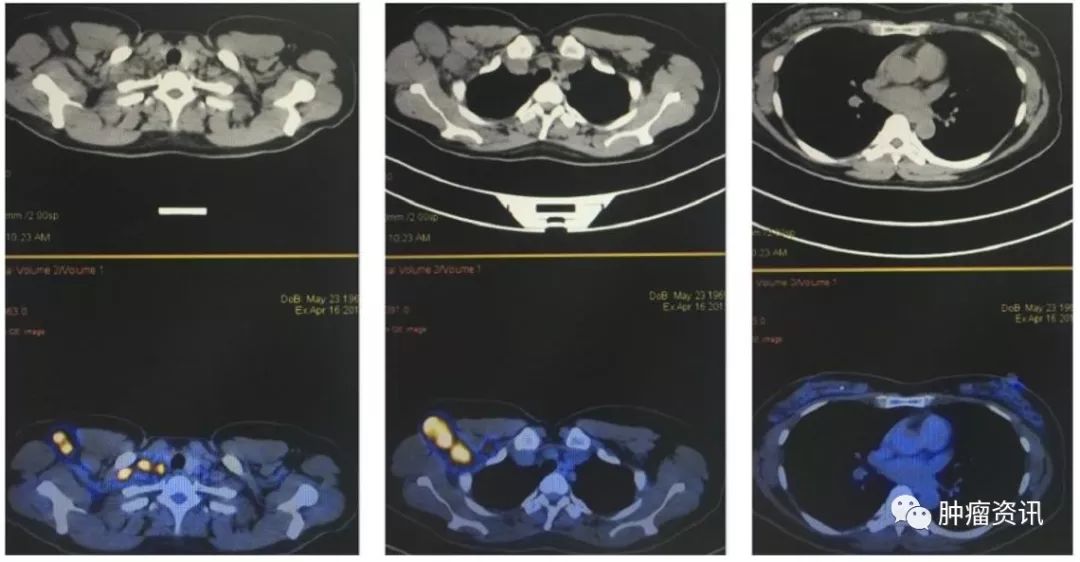
实验室检查:血肿瘤标记物:CA153 32.4U/ml,CA125 46.43 U/ml,CEA 5.92 ng/ml。乳腺MRI示(图1):右腋窝、右锁骨上肿大淋巴结,最大为38mm×38mm,强化明显,符合转移。右胸廓内动脉旁小淋巴结,9mm×8mm,强化明显,不除外转移。双乳可见直径为3~6mm多发小结节,等T1稍高T2信号,考虑为增生结节,余未见明显。颅脑MRI未见明显异常。PET-CT示(图2):右锁骨上、右腋窝多个肿大淋巴结,最大约为25mm×32mm,SUVmax为18,符合转移瘤,余未见明显异常。
图1 患者入院乳腺MRI
图2 患者入院PET-CT
诊疗经过
患者无明显禁忌,于2015年4月行超声引导下右侧腋窝淋巴结穿刺活检术。病理示:纤维组织中可见低分化腺癌浸润,结合免疫组化结果,考虑为乳腺来源(浸润性导管癌Ⅲ级)。
免疫组化:ER(-)、PR(-)、HER2(3+)、Ki-67(25%+)。
诊断
乳腺浸润型导管癌Ⅲ级并右腋窝、锁骨上淋巴结转移(cTxN3cM0 Ⅲc期)。
分子分型:HER2阳性HR阴性。
新辅助治疗
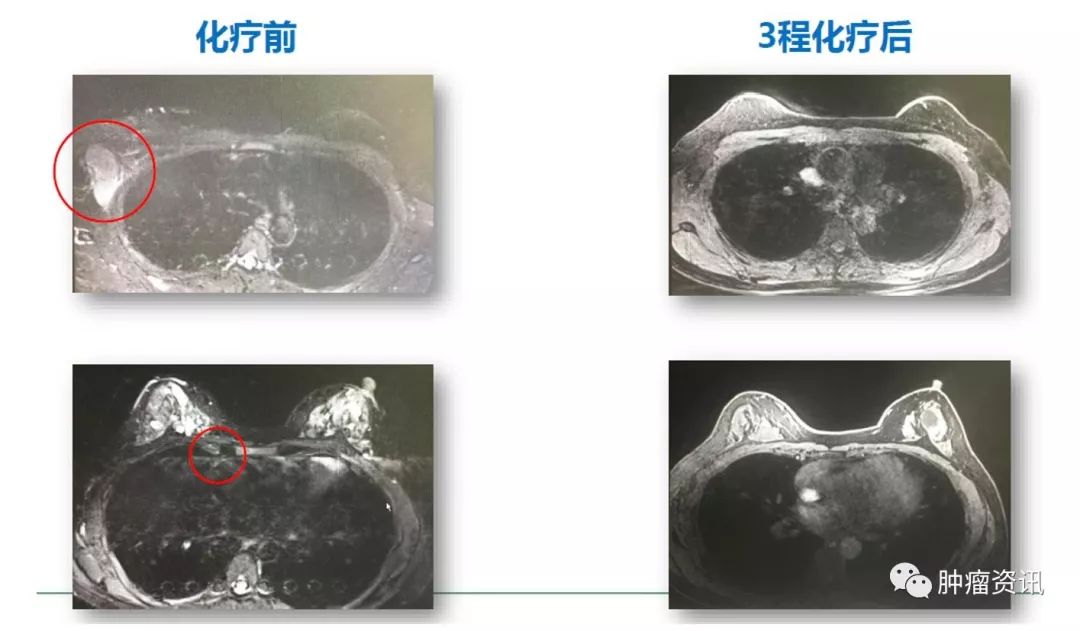
化疗联合靶向治疗:于2015年4月20日至6月8日,行FAC方案3周期,同时联合曲妥珠单抗。复查评估乳腺MRI示(图3):右腋窝、右锁骨上淋巴结肿大,部分融合,大小为38mm×20mm,强化明显,右胸廓内动脉旁小淋巴结大小为4mm×3mm,双乳多发小结节,考虑为增生结节,较前相仿。
图3 患者治疗后乳腺MRI
于2015年7月6日起行多西他赛联合曲妥珠单抗1周期,同时口服拉帕替尼1000mg qd,服药后3日出现三度腹泻,遂将拉帕替尼减量至500mg qd。但后续出现三度腹泻和四度中性粒细胞缺乏,故予以停药。
于2015年8月4日至9月21日行多西他赛联合曲妥珠单抗、帕妥珠单抗治疗3周期,治疗过程顺利。复查PET-CT提示影像学完全缓解。
手术治疗
患者于2015年10月19日行右乳改良根治术+右颈部择区淋巴结清扫术。
病理示:乳腺、乳头、皮肤未见癌,乳腺呈腺病样改变,大量纤维增生并炎症细胞浸润,符合治疗后改变。腋窝淋巴结可见转移癌:2/10,肌间和右颈部Ⅴb及Ⅳ区淋巴结未见癌。免疫组化:ER(-)、PR(-)、HER2(2+)、Ki-67(50%+)。
术后辅助治疗及随访
患者于2015年11月23日行TC方案1周期治疗,2015年12月行局部放疗,同时联合曲妥珠单抗维持治疗1年。截至目前定期复查未见复发转移。
患者超声引导下右侧腋窝淋巴结穿刺活检病理示:低分化腺癌浸润,考虑为乳腺来源。免疫组化:ER(-)、PR(-)、HER2(3+)、Ki-67(25%+)。后行FAC方案3周期联合曲妥珠单抗,后改为多西他赛联合曲妥珠单抗及拉帕替尼。因拉帕替尼难以耐受,将原方案更改为多西他赛联合曲妥珠单抗及帕妥珠单抗治疗3周期。于2015年10月行右乳改良根治术+右颈部择区淋巴结清扫术。病理示:乳腺、乳头、皮肤未见癌,乳腺呈腺病样改变,大量纤维增生并炎症细胞浸润,符合治疗后改变。腋窝淋巴结可见转移癌:2/10,肌间和右颈部Ⅴb及Ⅳ区淋巴结未见癌。免疫组化:ER(-)、PR(-)、HER2(2+)、Ki-67(50%+)。术后TC方案1周期治疗,联合局部放疗,同时联合曲妥珠单抗治疗1年。截至目前定期复查未见复发转移。
图4 治疗经过回顾
点评专家
华中科技大学同济医学院附属协和医院乳腺肿瘤放化疗科主任
中国临床肿瘤学会乳腺癌专家委员会常委
中国南方肿瘤临床研究协会乳腺癌专家委员会常委
中国医师协会精准医疗乳腺癌专家委员会委员
湖北省抗癌协会乳腺癌专家委员会副主任委员
湖北省乳腺甲状腺学会副会长
亚太医学生物免疫学会常务理事
湖北省医学生物免疫学会放射免疫专家委员会主任委员
点评
患者女性,45岁,发现无痛性右腋窝肿块3天就诊,行右侧腋窝淋巴结穿刺活检,病理诊断:(右乳腺)浸润性导管癌3级 ER(-)、PR(-)、HER2(3+)、Ki-67(25%+),临床诊断Her-2阳性Ⅲc期乳腺癌。根据NCCN2018 V3乳腺癌指南和我国CSCO 2018版乳腺癌诊疗指南,患者初始选择以曲妥珠单抗或者是曲妥珠单抗联合帕妥珠单抗靶向治疗为基础的方案新辅助治疗是合适的。
HER2阳性乳腺癌是一类侵袭性强、恶性度高的乳腺癌亚型,但随着抗HER2治疗的问世,其疗效得到极大改善。既往代表性的临床研究有HERA、NSABP B-31、NCCTG N9831和BCIRG-006研究,结果提示在原发灶直径>1cm,不管有无淋巴结转移患者,化疗加用曲妥珠单抗后可以显著降低复发转移风险,提高无病生存。曲妥珠单抗联合化疗与单用化疗相比能够显著提高pCR率,进一步奠定了新辅助治疗中曲妥珠单抗的基石地位。此外,NeoSphere、TRYPHAENA以及KRISTINE等研究,均显示了新辅助曲妥珠单抗联合帕妥珠单抗双靶治疗HER2阳性乳腺癌具有更高的病理缓解率。近期发布的PENOY研究是对亚洲人群进行的相关研究,对照组是多西紫杉醇联合曲妥珠单抗在新辅助阶段采用四个疗程,而研究组是帕妥珠单抗+曲妥珠单抗+多西他赛,即双靶联合化疗的方案。结果显示:多西他赛联合曲妥珠单抗tpCR率为21.8%,而双靶联合多西他赛治疗组的tpCR率达到了39.3%,有显著的统计学差异(P=0.0014)。目前帕妥珠单抗在中国2018年12月17日已获批上市,中国患者即将可以从双靶+化疗方案中获益。
该病例新辅助治疗后疗效评价为non-pCR,对于这部分未达到pCR患者后续应该如何治疗?近期公布的KATHERINE研究则回答了这个问题。研究设计将新辅助治疗未达到pCR的患者分为两组,一组使用曲妥珠单抗的治疗,另一组使用T-DM1(ado-trastuzumab,曲妥珠单抗-美坦新偶联物)治疗。该研究对照组3年iDFS为77%,而T-DM1组为88%,统计学存在显著差异。这提示新辅助化疗未达pCR的患者术后强化抗HER2治疗能够获益更多。
该病例选择曲妥珠单抗联合帕妥珠单抗双靶向治疗为基础的化疗方案新辅助治疗后原发灶达到pCR,腋窝淋巴结non- pCR。由于当时治疗期间KATHERINE研究结果尚未公布,该患者术后若继续使用曲妥珠单抗联合帕妥珠单抗可带来更多的获益。对于HER2阳性型乳腺癌患者来说,化疗联合靶向治疗是对于HER2阳性乳腺癌患者治疗环节必不可少的一个重要步骤。该患者治疗至今,未见明确复发,由此充分证实对于HER2阳性患者抗HER2治疗的必要性和重要性。
1.Longer-term assessment of trastuzumab-related cardiac adverse events in the herceptin adjuvant (HERA) trial[J]. Journal of Clinical Oncology, 2010, 28(21):3422-3428.
2.Gianni L , Dafni U , Gelber R , et al. Treatment with trastuzumab for 1 year after adjuvant chemotherapy in patients with HER2-positive early breast cancer: a 4-year follow-up of a randomised controlled trial.[J]. Lancet Oncology, 2011, 12(3):236-244.
3. 《乳腺癌HER2检测指南(2014版)》编写组. 乳腺癌HER2检测指南(2014版)[J]. 中华病理学杂志, 2014;43(4):262-267.
4. Baselga J, Swain S M. CLEOPATRA: a phase III evaluation of pertuzumab and trastuzumab for HER2-positive metastatic breast cancer[J]. Clinical Breast Cancer, 2010, 10(6):489-491.
5. Extra J M, Cognetti F, Maraninchi D, et al. Long-term survival demonstrated with trastuzumab plus docetaxel: 24-month data from a randomised trial (M77001) in HER2-positive metastatic breast cancer.[J]. Journal of Clinical Oncology, 2005, 23(16):17S.
6. Smith I , Procter M , Gelber R D , et al. 2-year follow-up of trastuzumab after adjuvant chemotherapy in HER2-positive breast cancer: a randomised controlled trial[J]. Lancet (North American Edition), 2007, 369(9555):0-36.
7. Rugo H, Brammer M, Zhang F, et al. Effect of trastuzumab on health-related quality of life in patients with HER2-positive metastatic breast cancer: data from three clinical trials[J]. Clinical Breast Cancer, 2010, 10(4):288-293.
8. Buzdar AU, Ibrahim NK, Francis D, et al. Significantly higher pathologic complete remission rate after neoadjuvant therapy with trastuzumab, paclitaxel, and epirubicin chemotherapy: results of a randomized trial in human epidermal growth factor receptor 2-positive operable breast cancer[J], J Clin Oncol, 2005;23(16):3678-3685.
41本肿瘤患者指南丛书
点击下方图片即可免费阅读
70个肿瘤相关临床试验招募患者
点击下方图片或识别图片二维码即可查看详情