【1930】【2018 ESMO ASIA】Tony Mok教授口头发言:IMpower133研究开启SCLC一线治疗新时代
2018年 11 月 23 日-25 日,欧洲肿瘤内科学会亚洲年会 (ESMO ASIA 2018) 在新加坡盛大召开。本次大会上,肺癌领域多项重磅研究报道,其中,香港中文大学Tony Mok教授口头报道了IMpower133研究:atezolizumab 联合EP用于广泛期SCLC一线治疗的初步疗效和安全性及CNS相关不良事件,这一研究作为本次的LBA重磅发布。大会现场,来自西班牙的Pilar Garrido教授对这一研究进行现场点评。
LBA1 IMpower133研究: atezolizumab 联合EP用于广泛期SCLC一线治疗的初步疗效、安全性及CNS相关不良事件
图:莫树锦教授汇报IMpower133研究
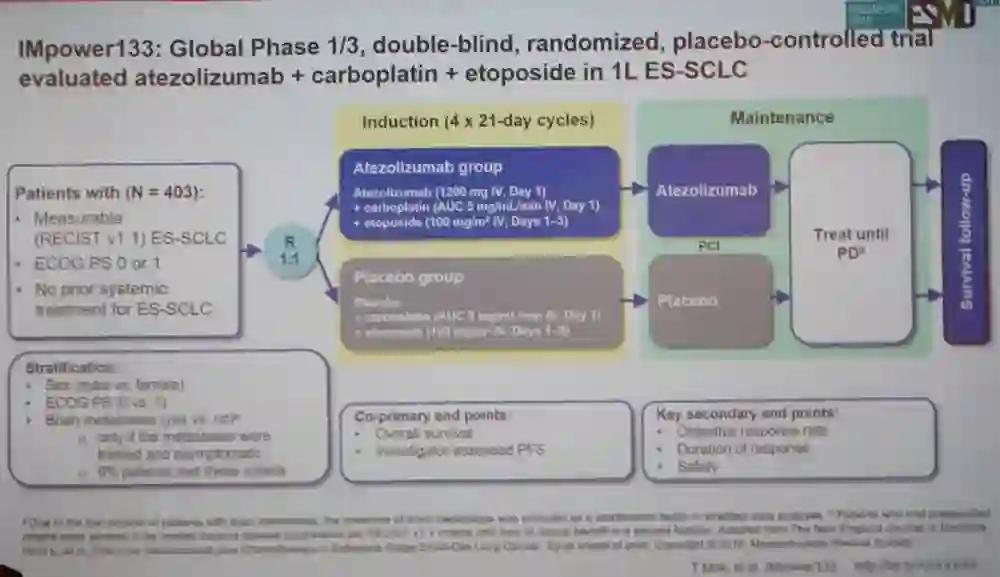
广泛期SCLC的一线标准治疗为铂类(卡铂或顺铂)联合依托泊苷,尽管一线化疗的缓解率较高,但患者的预后较差。IMpower 133研究是一项全球I/III期、双盲、随机、安慰剂对照的研究,旨评估在EP方案的基础上联合抗PD-L1单抗atezolizumab (atezo)或安慰剂用于晚期SCLC一线治疗。本次分析旨在评估IMpower 133研究中接受PCI治疗患者CNS相关不良事件(AE)发生率。
方法
IMpower 133研究入组了既往未接受过治疗的广泛期SCLC患者,不要求进行PD-L1检测。患者1:1随机分配接受4个周期的卡铂(AUC 5 mg/mL/min IV,第1天) + 依托铂苷(100 mg/m2 IV,第1-3天)联合atezo (1200 mg IV,第1天) 或安慰剂,21天为一个治疗周期,然后给予atezo或安慰剂维持治疗,直至疾病进展、不可耐受的毒性或不再有临床获益。在维持治疗期间,方案允许患者进行预防性脑照射(PCI)。但不允许患者接受根治性胸部放疗(TR)。共同主要终点为OS和研究者评估的PFS。外周血肿瘤突变负荷(bTMB)是一个探索性的研究分析终点,采用既定的cutoff值(≥16 vs < 16和≥10 vs < 10 mutations/Mb)进行分析。
图:IMpower133研究设计
结果
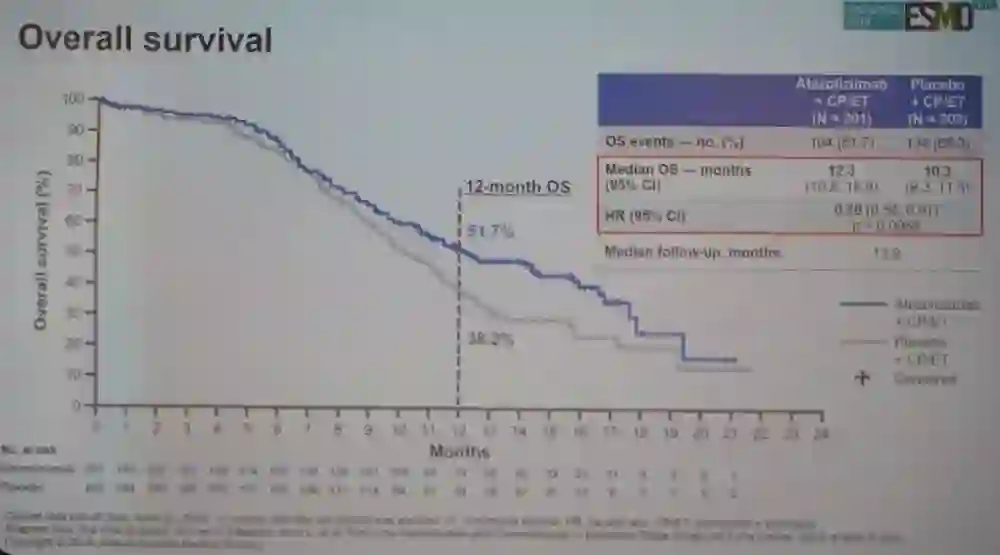
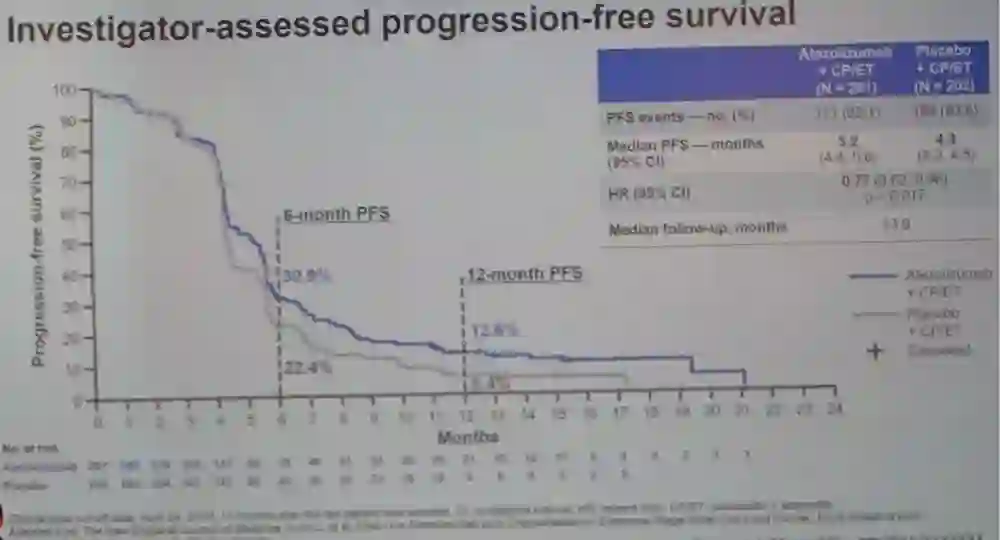
IMpower133研究中,atezo组 vs 安慰剂组分别入组了201例和202例患者,入组时合并脑转移患者两组分别有17例(8.5%)和18例(8.9%)。研究过程中,共44例患者接受PCI治疗,每组各22例。与既往研究结果一致,在EP方案的基础上联合atezo用于广泛期SCLC一线治疗,显著改善患者的PFS和OS,疗效见下表。Atezo组 vs 安慰剂组显著延长OS,两组的mOS分别为12.3 vs 10.3个月,HR 0.70 [95% CI 0.54–0.91; P = 0.0069],在重要亚组和既定的bTMB cutoffs 值分组中,均观察到一致的生存获益。两组的mPFS分别为5.2 vs 4.3个月,HR 0.77[95% CI 0.62–0.96; P = 0.017],在重要亚组和既定的bTMB cutoffs 值分组中,均观察到一致的PFS获益。确认的ORR对比,两组分别为60.2% vs 64.4%;mDOR分别为4.2 vs 3.9个月,HR 0.70[95% CI 0.53–0.92]。两组患者接受后续治疗的比例相当,Atezo组 vs 安慰剂组分别有3.0%和7.4%的患者接受了后续免疫治疗。
图:两组的OS对比
图:两组的PFS对比
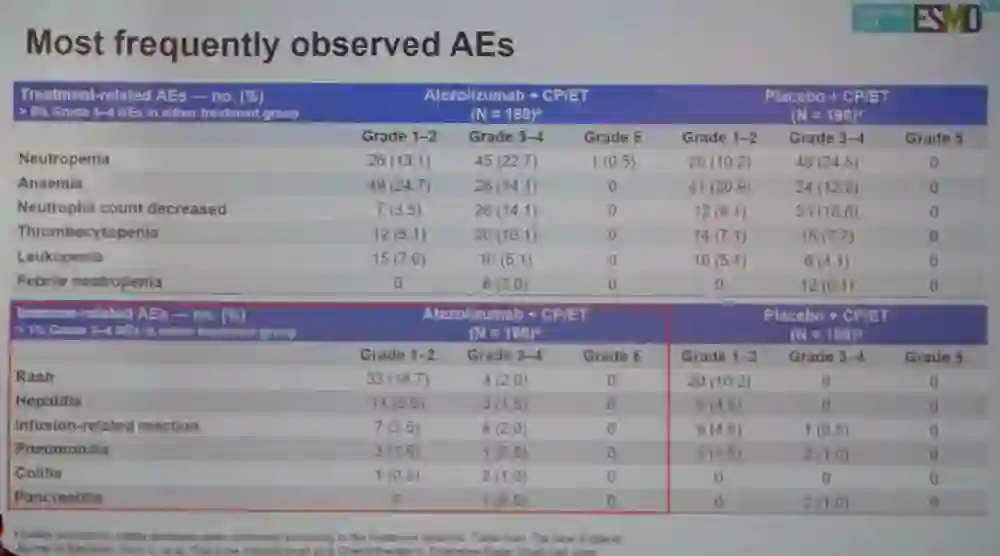
安全性分析:共44例(每组22例)患者接受PCI治疗,7例(atezo 组3例;安慰剂组4例)患者接受胸部放疗。Atezo组 vs 安慰剂组,3–4度治疗相关的不良事件(AE) 发生率分别为56.6% vs 56.1%;治疗相关严重AEs发生率分别为22.7% vs 18.9%。治疗相关的常见AEs(发生率>5%的3-4度AE)包括中性粒细胞减少、贫血、中性粒细胞计数减低、血小板减低、报喜不减低和粒缺性发热。常见的免疫相关AE(>1%的3-4级AE)包括皮疹、肝炎、输液反应、肺炎、结肠炎和胰腺炎,总结见下图。
图:治疗过程中的常见AE
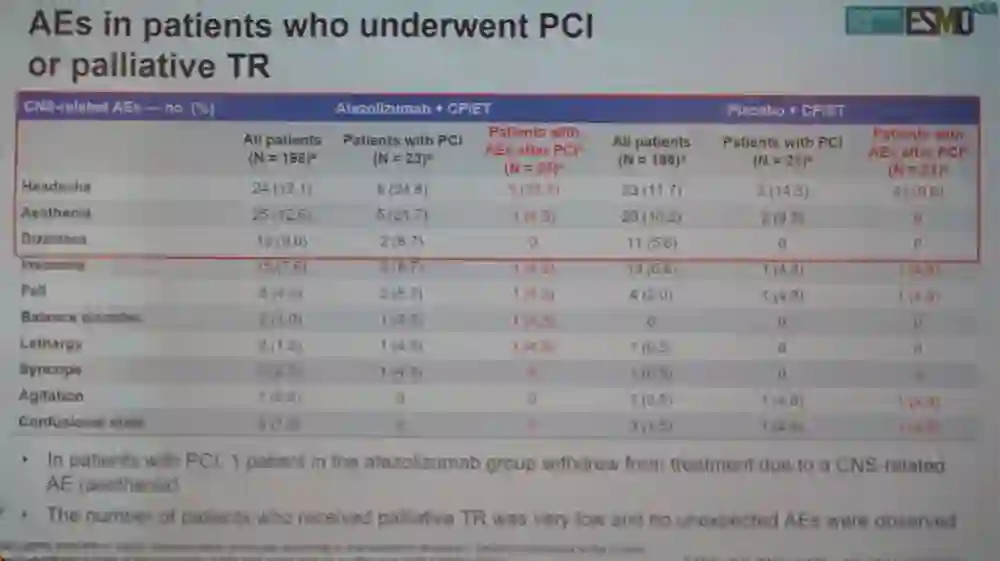
接受PCI治疗或胸部姑息性放疗的患者,CNS相关的AE发生率总结见下图。
图:接受PCI或姑息性胸部放疗患者的AE总结
结论
IMpower133研究是20年来,第一个组广泛期SCLC一线治疗上,观察到超越标准治疗方案,取得有临床意义OS改善的研究。相比于单纯EP化疗,在EP方案的基础上联合atezo用于未经选择的广泛期SCLC一线治疗,可以显著延长PFS和OS。与预期一致,atezo联合EP方案,未观察到预期以外的安全性事件,包括接受PCI或胸部放疗的患者。在接受PCI治疗的患者中,头痛是最常见的CNS相关AE。本研究中未探索根治性胸部放疗,可以考虑在后续研究中进一步探索。这一研究结果提示,Atezo +EP方案应该推荐作为初治广泛期SCLC患者一线治疗新标准。
现场点评:IMpower133研究开启SCLC一线治疗新时代
大会现场,来自西班牙的Pilar Garrido教授对这一研究进行现场点评。
现场点评:Pilar Garrido教授
SCLC约占所有肺癌的15%,几乎所有的患者均为既往或当下吸烟者。超过2/3的患者诊断时为IV期,自1996年获批依托泊苷以来,未取得任何重要临床进展。因此,SCLC的预后较差,2年生存率<5%。多个原因导致SCLC的转化研究非常困难,包括很难获取活检和手术标本、SCLC的分子异质性,对SCLC耐药机制的了解甚少、SCLC通常表现为快速进展等。
免疫治疗的问世,为SCLC带来新希望。SCLC肿瘤与增加的免疫原性相关,如SCLC患者常出现副瘤综合症,免疫介导的副瘤综合症与更好的预后相关。此外,一些研究显示,SCLC中CD45 T细胞浸润预示着患者有更好的OS;局限期SCLC相比于广泛期SCLC,有更多效应T细胞。吸烟与更高的突变负荷相关。
早期,CTLA-4单抗伊匹木单抗在SCLC中进行了多项研究,均取得阴性结果。在随机III期研究中,伊匹木单抗联合EP方案用于SCLC一线治疗,未观察到PFS和OS获益,且带来了严重的毒性。IMpower133研究是第一项取得阳性结果的III期免疫治疗研究。研究以患者是否合并脑转移作为分层因素。脑转移在SCLC患者中发生率较高,诊断时约10%的患者合并脑转移,合并脑转移的患者,治疗1年和2年失败率分别为28%和58%。尽管脑转移发生率较高,但合并脑转移的患者,在临床研究中常被排除在外。仅27.7%的晚期NSCLC患者研究允许无症状脑转移患者入组;仅3.7%的研究允许有症状或进展性脑转移患者入组。随着影像学检查的普及和越来越多有效系统性方案的出现,合并脑转移的SCLC患者会越来越多,这是一个很大的、未被满足的群体。接受系统性方案治疗后取得CR或部分PR的患者,PCI已经推荐作为标准治疗。然而,60%接受PCI治疗的患者在治疗1年后会出现中枢神经认知功能夏季,这可能显著影响患者的生活治疗。研究显示,大多数未接受PCI治疗的广泛期SCLC患者,会发生脑进展,需要接受高剂量的放疗。近期的一些临床实践调查结果,关于PCI的应用价值不一。
临床前研究显示,脑并不是一个免疫豁免器官。脑转移病灶也处于一个炎症性的微环境中,肿瘤组织中有较多的TILs。免疫检查点抑制剂虽然不能直接作用域肿瘤,但可以刺激外周T细胞,让其穿越血脑屏障,进入CNS产生抗肿瘤效应。放疗联合免疫治疗的临床前研究提示,放疗可以诱导肿瘤细胞坏死,增加肿瘤新抗原的是否,增加TMB,此外,放疗还可以增加PD-L1表达。脑转移灶中PD-L1表达水平中等。但在一项纳入32例脑转移患者的研究中,75%的患者显示出PD-L1高表达,且与TILs相关。随着免疫治疗的应用,越来越多的患者采用免疫治疗来控制颅外病灶,但是尚无前瞻性研究评估了同步放疗联合免疫治疗。回顾性研究证实,免疫治疗在黑色素瘤和NSCLC患者CNS转移灶中显示出疗效,但在接受PCI治疗的SCLC患者中,尚未表现出疗效。因此,需要进行前瞻性的研究来评估这一联合治疗模式,因此CNS毒性会显著影响患者的生活质量,此外,放疗的疗效可以被免疫治疗强化。然而,关于放疗和免疫治疗联合的最佳组合方式,目前尚未可知。
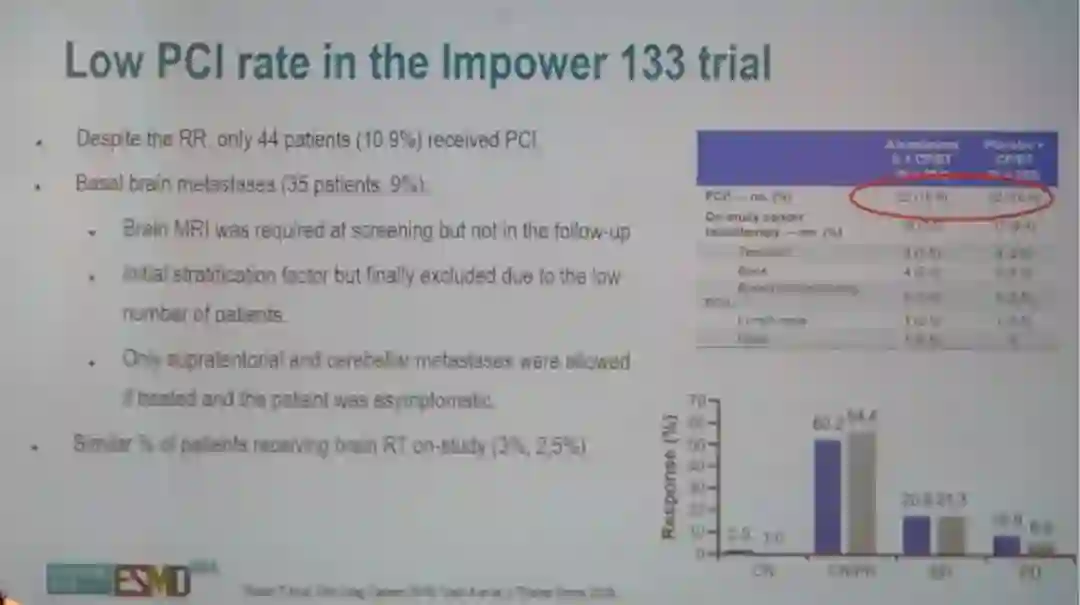
在IMpower133研究中,虽然两组患者的ORR较高,但仅有44例(10.9%)的患者接受了PCI治疗。基线时,共35例(9%)患者合并脑转移,研究在入组筛查时要求患者进行头颅MRI检查,但在随访过程中并未进行MRI检查。研究最初设计时将脑转移与否作为分层因素纳入,但最终因为患者人数较低,不再纳入分层分析。研究入组时,仅允许入组接受过局部治疗的脑转移患者以及无症状脑转移患者。
41本肿瘤患者指南丛书
点击下方图片即可免费阅读
70个肿瘤相关临床试验招募患者
点击下方图片或识别图片二维码即可查看详情