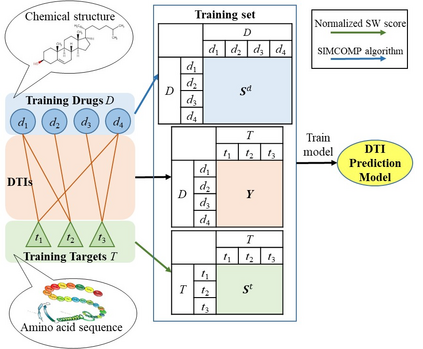
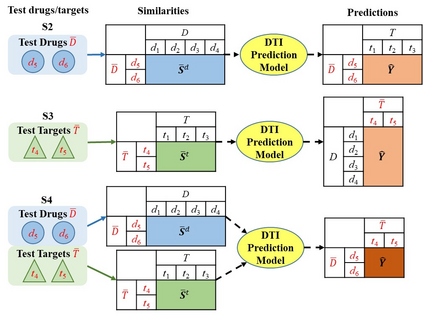
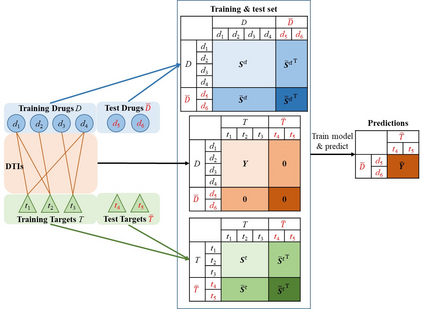
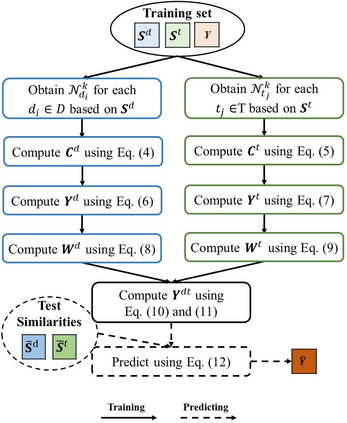
Predicting drug-target interactions (DTI) via reliable computational methods is an effective and efficient way to mitigate the enormous costs and time of the drug discovery process. Structure-based drug similarities and sequence-based target protein similarities are the commonly used information for DTI prediction. Among numerous computational methods, neighborhood-based chemogenomic approaches that leverage drug and target similarities to perform predictions directly are simple but promising ones. However, existing similarity-based methods need to be re-trained to predict interactions for any new drugs or targets and cannot directly perform predictions for both new drugs, new targets, and new drug-target pairs. Furthermore, a large amount of missing (undetected) interactions in current DTI datasets hinders most DTI prediction methods. To address these issues, we propose a new method denoted as Weighted k-Nearest Neighbor with Interaction Recovery (WkNNIR). Not only can WkNNIR estimate interactions of any new drugs and/or new targets without any need of re-training, but it can also recover missing interactions (false negatives). In addition, WkNNIR exploits local imbalance to promote the influence of more reliable similarities on the interaction recovery and prediction processes. We also propose a series of ensemble methods that employ diverse sampling strategies and could be coupled with WkNNIR as well as any other DTI prediction method to improve performance. Experimental results over five benchmark datasets demonstrate the effectiveness of our approaches in predicting drug-target interactions. Lastly, we confirm the practical prediction ability of proposed methods to discover reliable interactions that were not reported in the original benchmark datasets.
翻译:通过可靠的计算方法预测药物目标的相互作用(DTI)是减少药物发现过程的巨大成本和时间的一个有效而高效的方法。基于结构的药物相似性和基于序列的目标蛋白质相似性是用于DTI预测的常用信息。在许多计算方法中,基于街区的化学基因学方法是简单但有希望的方法。然而,现有基于类似性的方法需要重新培训,以预测任何新药物或目标的相互作用,不能直接预测新药物或新目标的相互作用,也不能直接预测新药物、新目标以及新的药物目标配对。此外,当前DTI数据集中大量缺失(已解析)的相互作用妨碍了大多数DTI的预测方法。为了解决这些问题,我们提出了一种新的方法,即利用药物的W-Nearst Neighbor和互动复苏(WkNNIR)的 Weight K-NNIR 模型,不仅可以估计任何新药物和/或新目标的相互作用,而无需再培训的任何方法,而且还可以确认缺失的相互作用(虚假的) 。此外,WKNNIR的模型的精确性互动能力也阻碍大多数DTI的预测方法。此外,WkNIR还利用了原始的模型的模型的模型的精确性分析方法,我们提出了一种比较的模型的模型的模型的模型的模型的模型的模型的模型的模型的模型的模型的精确性方法,从而可以改进了其他的精确性的方法。