【2019 WCLC】CheckMate 017/057研究5年OS数据公布,中外专家共议免疫治疗的长期生存获益
2019年9月7日至10日,世界肺癌大会(WCLC)在西班牙巴塞罗那隆重召开。CheckMate 017/057的汇总五年总生存(OS)数据在本次大会上重磅发布,以纳武利尤单抗为代表的免疫检查点抑制剂引领了NSCLC的治疗变革。WCLC期间,CheckMate 017/057研究者之一、耶鲁癌症中心医学肿瘤科的Scott Gettinger教授和上海交通大学附属胸科医院的韩宝惠教授应邀接受采访,分享他们对CheckMate 017/057的5年OS数据的解读。
上海市领军人才、优秀学科带头人
上海市胸科医院呼吸内科主任
上海市胸部肿瘤研究所副所长
上海第二医科大学博士及博士后导师
上海市胸科医院药物临床研究机构主任
亚太医学免疫学会肿瘤分会主委
国务院特殊津贴
国家药监局(CFDA)审评专家
CSCO肿瘤血管靶向专业委员会主委
CSCO肿瘤NSCLC专业委员会副主委
中国抗癌协会全国肿瘤临床执行委员
中国抗癌协会肿瘤精准诊疗专委会副主委
中华医师学会呼吸分会常委
CheckMate 017/057研究者之一
耶鲁癌症中心医学肿瘤科博士
CheckMate 017/057研究5年OS数据公布,免疫治疗NSCLC长期生存再添力证
在刚刚结束的WCLC大会上,CheckMate 017/057两项研究的长期汇总分析数据(5年OS)以口头报告的形式公布,这是目前肿瘤免疫治疗随机III期临床试验中报道过的随访时间最长的数据。
CheckMate 017/057研究分别针对二线鳞状和非鳞NSCLC患者,这2项研究的患者均在接受一线含铂化疗期间或之后出现疾病进展,随后以1:1的比例进行随机分组,以评估接受纳武利尤单抗治疗(3mg/kg,每2周给药一次)与标准治疗多西他赛(75 mg/m2,每3周给药一次)的疗效,直到疾病进展或出现不可耐受毒副反应。完成初步分析后,多西他赛组中未见生存获益的患者可交叉进入纳武利尤单抗组进行治疗。主要终点均为总生存(OS),其他终点包括无疾病进展生存(PFS)、客观缓解率(ORR)、根据肿瘤PD-L1表达状态的疗效、安全性和患者报告结局(PROs)等。
图1 CheckMate 017/057的研究设计
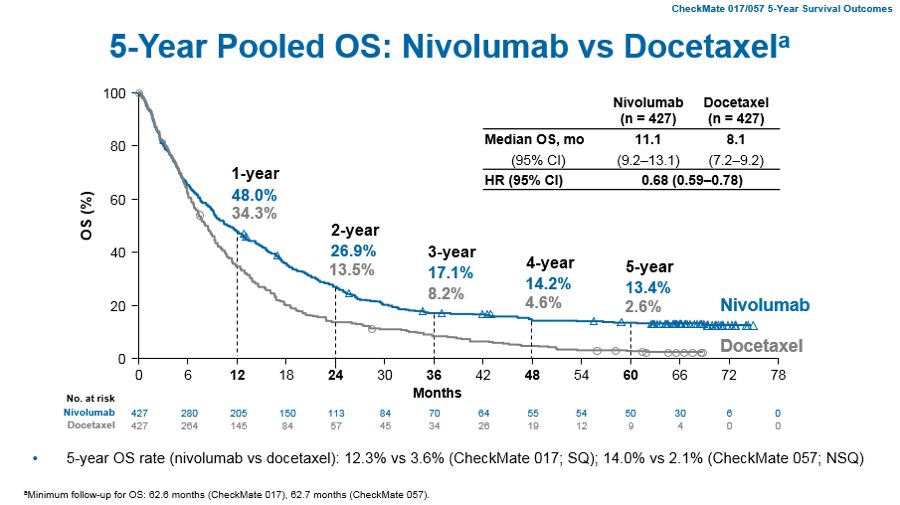
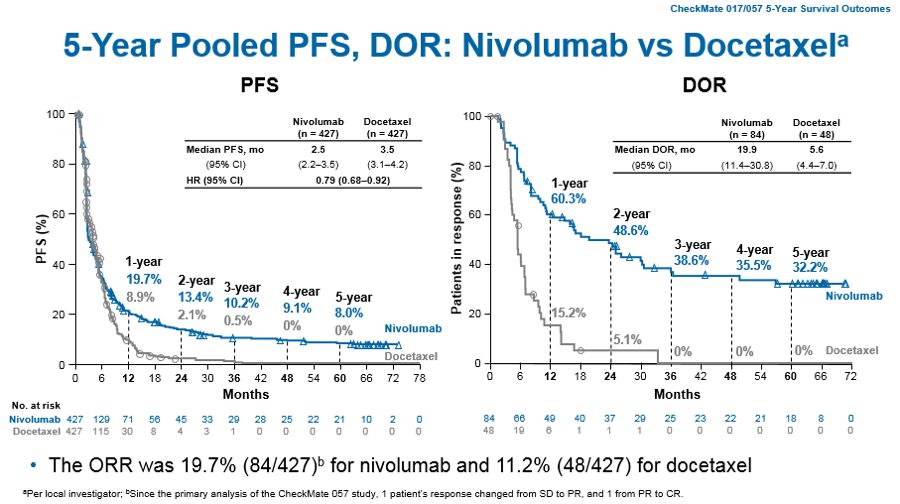
作为CheckMate 017/057的研究者之一,Scott Gettinger教授为我们详细介绍了此次汇总分析的数据。与多西他赛相比,接受纳武利尤单抗治疗的患者在5年时显示长期总生存(OS)持续获益,纳武利尤单抗组和多西他赛组的OS分别为13.4%与2.6%,PFS分别为8.0%与0%。另外,对纳武利尤单抗存在客观应答的患者中有32.2%在5年时仍持续应答,而对多西他赛应答的患者在5年时持续应答的比例则为0%。10%的5年随访时仍存活的患者已经停止使用纳武利尤单抗,并没有接受下一步治疗也未出现疾病进展。接受纳武利尤单抗治疗的患者保持应答的中位时间为19.9个月,而多西他赛组仅为5.6个月。
图2 CheckMate 017/057汇总分析的5年OS数据
图3 CheckMate 017/057汇总分析的5年PFS、DOR等数据
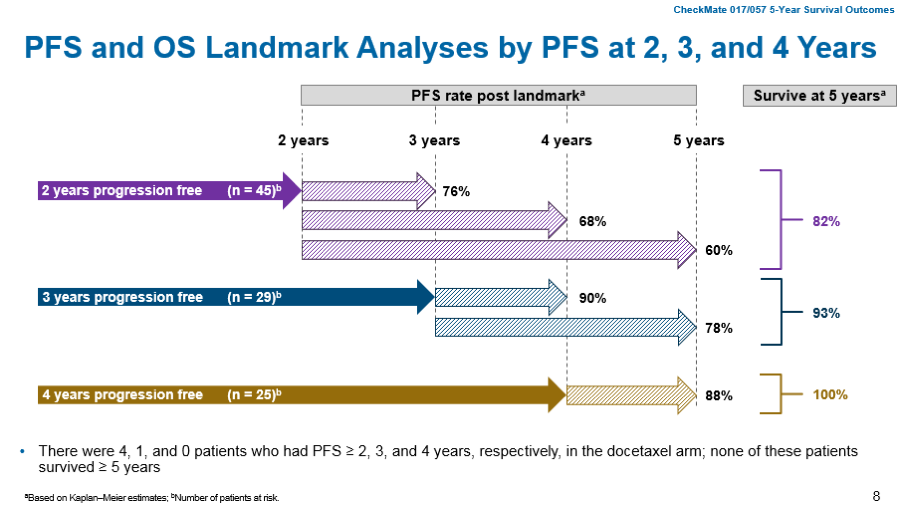
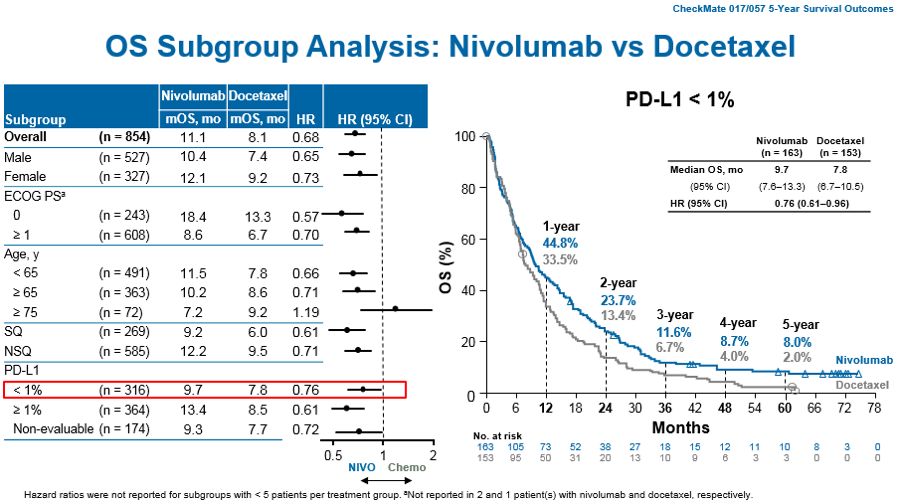
同时界标分析的数据表明,接受纳武利尤单抗治疗并在第2年和3年未发生疾病进展的患者,其在5年随访时无疾病进展的可能性(PFS率)分别高达60%和78%;5年随访时仍存活的可能性(OS率)分别为82%和93%;第4年未发生疾病进展的患者中,5年无疾病进展和仍然存活的比例分别高达88%和100%,另外在接受纳武利尤单抗治疗的所有亚组中均观察到OS获益。
图4 CheckMate 017/057的界标分析数据
图5 CheckMate 017/057汇总分析中各亚组OS数据
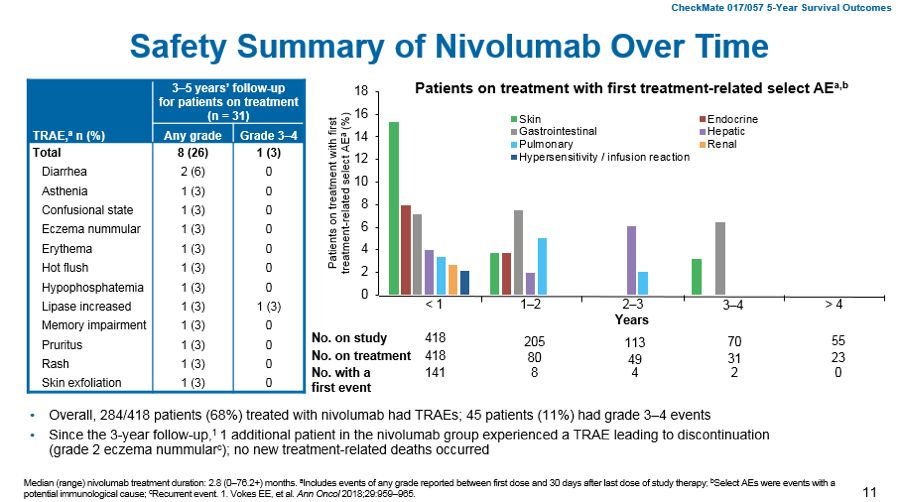
接受纳武利尤单抗治疗的患者,其安全性与既往报道的NSCLC二线治疗研究结果一致,并且在长期随访中未发现新的安全信号。在3-4年时仍然在组的70名患者中,有2名在此期间出现了新的治疗相关不良反应。而在4-5年仍处于研究中的55名患者,在此期间没有发生新的治疗相关不良反应。
图6 CheckMate 017/057的安全性数据
Scott Gettinger教授提到,“纳武利尤单抗早已获批上市,本次汇总分析的结果十分重要,为我们提供了免疫治疗的大样本长期疗效数据,证明了纳武利尤单抗相比传统化疗能为患者带来更为持久的获益”。
韩宝惠教授也表示,“接受纳武利尤单抗治疗的患者5年OS提高至化疗的5倍,这一历史性的进步意味着肺癌成为慢性病已逐渐成为现实。同时我们可以看到相当高比例的患者在接受纳武利尤单抗治疗5年后肿瘤仍在持续缓解,这对患者生活质量的改善具有极其重要的意义”。
CheckMate 078与全球研究结果一致,中国患者同样获益显著
CheckMate 078是以中国患者人群为主的研究,此前公布的研究数据表明,CheckMate 078研究的总生存、客观缓解率和起效时间,均与CheckMate 017/057数据一致,纳武利尤单抗在亚洲人群同样具有较好疗效,并无人种差异性,可见在二线治疗中,免疫治疗已全面超越化疗。韩宝惠教授表示,“既往的研究中,无论是化疗还是靶向治疗,中国人群的数据均略优于国外数据,这可能与人种特性有关”。对于近几年才进入中国的免疫治疗,中国数据是否能重复甚至优于全球数据?对于CheckMate 078研究,韩教授提到该研究的入组速度非常快,大约1年的时间便入组完毕,表明纳武利尤单抗的患者依从性较好,而且初步疗效显著,患者入组研究的意愿强烈,促成了整个临床研究的顺利开展。CheckMate 078的2年OS数据将在九月中旬的CSCO大会上公布,韩教授期待CheckMate 078研究将同样会取得令人满意的结果。
免疫治疗全面布局NSCLC领域,为各线肺癌患者带来持久获益
多项临床研究已经证实,以纳武利尤单抗为基础的免疫肿瘤治疗能为各线肺癌患者带来长期的生存获益。Scott Gettinger教授分析道,如今,多家公司均拥有自己的PD-1/PD-L1产品,肺癌的免疫治疗是当前非常火热的研究领域。纳武利尤单抗布局一线治疗的CheckMate 227 研究的初步结果已表明纳武利尤单抗联合伊匹木单抗的双免疫联合一线治疗能为晚期NSCLC患者带来显著的生存获益,特别是肿瘤突变负荷(TMB)高的患者,相信双免疫联合治疗方案也将很快获批应用于肺癌的一线治疗。除了一线治疗,Scott Gettinger教授还提到纳武利尤单抗引领了免疫新辅助/辅助治疗,初步研究数据极具前景。
韩宝惠教授认为,如果将来我们能找到较好的生物标记物用于获益人群的筛选,纳武利尤单抗的应用将越来越广泛。未来,以纳武利尤单抗为基础的联合治疗可能并不局限于PD-L1高表达或高TMB的患者,如联合传统化疗、联合抗血管生成药物,作为有效的强强联合,能发挥1+1>2的协同作用,这样就无须进行生物标记物的检测,同时疗效能得以提高。期待以纳武利尤单抗为代表的免疫治疗能在更多的联合策略上开展临床研究,探索更多联合治疗的可能性。
免疫治疗发展潜力巨大,有望成为肿瘤治疗主力军
谈及免疫肿瘤治疗未来的发展趋势,Scott Gettinger教授提到,如果不局限PD-L1或TMB状态,目前仅约15%-20%的患者对免疫治疗有响应,对于这类患者,我们未来要进一步研究如何解决后续的获得性耐药问题。而对于对免疫治疗无响应的患者,如何充分调动免疫系统参与到肿瘤的抗争中,提高免疫治疗的整体响应率,是当前需要攻克的难题。另外,对于靶向治疗失败的驱动基因(如EGFR/BRAF/ALK/ROS1等)阳性晚期NSCLC患者,未来需要探讨如何将免疫治疗更好地应用于这类患者并为他们带来更多获益。
韩宝惠教授则认为战线前移、联合治疗将是未来免疫治疗的主要发展方向。韩教授解析道,从免疫治疗理论来看,分期越早肿瘤负荷越低,免疫防线的受破坏程度越小,肿瘤对免疫治疗的响应可能会更好,因此应将免疫治疗的关口前移,在更早线的患者人群中进行探索。另外,免疫联合治疗也是重要的研究方向,因为单一的免疫治疗的有效率相对有限,联合化疗或靶向治疗或许能达到优势互补的效果,取得更好的疗效。
最后,韩宝惠教授感慨道,肿瘤免疫治疗方兴未艾,虽然免疫治疗在国际上已有约10年的历史,但近3-5年肺癌的免疫治疗才开始在我国开展临床研究,并在去年才正式获批上市。根据当前临床研究的数据,免疫治疗在提高长期生存方面具有独特的优势,未来免疫治疗将从二线治疗到一线治疗、从单药治疗到联合治疗、从晚期治疗到辅助治疗和维持治疗,全面推动晚期NSCLC临床实践的变革。