【Blood】速度围观!原发皮肤淋巴瘤2018版WHO-EORTC共识分类更新出炉
原发皮肤淋巴瘤是皮肤的非霍奇金淋巴瘤,诊断时无皮肤外表现,包括皮肤T细胞淋巴瘤(CTCLs)和皮肤B细胞淋巴瘤(CBCLs),临床和组织学特征高度特异,治疗与预后完全不同于继发皮肤表现的原发于淋巴结的淋巴瘤。2005年首次公布原发性皮肤淋巴瘤世界卫生组织-欧洲癌症研究和治疗组织(WHO-EORTC)共识分类,成为诊断和分类的金标准。本文将介绍2018更新的WHO-EORTC分类和分子研究结果。
MF、MF变体和SS
蕈样霉菌病(MF)和SéZary综合征(SS)是CTCL的经典类型,MF占CTCL60%,占所有原发性皮肤淋巴瘤50%,滤泡性MF(FMF)、派杰样网状组织细胞增生症和肉芽肿性松弛皮肤症是MF的变体,后两者极为罕见。FMF占MF的10%,不同于MF的是滤泡性浸润,较少累及表皮,头颈部皮肤多发,成簇的滤泡性丘疹、痤疮样病变和脱发,FMF对针对皮肤的治疗反应较差,临床过程更侵袭,因此治疗应更积极。近期研究明确了FMF的一个亚型,临床经过惰性,预后良好。
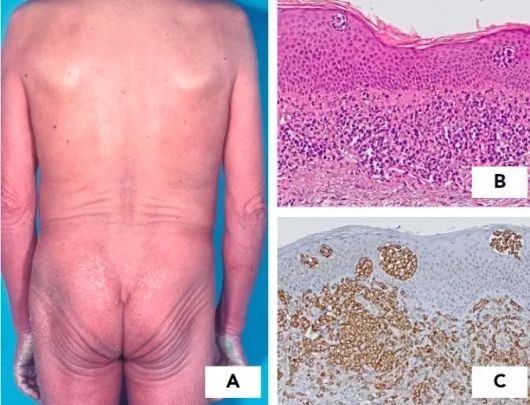
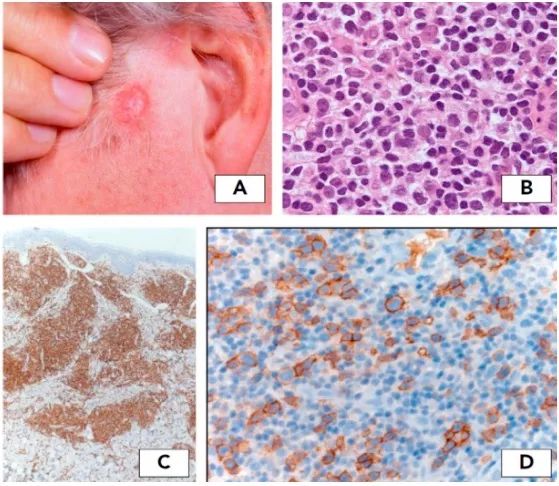
SS是罕见的白血病型CTCL,三联特征表现包括瘙痒性红皮病、全身淋巴结肿大和脑回样核的克隆性T细胞(SéZary细胞)。早期SS与红皮性炎性皮肤病(EIDs)鉴别困难,诊断标准包括皮肤和外周血克隆性T细胞,或是绝对Sézary细胞>1000/µL,或CD4+ T 细胞增加导致CD4+/CD8+ 细胞≥10、CD4+/CD7- 细胞≥30%或CD4+/CD26-细胞≥40%。新的生物标志物包括PD-1(CD279)和KIRDL2(CD158k),有助于鉴别皮肤和外周血的SS和EIDs(图1)。循环中Sézary细胞基因分析显示特征性过表达PLS3、TWIST1、DNM3、EPH4、CD158k/KIRDL2和NKp46。
图1 Sézary综合征。(A)红皮病;(B)浅层真皮不典型淋巴样细胞带状浸润形成微脓肿;(C)肿瘤T细胞强表达CD279(PD-1),是鉴别Sézary综合征与EIDs的标志
原发性皮肤CD30+ T细胞 LPD
原发性皮肤CD30+ 淋巴增殖性疾病(LPDs)是CTCL第二常见类型,占所有CTCL的25%左右,包括原发性皮肤间变性大淋巴瘤(C-ALCL)和淋巴瘤样丘疹病(LyP),临床表现有助于两者鉴别并选择合适治疗。C-ALCL表现为孤立或成簇或多灶性结节与肿瘤,皮肤复发常见,10%~15%有皮肤外播散。LyP特点是慢性过程,反复复发,自愈性丘疹性皮损或结节性皮损,组织学变化很大,包括LyP A、B、C、D、E型以及一些不常见变体,还有一种亚型携带6p25.3的DUSP-IRF4重排。表1列举了LyP主要类型及需鉴别的CTCLs。
表1 LyP组织学亚型及主要鉴别疾病
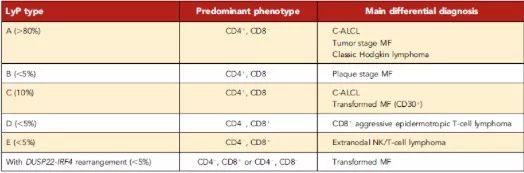
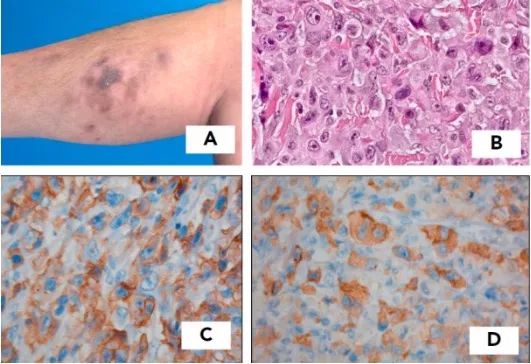
图2 皮肤单变大细胞淋巴瘤,表现为右下肢多发皮损。(A)部分自然消失;(B)组织学显示弥漫性大的间变细胞浸润;(C)CD30阳性;(D)胞浆ALK染色
25%的C-ALCL和小部分LyP有 DUSP22-IRF4重排,但无预后作用,组织学上病变双相生长,表皮中是小的CD30+脑回状细胞,真皮中是大的CD30+转化细胞,细胞毒蛋白表达减少。
TP63基因重排与ALK− 系统性ALCL生存差有关。新发现的NPM1-TYK2融合基因,影响STAT信号传导,C-ALCL和LyP中均可见,15%原发性皮肤CD30+ LPDs出现TYK2断裂。含CDKN2A 抑癌基因的9p21.3缺失很少见于C-ALCL。
其他CTCLs
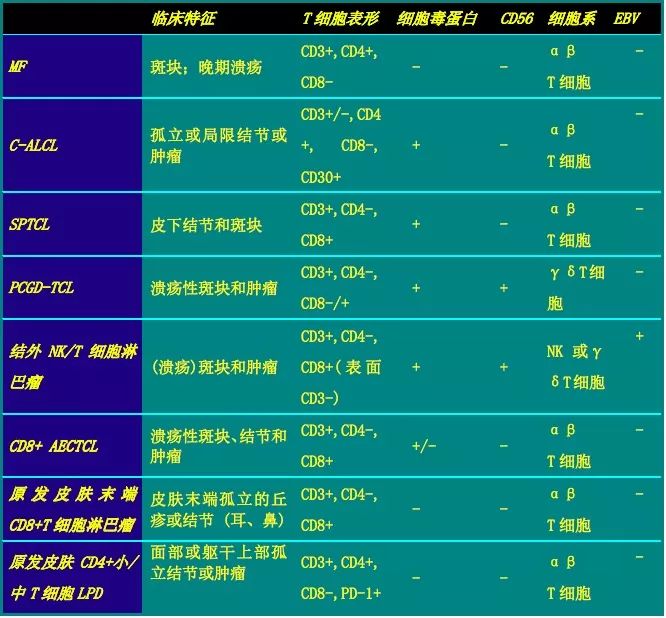
MF、SS和原发性皮肤CD30+ LPD之外的CTCLs罕见,不足10%。表2总结了其他类型CTCLs的临床、组织病理学和免疫表型特征。原发性皮肤γδ T细胞淋巴瘤特征是TCRγδ+ 、βF1− T细胞表型,但在MF或LyP中也偶有TCRγδ表达,与αβ T细胞表型相同,惰性经过。儿童慢性活动性EB病毒(EBV)感染、原发性皮肤末端CD8+ T细胞淋巴瘤和原发性皮肤CD4+ 中/小T细胞LPD在下一节讨论。
表3 其他CTCL的临床和免疫表型特征
儿童慢性活动性EBV感染
儿童EBV+ LPD包括种痘水疱病样LPD(HV样LPD)和蚊咬超敏反应,均是慢性活动性EBV感染的皮肤表现,可能发展为系统性EBV+ T或NK细胞淋巴瘤,部分患者有全身慢性活动性EBV感染证据。多数HV样LPD为CD8+T细胞表型,蚊咬超敏反应更多是NK细胞表型。HV样LPD是HV和HV样T细胞淋巴瘤总称,主要见于亚洲儿童和青少年或中美洲、南美洲及墨西哥土著居民。
经典HV表现为外露皮肤,特别是面部、耳垂和手背丘疹,无全身症状,多有季节性,严重病例的皮肤病变还可见于非暴露皮肤,面部肿胀和广泛溃疡也很常见,可有全身症状如发热、消瘦、淋巴结肿大和肝脾肿大。蚊咬高敏患者在蚊叮咬部位出现溃疡坏死性皮损,出现类似于HV样淋巴瘤的全身症状,发展为系统性淋巴瘤之前,可有多年反复皮肤损害。
原发性皮肤末端CD8+T细胞淋巴瘤
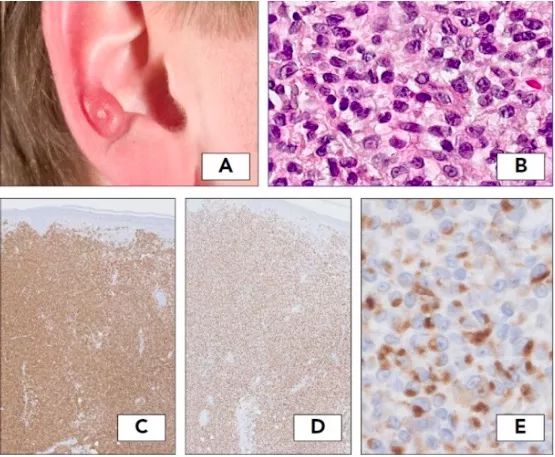
临时类型,特征是中等大小CD8+细胞毒性T细胞弥漫性浸润,组织学表现为侵袭性,但临床惰性。通常表现为孤立的、进展缓慢的丘疹或结节,主要位于耳部,或其他皮肤末端如鼻和足(图3A)。病变中克隆性中等大小原始细胞在真皮层弥漫增殖,有清晰的境界带,细胞CD3+、CD4−、CD8+和CD30−,PAN-T细胞抗原(CD2、CD5、CD7)不同程度丢失,TIA-1阳性,其他细胞毒蛋白(颗粒酶B,穿孔素)阴性,CD68常呈高尔基点状染色阳性(图3),几乎所有病例的增殖率都很低(<10%),EBV阴性。
图3 原发性皮肤末端CD8 + T细胞淋巴瘤。(A)典型临床表现,右耳缓慢进展的肿瘤;(B)真皮内中等大小多形性细胞弥漫性增殖;(C) CD8阳性;(D) TIA-1阳性(E) CD68阳性
本病预后良好,不推荐分期,皮损可采用手术切除或放疗,皮肤外复发少见,能否称为淋巴瘤仍有争议。由于临床惰性,应避免不必要治疗,病理上应与原发性皮肤侵袭性表皮CD8+ T细胞淋巴瘤和CD8+ MF进行区分。
原发性皮肤CD4+小/中T细胞LPD
2005年WHO-EORTC分类中,原发性皮肤CD4+小/中T细胞淋巴瘤被列为临时分类,表现为孤立斑块或肿瘤多发于面部、颈部或躯干上部,病变中CD4+小/中多形性T细胞结节状或弥漫性真皮内浸润,<30%的病变是大的多形性细胞,表达滤泡辅助T细胞标志PD-1(CD279)、BCL6和CXCL13(图4),增殖率多<5%,几乎所病例都包含小的反应性CD8+T细胞、B细胞和组织细胞。预后良好,典型病例不推荐分期,皮损如不能自发缓解,可行病灶内激素治疗、手术切除,偶可放射治疗。此病良性病程,2016年WHO-EORTC分类中称其为增生性疾病而非淋巴瘤。如果表现为全身皮肤病变和大且生长迅速的肿瘤,>30%大的多形性T细胞和高增殖率时,临床经过侵袭,应归入外周T细胞淋巴瘤,NOS。
图4 原发性皮肤CD4+小/中T细胞LPD。(A)左颊部肿瘤;(B)真皮层内小/中淋巴样细胞为主,散布大的淋巴样细胞;(C)CD4阳性;(D)中等至大细胞表达CD279/PD-1
CBCL
2005 WHO-EORTC分类中,CBCL主要有3种类型:原发性皮肤边缘区淋巴瘤(PCMZL)、原发性皮肤滤泡中心淋巴瘤(PCFCL)和原发性皮肤大B细胞淋巴瘤,腿型(PCDLBCL,LT),后二者是独立分型,前者则被列为粘膜相关淋巴组织结外边缘区淋巴瘤(MALT淋巴瘤)。EBV+皮肤黏膜溃疡是新的临时分类。
PCMZL
PCMZL主要影响年轻人,表现为孤立或多灶性斑块或结节,主要发生于躯干和手臂,皮肤复发常见,特别是多灶性皮损时,但很少向皮肤外部位传播。PCMZL非常惰性,预后良好,5年无病生存率近100%。PCMZL有2种类型,多数PCMZLs表达多种免疫球蛋白,不表达趋化因子受体CXCR3,肿瘤中以T细胞为主,肿瘤性B细胞只占小部分;小部分PCMZL的肿瘤性B细胞弥漫性增生或形成大结节,B细胞表达IgM和CXCR3,与其他结外MALT淋巴瘤有许多共同特征,常伴皮肤外损害。二种类型匀可能源于皮肤内抗原刺激所致。
PCFCL、PCDLBCL,LT和PCDLBCL,其他
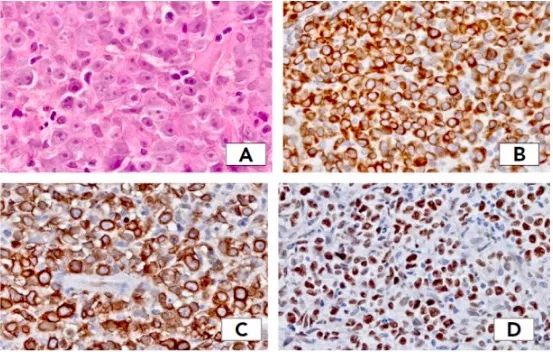
2005年WHO-EORTC将具有DLBCL组织学特征的CBCL分为2种类型:PCDLBCL,LT和弥漫性生长的PCFCL,此外还有PCDLBCL,其他。区分PCDLBCL,LT和PCFCL非常重要,因为预后与治疗不同。PCFCL是滤泡中心细胞肿瘤,以大的中心细胞为主,主要表现为头或躯干局部皮肤病变,放疗可控制病情,预后良好。PCDLBCL,LT是侵袭性较强的CBCL,组织学特征为中心母细胞和/或免疫母细胞增殖,多影响老年妇女,肿瘤快速进展。与PCFCL相比,更易播散到皮肤外部位,预后不佳。免疫表型和遗传变异也有助于鉴别诊断,PCDLBCL,LT强表达BCL2、IRF4/MUM1和IgM, 65%表达MYC,2/3的PCDLBCL,LT双表达MYC和BCL2,有助于与PCFCL鉴别(图5)。30%的PCDLBCL,LT有MYC基因重排,少数病例同时有BCL6重排。
图5 PCDLBCL,LT。(A)排列紧密的大的转化细胞,核仁突出;(B)BCL2强表达;(C)IgM阳性;(D)MYC阳性
遗传学研究不但有助于了解这些淋巴瘤的分子发病机制,对诊断和预后也有帮助。CDKN2A缺失和MYD 88L265P突变见于2/3的PCDLBCL,LT,提示预后较差。MYD 88 L265P突变和B细胞受体信号通路基因突变,提示PCDLBCL, LT中的NF-κB激活, PCDLBCL,LT中还存在PDL1/PDL2易位,这些改变与DLBCL,NOS的ABC亚型有交叉,与原发中枢神经系统淋巴瘤和原发睾丸淋巴瘤非常相似。PCFCL中无MYD88L265P突变,CDKN2A缺失或失活也很少见。PCDLBCL,LT应与医源性免疫缺陷相关LPD和继发性皮肤DLBCL区别。
PCDLBCL,其他在2005年WHO-EORTC分类中引入,它包括以皮肤为首发表现的DLBCL且不能归类为PCDLBCL,LT或PCFCL,2018 WHO-EORTC分类中不再包含该类型,少数不能归类为PCDLBCL,LT或PCFCL的病例,诊断为原发性皮肤DLBCL,NOS。
血管内大B细胞淋巴瘤很罕见,定义为血管腔内大量肿瘤B细胞积聚,通常影响中枢神经系统、肺和皮肤,预后不良。有一种局限性皮肤疾病变体,主要影响女性,预后优于系统性疾病。
EBVMCU和其他皮肤免疫缺陷相关B细胞LPDs
EBV+粘膜皮肤溃疡(EBVMCU)指孤立的、轮廓清楚的溃疡,累及皮肤、口咽粘膜或胃肠道,患者为年龄相关或医源性免疫抑制(甲氨蝶呤、硫唑嘌呤、环孢素、肿瘤坏死因子抑制剂)。病变在混合炎症背景中,有大的、霍奇金样EBV+ B细胞, PAX5+,可表达CD20,非生发中心表型(IRF4/MUM1+),典型表达CD30,一半病例共表达CD15。EBVMCU通常自限性,惰性过程。医源性病例中,单纯减少免疫抑制治疗即可病情完全缓解。
医源性免疫抑制时还可有其他B细胞LPDs的皮肤表现。甲氨蝶呤相关B细胞LPDs通常表现DLBCL或霍奇金样病变的组织学特征,后者在EBV+病例中常见。识别医源性免疫缺陷有关病变很重要,因为减少或停用免疫抑制治疗可能使病情缓解。
Willemze R, Cerroni L, Kempf W etal. The 2018 update of the WHO-EORTC classification for primary cutaneous lymphomas[J].Blood 2019, 18;133(16):1703-1714.
欲了解更多血液肿瘤、淋巴瘤相关资讯,与全国各地血液肿瘤、淋巴瘤医生交流讨论,请扫描以下二维码,备注“血液肿瘤”,添加【肿瘤资讯-娜小编】微信!