7000字详解“AI+放疗”的临床痛点、核心技术与行业前景(附PPT下载)
作为医学影像AI细分市场中的蓝海,放疗靶区勾画受到许多企业、投资人、医生和技术研究者的关注与青睐。
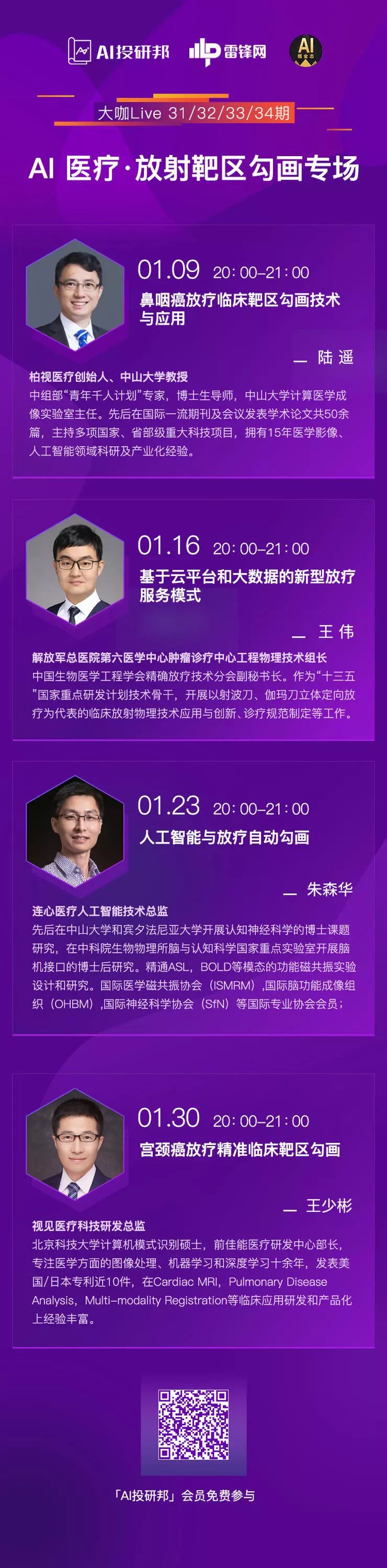
为此,AI掘金志【大咖Live】精心策划了一个四期的“智能放疗靶区勾画”系列课程,邀请资深行业专家进行线上分享。
系列课程第一期,分享嘉宾柏视医疗创始人陆遥从临床痛点、核心技术、发展前景三个维度对鼻咽癌放疗的智能靶区勾画技术作了详细介绍。
陆遥教授是美国雪城大学&中科院数学与系统科学研究院双博士学位,中组部“青年千人计划”专家,中山大学教授、博士生导师,中山大学计算医学成像实验室主任。先后在国际顶级期刊及会议发表学术论文共50余篇,主持多项国家、省部级重大科技项目和课题,拥有15年医学影像及人工智能科研及产业化经验。
以下是陆遥教授的全部分享内容,AI掘金志在不改变原意的基础了做了整理和精编(关注“AI掘金志公众号”,对话框回复关键字“放疗”,下载完整课程ppt):
大家好!我是陆遥,广州柏视医疗科技有限公司创始人。今天向大家介绍柏视在放疗靶区勾画方面的工作。这是本期报告提纲,以鼻咽癌为例介绍放疗靶区勾画的技术思路和临床应用。
背景介绍
首先介绍鼻咽癌放疗靶区勾画背景情况,包括鼻咽癌的定义,2018年全球及中国鼻炎癌发病率情况,目前主要的治疗手段以及放疗中靶区的定义,以及柏视在鼻咽癌放疗靶区勾画方面的技术方案(GTV分割和CTV预测),并重点介绍基于小样本的OAR分割技术。
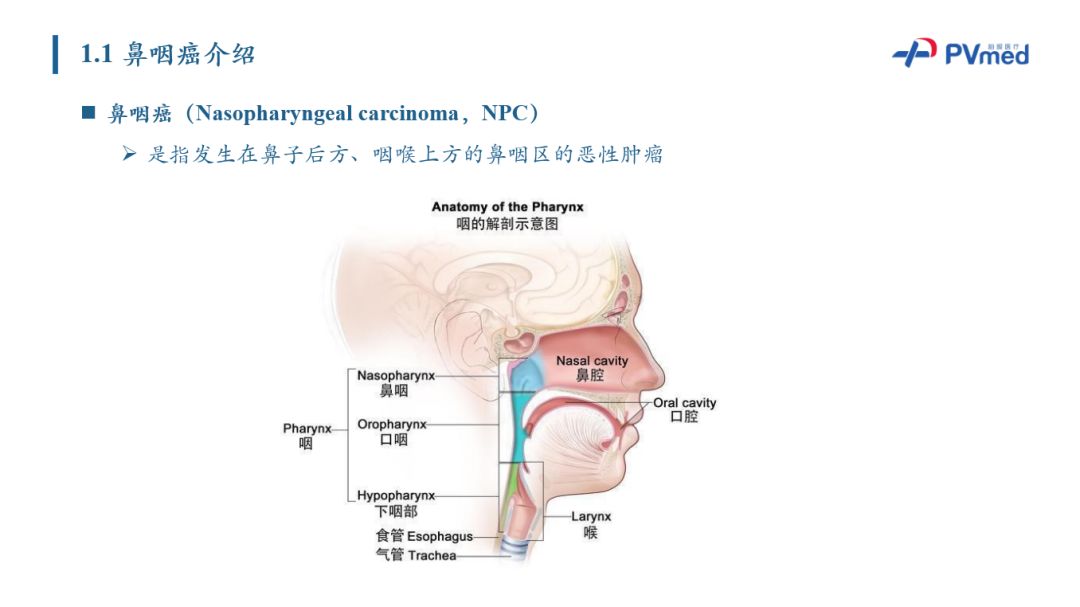
首先介绍鼻咽癌放疗靶区勾画的相关背景。鼻炎癌指发生在鼻子后方、咽喉上方的鼻咽区的恶性肿瘤。2018年9月份的数据调查显示:全球范围内,2018年1-9月,新增鼻咽癌病例接近13万,占所有癌症病例的0.7%,在全球癌症发病率排名25位,其中死亡病例大概7万例,占全球癌症死亡病例0.8%,死亡率排名21位 。
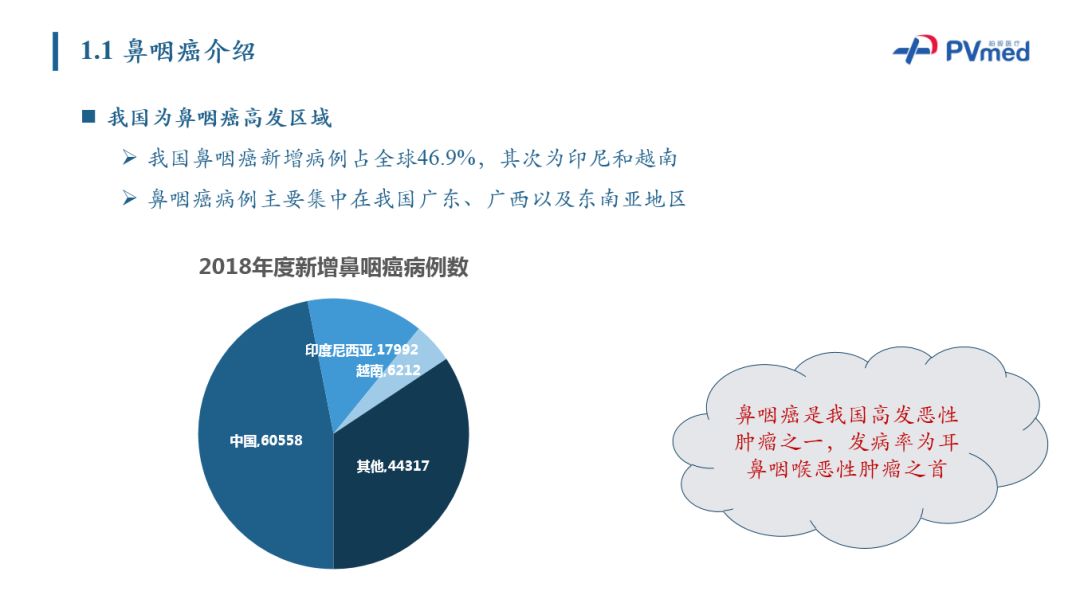
尽管在全球范围看,鼻咽癌新发病例数占新增癌症病例比例并不高,但在中国而言,新发病例比例是全球的两倍(占比1.47%)。数据统计显示:在以上全球新增的13余万鼻炎癌病例中,超6万例发生在中国,占46.9%,即近一半的新增病例出现在中国。
受到遗传、环境或病毒等因素的影响,中国鼻咽癌大部分集中在广东广西等华南地区,尤其广东为高发区。所以鼻咽癌又称为“广东癌”。印尼、越南等东南亚国家也是鼻咽癌高发区。总体来看的话,鼻咽癌是我国和东南亚地区的高发癌症,其发病率是耳鼻咽喉恶性肿瘤之首。
世界卫生组织将鼻咽癌分成三种类型:第I型,角化鳞状细胞癌(高分化);第II型,非角化癌(中分化);第III型,未分化癌;在中国地区,95%的鼻咽癌为第III型,其余5%中,绝大多数为第II型,大多数鼻咽癌病例对放射治疗具有中度敏感性。鉴于鼻炎和颅底接近,60%-70%的患者在就诊时可能会出现颅底骨质破坏,约18%患者伴有颅内或者海绵窦的侵犯,因此手术比较困难。 同时约85%的患者伴有颈部或者咽喉淋巴结转移,不适合进行手术。
从鼻咽癌分类比例来看,大部分病例对于放射治疗具有中度敏感性,因此放射治疗是鼻炎癌主要的治疗方法。调强放疗是目前鼻咽癌治疗的主要手段。在放射治疗前的话,它需要医生制定放疗方案,包括放疗、确定照射的区域,照射的强度等,因此需要在影像上对相应区域轮廓进行勾画,包括肿瘤区域、临床靶区、危及器官、计划靶区。
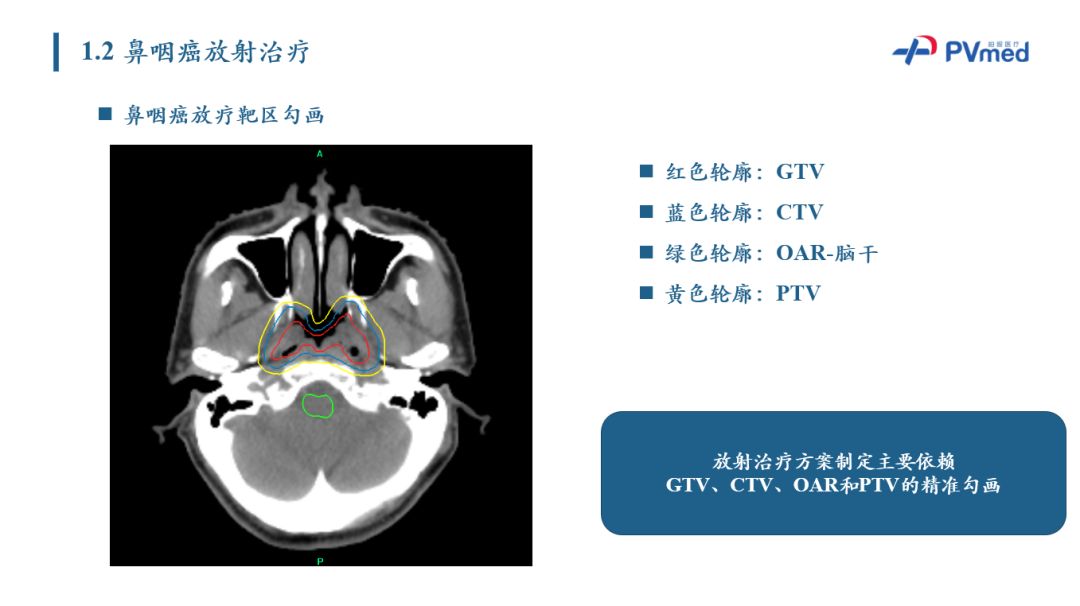
肿瘤靶区(GTV)在临床上可见,或临床可证明的恶性肿瘤生长位置,是肿瘤实际所在区域。临床靶区,包含GTV在内的具有一定肿瘤扩散概率的区域,是放射治疗临床照射区域。危机器官是指头颈部正常组织器官,其需要在放疗时尽量避免照射。OAR辐射敏感性将显著影响治疗计划。计划靶区为放射治疗计划引入的概念(即PTV),PTV对于鼻咽癌而言相对较简单。一般情况,我们会把GTV和CTV会外扩一定距离。
以上图为例,不同颜色轮廓代表不同区域。 红色的轮廓是GTV,蓝色的轮廓是CTV,绿色的轮廓是在这一层勾画出来的脑干危机器官OAR,黄色的轮廓是PTV。对于放疗医生而言,其在制定治疗方案的过程中的主要工作之一就是完成靶区勾画。对于物理师而言,其根据规划结果,对加速器的设备参数进行配置,来完成放疗过程。目前放疗靶区勾画临床痛点是勾画效率较低,绝大多数放疗靶区目前主要依靠放疗医生手动勾画。对于一个有经验的医生来说,勾画一个完整的鼻炎癌放疗靶区需要2-3小时。这占用了放疗医生大量的工作时间。
根据早前数据,我国鼻咽癌发病率远高于全球平均水平。但是我国放疗医生和物理师的数量严重不足,这导致我国恶性肿瘤治疗中放疗采用率相对较低,远远达不到70%的理论推荐值。换句话说,很多患者无法得到及时有效的治疗。
技术方案
鼻咽癌放疗靶区勾画另一临床痛点即靶区勾画主观性强,对放疗医生要求高。基层医院医生普遍经验不足,独立完成靶区勾画较难。这会导致两方面的问题:一方面即靶区不精准会导致放疗难以达到预期效果;第二方面即危机器官分割不精确、对危机器官过量照射会导致并发症。譬如可能出现口干、进食困难、颞颌关节功能障碍、放射性颌骨骨髓炎和放射性脑脊髓病等并发症,这会影响病患生活的质量。
针对上述临床痛点,柏视提出并实现了一套鼻咽癌放疗靶区的智能勾画技术方案。柏视目标是希望通过技术手段来实现放疗靶区的自动勾画。一方面为放疗医生提供完整治疗方案的参考,另一方面支持医生基于自动勾画结果进行手动调整。
既要提高靶区勾画效率,同时保证勾画精准程度。柏视之所以能够实现以上目标,是基于多年来在行业内的技术和数据积累。近年来,以整机神经网络为代表的深度学习技术迅速的发展,并且在医学图像处理领域有诸多成功应用。随着放射治疗技术的发展和医学成像设备的普及,放疗领域积累了大量历史数据。随着GPU的发展,计算能力突飞猛进,这为深度学习在放射治疗领域的应用奠定了基础。
目前医学影像分割技术仍然面临着挑战,比如医学影像对比度较低,存在多层影像间的信息依赖。因为肿瘤通常为三维目标,需要对多层影像特征进行关联分析。另外,前景与背景极度不平衡,数据需求量大,训练样本标注时间成本过高也是一大问题。
这是柏视医疗技术路线的核心思路,也是技术亮点。即采用基于知识的小样本机器学习算法,将医生临床知识病史等临床数据和影像的深度学习相结合,能够极大的降低模型训练所需要的样本量,同时也有利于技术模型和产品的快速成型。
基于这一技术路线,柏视医疗在GTV勾画、CTV预测以及OAR分割方面都取得技术突破。GTV勾画相较CTV影像(例如磁共振影像对软组织的对比度)更强,因此更容易将早期的肿瘤组织与咽喉鼻咽癌(例如淋淋巴结区域)分开,在磁共振影像方面对GTV区域的诊断更加精准,也可降低GTV区域在治疗中被遗漏的风险。因此柏视选择在MA序列上进行GTV自动分割。同时在临床上会采集多个序列MA图像以为更准确的分割。
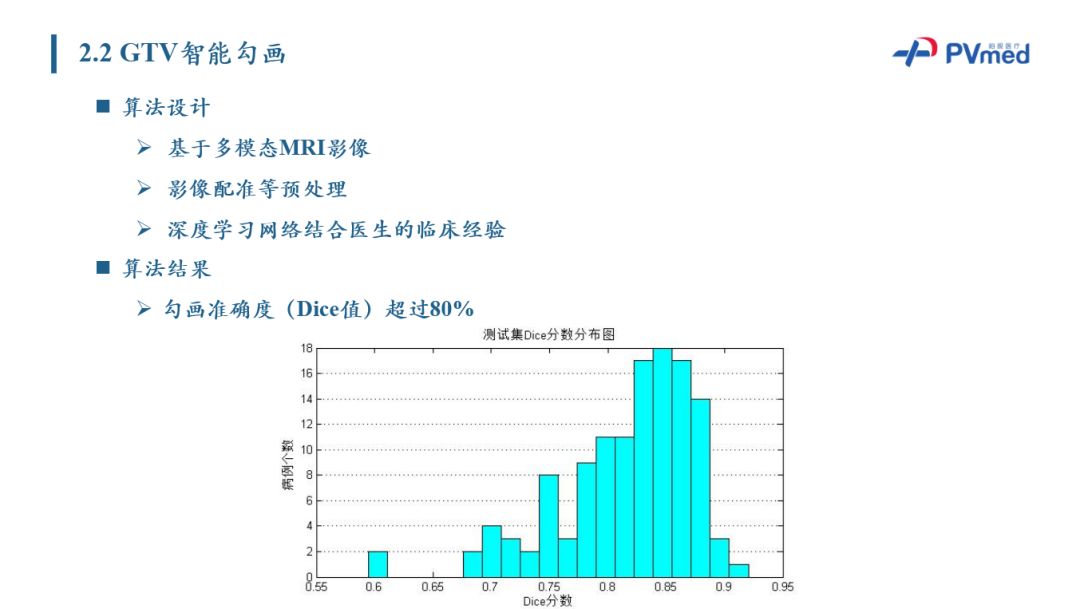
柏视同时采取多序列进行分割,由于MI图像灰度值无法对应到特定组织,即使相同的病人,在相同的机器和不同的时间下,采集到的图像可能出现不同的灰度分布。为保证模型的鲁棒性,柏视对图像进行了大量的数据规范化预处理,保证图像灰度分布的规范化。在此基础上,柏视再将机器学习技术、深度学习网络和医生临床经验相结合,进行模型训练和优化,得到GTV自动勾画算法。
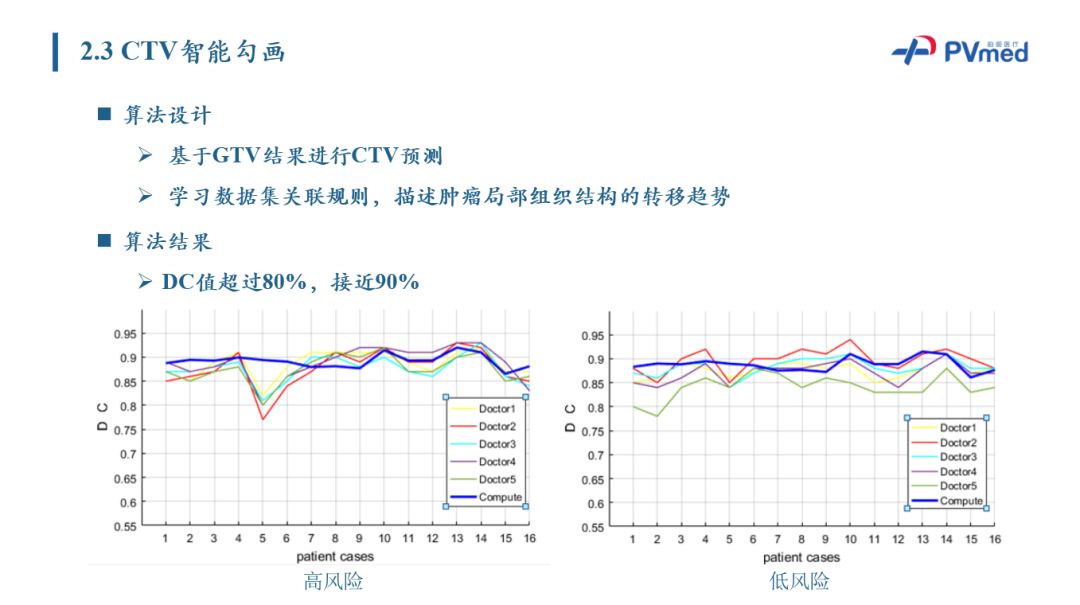
很坦率的说,整个过程中标注的质量非常重要。柏视通过和主任级别的医生进行合作,对测试数据的勾画结果进行统计,并以主任级专家勾画结果作为参考,以这种Dice值作为评价的标准,算法勾画准确度超过80%,达到了很高的勾画准确度。基于GTV结果进行CTV预测,柏视从训练数据集中来学习图像特征,来描述肿瘤局部组织结构的转移趋势。并且在此基础上,柏视对CTV进行预测。为达到更好的应用的体验,CTV预测算法提供了多种这种概率的等高线供医生来选择。
通过抽取约一百个病例作为测试数据,柏视以中山大学肿瘤医院主任级别的专家勾画结果作为参考标准,同时选取五个临床医生的CTV勾画结果作为对比。从Dice系数来看,算法自动勾画DC值超过80%,接近90%,高于对比组医生的平均水平。如果用Patient cases作为衡量指标,算法同样具有比较好的勾画结果,MSD平均值约为2mm。
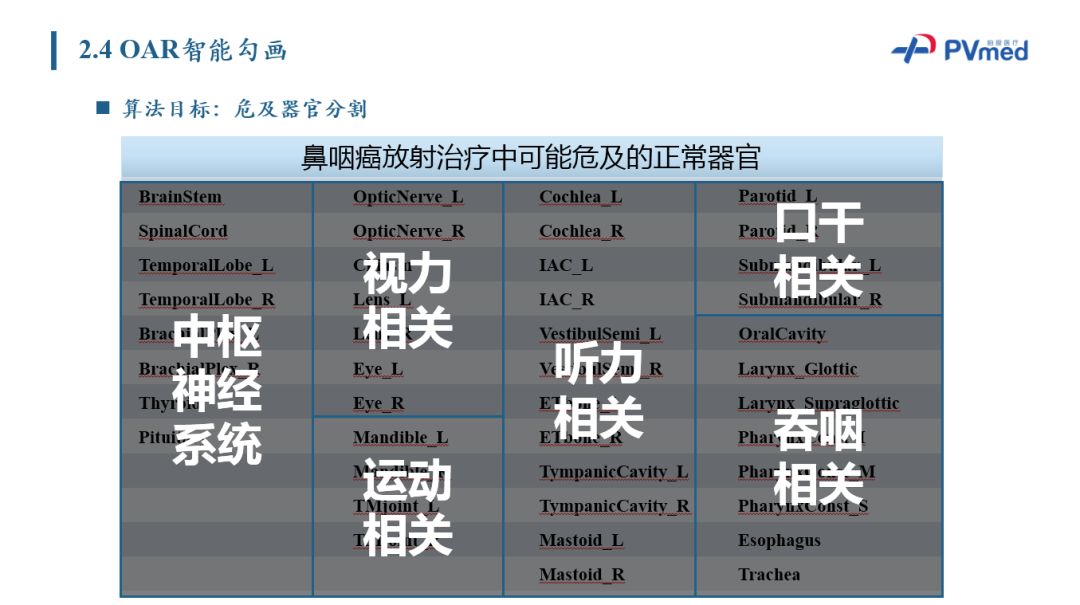
放疗会出现口干(进食困难)、放射性脑脊髓病等并发症,主要一大原因即危机器官受到影响。针对鼻咽癌放疗的临床需求,柏视大概共分割出临床上需要保护的43个器官,包括中枢神经、视力、运动、听力、口干和吞咽相关的六大部分器官,据调研,目前关于上述器官分割报道并未出现。
头颈部危机器官分割方面,存在以下几大挑战:
待分割器官数量较多;
分割器官的体积差异较大,体积低于1cc的器官超过15个;
各个器官之间的灰度特征存在较多的共性,对比度比较差。在这种情况下,临床经验不足的医生很难从图像上分辨出目标的分界线,例如腮腺和下限、视神经视交叉、垂体等;
危及器官覆盖的区域非常广,上至头部的颞叶,下至靠近肺部的脊髓和臂丛神经。
对于OAR智能勾画目前已有一些分割的算法,大致分为三类:
ABAS:ABAS基于单个或者多个模板,通过配种方法实现目标病例上的器官分割,从而可以减少不同医生勾画的差异,这也是自动勾画的主要优势之一。基于同样的原因,ABAS方法对于病人和模板之间的解剖学差异非常敏感。在低对比度器官,尤其是小结构分割上,它表现比较差。
与视觉相关的危机器官分割研究,对多种商用的ABAS方法进行了验证,结果发现其在向小脑、脑干、眼球这等大结构分割的准确度比较高,但是在低对比度或者小结构上的分割精度非常差。
第二类比较流行的方法是主动形状模型,其基本原理如图所示,首先给定初始轮廓线,通过最小化能量函数驱动轮廓线上的点,沿着梯度方向进行移动,通过多次的迭代能够得到目标的分割轮廓线。
如图所示,通过若干次迭代,模型更好的收敛到目标轮廓线附近。但分割对于初始的轮廓线要求较高,如果没有较好的初始化,有可能得到完全错误的分割。对于主动轮廓或者主动形状模型,称之为偏微方程算法,多和梯度流算较好的紧密结合。柏视合伙人是GTV的提出者,在该领域有较多研究。传统的方法或多或少依赖简单的先验知识或者好的初始化条件,例如病人解剖结构,基本稳定相形变比较小,但一旦条件无法满足时,这个方法通常会失败。迅速发展的深度学习提供了一种以特定目标导向来学习历史数据的方法。
该图较好地展示了机器学习中卷积神经网络的强大学习能力。其在多种模态或者多个部位数据的训练下,CNN针对不同的图像,在多数的情况下能得到较好的结果。对于多目标的分割,传统的算法中较难实现,但对于深度学习而言较容易。
这篇文章中,卷隙性神经网络用于头颈部肿瘤放疗的危机器官分割有非常好的表现,且方法非常自然。即基于图像配置训练分类网络,对于图像中像素点为中心的配置进行分类,从而实现目标分割,同时添加可随机模型对分割进行后处理,对离散的过分割点进行去除。
相比较于传统算法,基于CNN分类的分割算法,在大多数的危机器官上明显优于传统方法,但在小结构分割上依然不理想。
这是沈老师团队在该领域的研究,基于随机森林的方法,首先检测多个目标的关键顶点,然后加入形状鲜艳的信息来逐步迭代检测更多目标表面的顶点,从而最终实现分割目标。迭代策略是非常好的人类行为。首先粗略地找到目标,然后逐步进行修改,最后比较精确的结果。 基于这样的方法,最后得到分割的结果具有人类手动勾画的特征,比如离散分割比较少、层间截段等,比常规的机器学习收敛效果更好。
对上面介绍的三类方法优缺点进行一下总结:
ABAS方法,无需训练,分割快速。缺点就是依赖配准算法和模板,分割准确度不高;
ASM方法,则无需配准,无需模板,无需训练,但是需要较好的初始化,依赖形状先验;
ML方法,具有极强的学习能力,能很好的学习历史数据信息,但是可解释性有待提高。
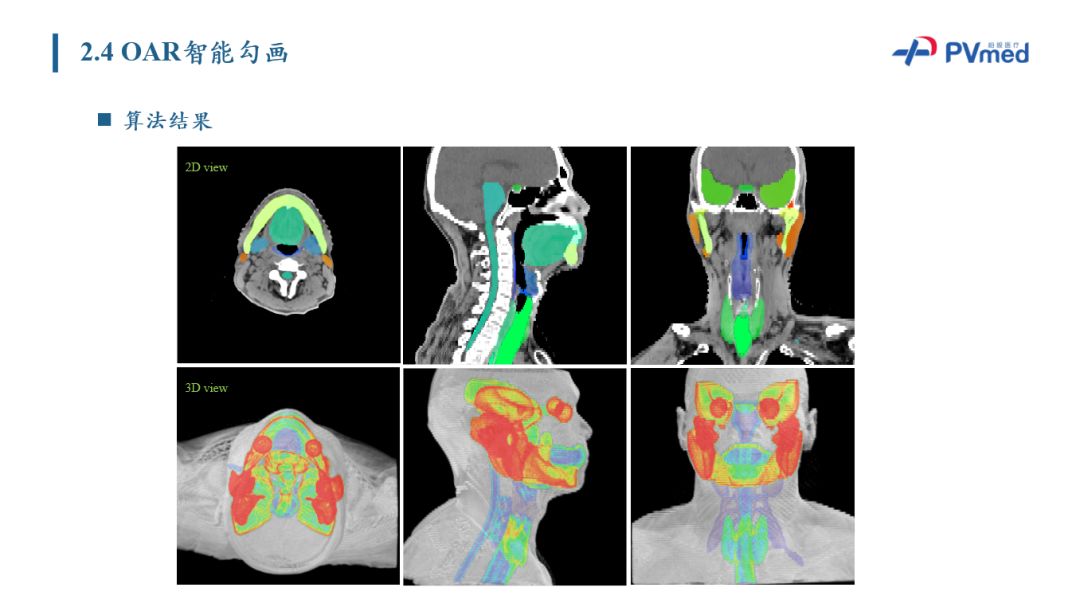
柏视技术方案以DICOM图像输入,以深度学习作为基本框架,在目标区域上采用迭代分割的模型对目标器官进行分割。对于迭代分割的思想,它其实是一个普世性框架,需要同医生经验进行结合、增强。这是柏视算法所做的分割测试例子,上面是二维的三个断面的是R视角,下面是所有器官分割结果的三维的展示,不同的颜色代表不同的危机器官。
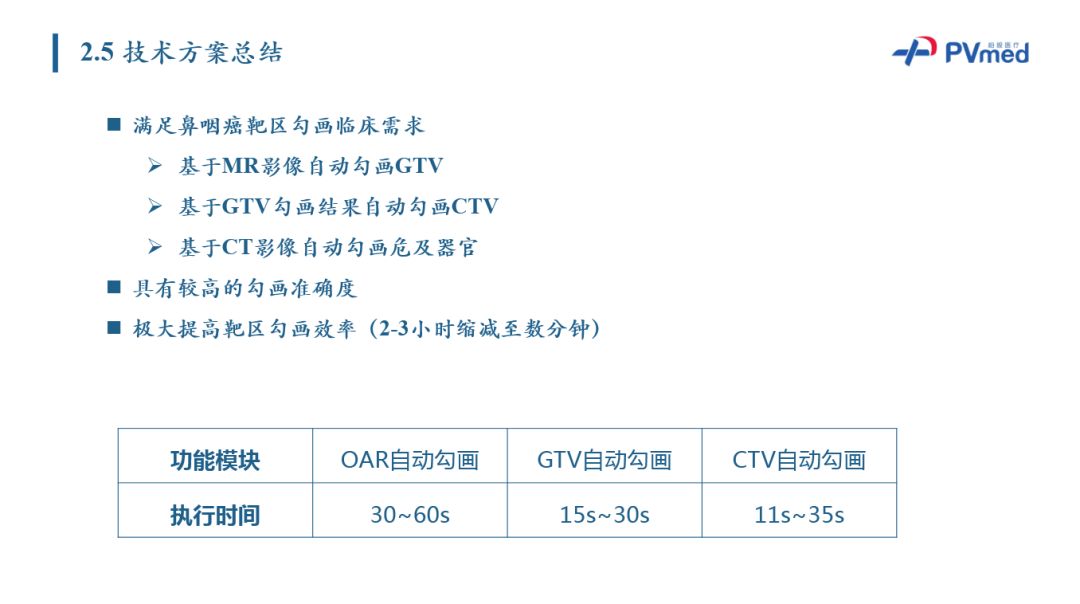
总结来看,柏视提出鼻咽癌靶区勾画技术方案,它包括GTV勾画、CTV预测和OAR分割。基于柏视算法,放疗医生工作时间由2-3小时缩减至数分钟。柏视提供模板算法算出的模板,同时也提供编辑工具帮助医生在模板的基础上进行分割,可较好地满足靶区勾画的临床需求。
临床应用
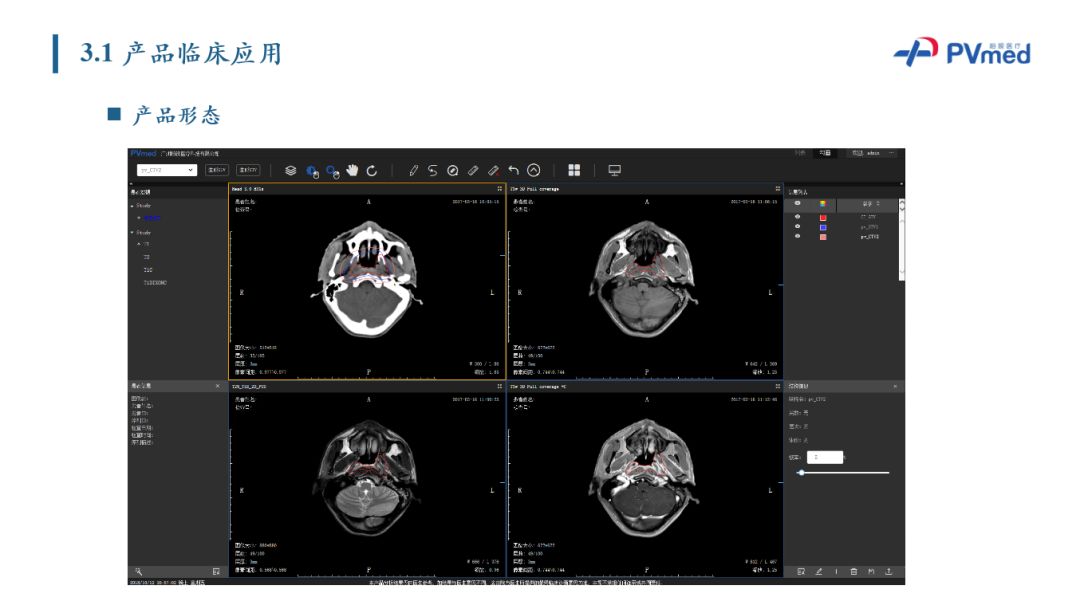
面向GTV勾画、CTV预测和OAR分割功能,柏视在发展云平台提供产品化的服务,并在合作的医疗机构中进行临床试用。接下来介绍柏视产品临床应用情况。
柏视鼻咽癌靶区勾画产品目前在临床上进行试用,提供多模态影像同步的修改。对于轮廓线,柏视也提供便利的修改辅助工具。其中一个亮点是,右侧结构信息模块可以通过调整肿瘤发生可能性的百分比,来控制CTV预测的轮廓范围。
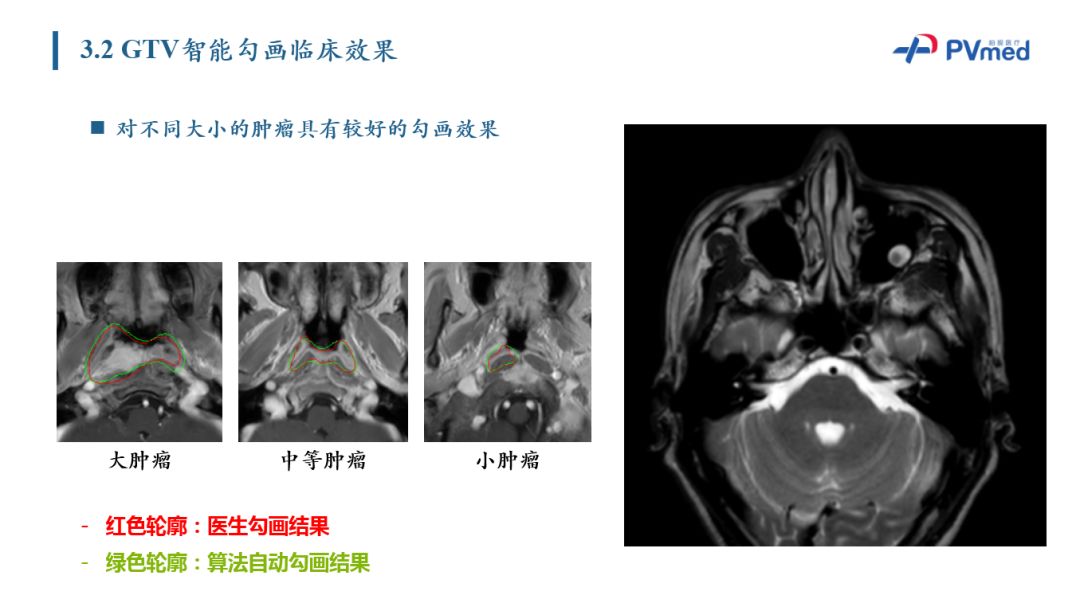
从GTV规划的临床效果来看,左侧展示了对于大中小尺度的肿瘤算法都能够有比较好的勾画的效果,右侧是对患者的GTV勾画结果动态展示。和医生勾画的轮廓线相比较的话,算法分割的结果在Z轴方向有较好的三维连续性,在病灶首尾两端存在一定的分割误差,这也是由医生在病灶首尾两端存在不同的勾画分割所造成的。
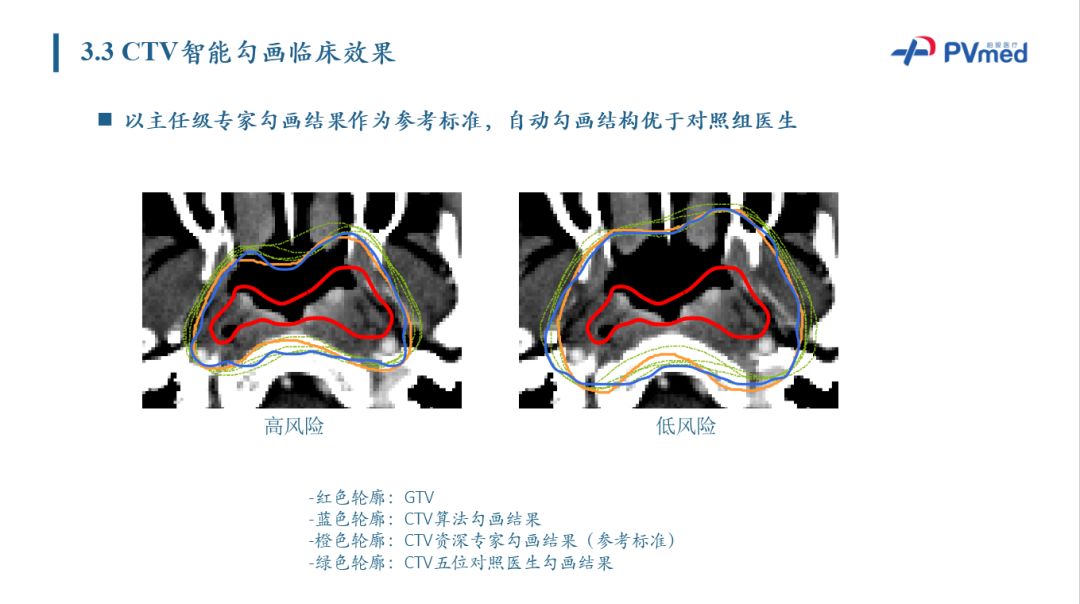
对于CTV预测临床效果,在图中可以看到,无论是高风险还是低风险的CTV预测,预测结果和参考的资深医生勾画的CTV轮廓是基本一致的。 相较于资历较浅医生所勾画的CTV,自动预测的CTV精准度高于对比医生的平均水平。
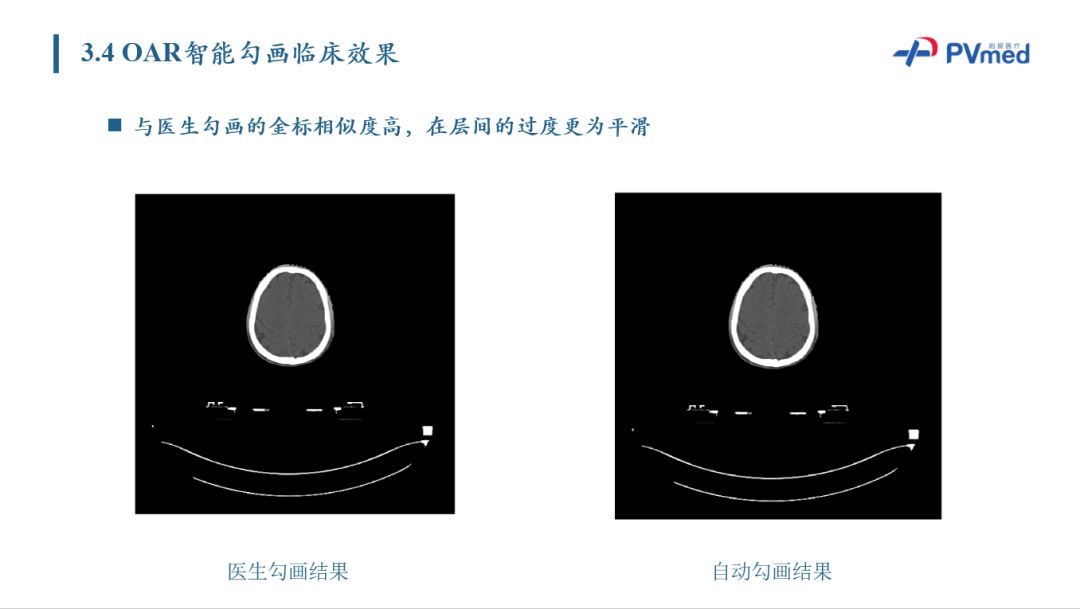
在OAR分割临床效果方面,与医生勾画的金标相似度高,并且在层间的过度更为平滑。除了自有的放到云平台的产品,柏视医疗还针对鼻咽喉勾画产品的特点进行多样化落地应用。目前作为唯一的第三方人工智能模块,与飞利浦IntelliSpaceDiscovery(ISD)平台实现集成,落地吉大一附院。对于此类产品,柏视作为第三方的医疗模块进行平台级合作。
发展前景
下面将基于柏视在放疗靶区勾画领域长期以来的研发工作和临床的实践,从技术产品市场角度对该领域未来发展前景做展望:
靶区规划技术的发展趋势:目前靶区勾画技术水平依然较大的提升空间,主要体现在三个方面。
一:靶区勾画精准度还需进一步提升,尤其是算法。面向来自不同医院或不同成像设备,影像泛化性能,需要不断提高勾画结果的精准程度,以更好地体现临床的价值。
二:进一步提高靶区勾画算法的速度,目标是希望把分钟级的算法执行度缩短到几秒之内。
三:更好地融入临床医生的工作流程。
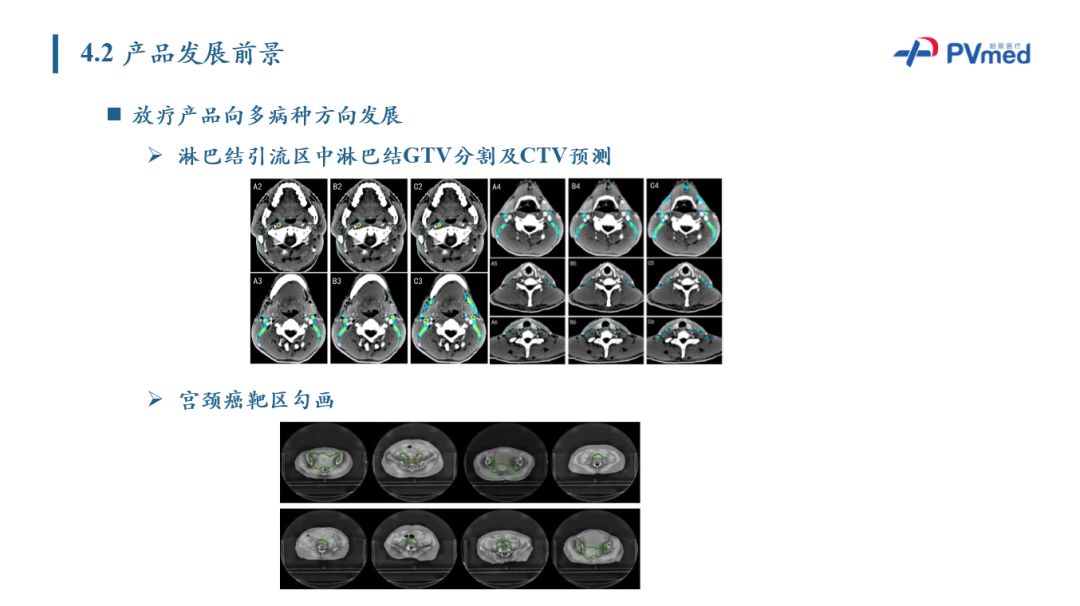
其次是放疗靶区勾画产品的趋势,即多病种的靶区勾画是主要产品拓展方向。柏视已经开始进行淋巴结引流区中淋巴结GTV分割及CTV预测,且目前已有较好的工作。这里展示的是淋巴结引流区的典型层面中不同组别淋巴结的分布的概率。
放疗也是宫颈癌的主要治疗手段之一,宫颈癌靶区勾画也是虚构化产品的主要的方向。
最后是放疗靶区勾画的市场前景。从医学影像的整体市场来看,由于医药分离政策因素的影响,医学影像以及基于影像的诊疗,成为医疗机构的重要收入来源。据相关机构预测,医学影像市场规模将保持超过20%的增长速度,2020年,医学影像市场规模将达到6000-8000亿。
另一方面,放疗市场近年来也在不断的增长,国内放疗市场年复合增长率约为25%,2015年已达269亿。目前放疗采用率还处于较低水平,随着放疗采用率的逐步提高,放疗市场还有较大的上升空间。如果放疗采用率达到理论推荐的70%,我国放疗的市场空间则将达到800 亿。总体来看,放疗靶区勾画的市场发展方向非常好。作为提供靶区勾画产品和服务的企业而言,它更重要的是把握市场拓展的路线和方向。一方面逐步提高三甲医院的使用率,在同样的医疗资源条件下,能够收治更多的放疗病患,帮助医院增收。另一方面,逐步向基层医院普及,帮助拥有放疗设备的基层医院提供高质量的放射治疗,避免病患外流,在促进完善分级诊疗的同时提高基层医院收入。
公司概况
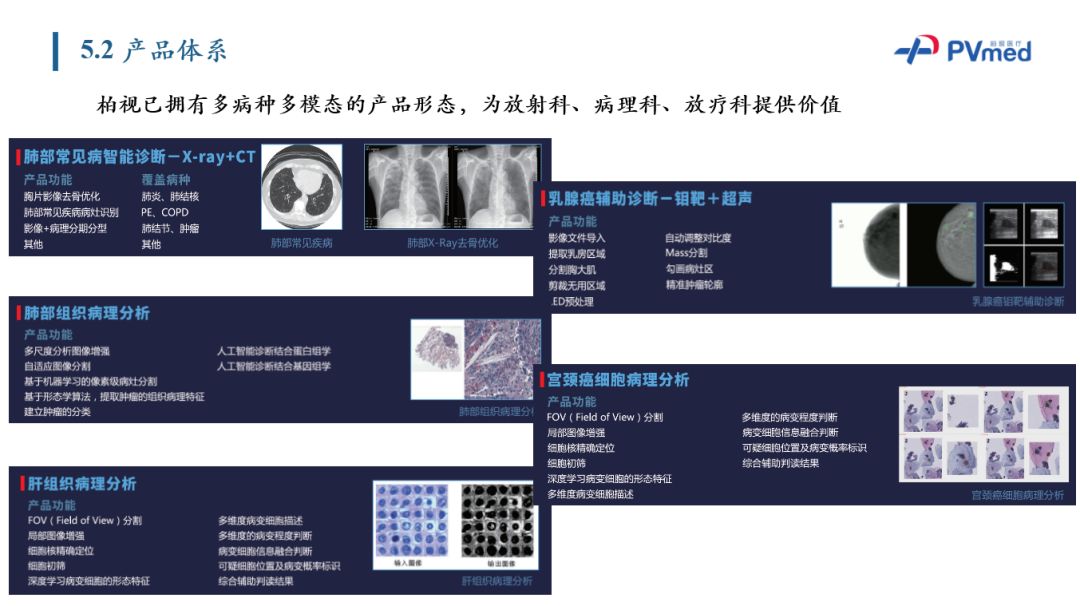
最后简单介绍柏视医疗科技有限公司。柏视定位于医疗人工智能技术引领者和技术提供商。公司成立于2017年5月,现已发展为业内最具竞争力的初创企业。公司形成了核心技术优势,同时也打造了领先的产品的体系。目前柏视医疗以放疗为主,形成一个多模态多病种的产品体系,打通了影像、病理、放疗科,从而真正实现了从诊断到确诊到治疗的数据流和工作流。
除鼻咽癌放疗靶区勾画之外,柏视已拥有多病种多模态的产品形态,为放射科、病理科、放疗科提供价值。公司具有顶级计算机辅助人工智能团队,具有多年顶级的人工智能的技术积累和丰富的医疗资源。本人也在医学院工作多年,一直从事医疗人工智能研究,所以在行业内有多年的积累。团队研发占据80%,大部分具有海归经历,因此是一个典型的技术型公司。
Q&A
1. 在放疗靶区勾画领域,传统机器学习技术和深度学习技术哪个更有优势?
对于深度学习而言,它是一个典型的记忆性学习方法。其好处是可以从数据中总结和归纳一些规律。但正因如此,对于总结出来的规律或准则,很难解释或形成临床经验。在这种情况下,通过传统机器学习基于既定规则,同医生经验结合。因此对于传统机器学习应该有效的和深度学习结合,把可解释的机器学习算法和基于数据的深度学习的算法结合是未来发展的一个方向。
2. 除了鼻咽癌,还有哪些癌症的AI放疗靶区勾画是发展前景比较好的?
除了鼻咽癌,放疗科肿瘤的AI放疗靶区勾画均是发展前景,例如肺、乳腺、结直肠、宫颈、前列腺,目前放疗科的应用越来越多了。在癌症中,鼻咽癌是技术难度最高的,因其在头颈部位,解剖结构也最复杂。当初柏视选择该病种也是和医生之间用科研合作方式进行,即医生认为最难的病种。
3.是否基于双能CT图像进行勾画?
双能CT对于危机器官的勾画是有帮助的,可以较好的对危机器官进行区域分割和深度学习。
4.请问为什么OAR或者靶区勾画都在CT图像上做呀?MR图像是不是会有更好的软组织对比度呢?
实际上,对于医学影像而言,特别是MR图像,其整个规范化处理相对比较困难。在这种情况下,同时要在灰度域和空间域来进行数据处理。为了让视觉影像达到更好的效果,需要灰度域和空间域同时进行。
MR图像对软组织分辨率非常好,因此GTV勾画也在MA上进行。目前直线加速器计划制定依旧在CT图像上进行。
本系列课程的最后一期,将于1月30日(本周三)晚上八点开讲。届时视见医疗科技研发总监王少彬将分享他在鼻咽癌、宫颈癌两个病种的放疗靶区勾画中的技术探索与实践。欢迎扫描下方图片中的二维码关注课程。「AI投研邦」会员免费参与直播或收听音频版。
推荐阅读
「AI投研邦」首份年度福利,错过再等一年
*点击图片查看详情