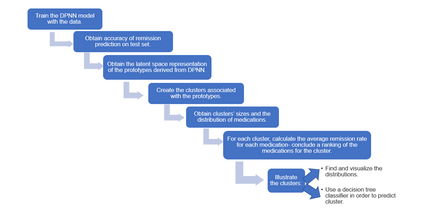
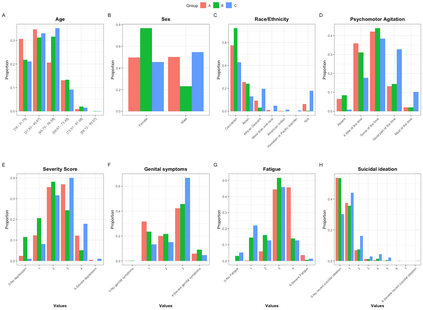
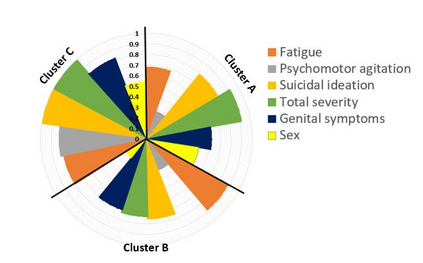
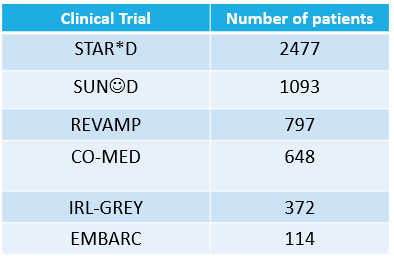
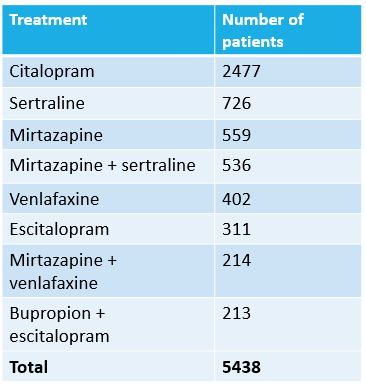
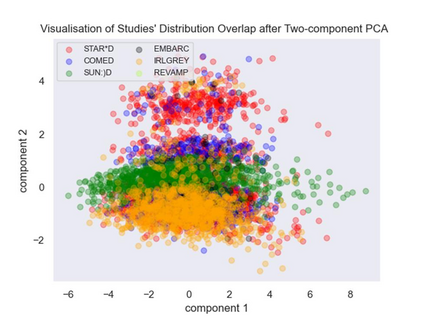
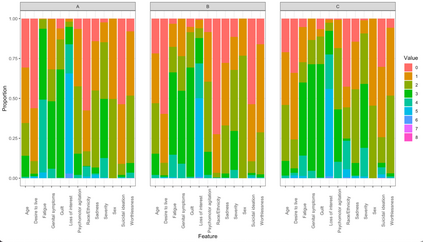
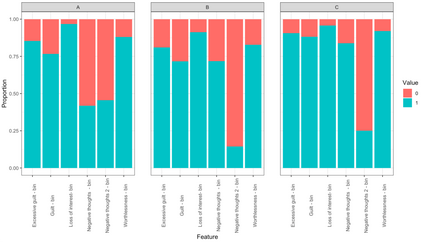
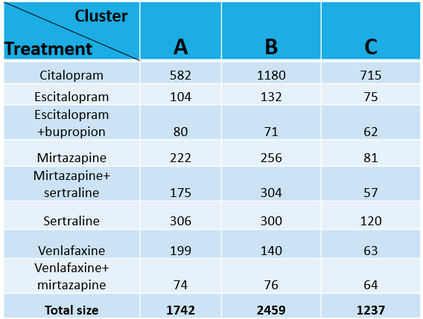
Major depressive disorder (MDD) is a heterogeneous condition; multiple underlying neurobiological substrates could be associated with treatment response variability. Understanding the sources of this variability and predicting outcomes has been elusive. Machine learning has shown promise in predicting treatment response in MDD, but one limitation has been the lack of clinical interpretability of machine learning models. We analyzed data from six clinical trials of pharmacological treatment for depression (total n = 5438) using the Differential Prototypes Neural Network (DPNN), a neural network model that derives patient prototypes which can be used to derive treatment-relevant patient clusters while learning to generate probabilities for differential treatment response. A model classifying remission and outputting individual remission probabilities for five first-line monotherapies and three combination treatments was trained using clinical and demographic data. Model validity and clinical utility were measured based on area under the curve (AUC) and expected improvement in sample remission rate with model-guided treatment, respectively. Post-hoc analyses yielded clusters (subgroups) based on patient prototypes learned during training. Prototypes were evaluated for interpretability by assessing differences in feature distributions and treatment-specific outcomes. A 3-prototype model achieved an AUC of 0.66 and an expected absolute improvement in population remission rate compared to the sample remission rate. We identified three treatment-relevant patient clusters which were clinically interpretable. It is possible to produce novel treatment-relevant patient profiles using machine learning models; doing so may improve precision medicine for depression. Note: This model is not currently the subject of any active clinical trials and is not intended for clinical use.
翻译:抑郁症是一种异质性疾病,多种潜在的神经生物学基础可能与治疗反应的变异有关。了解这种变异的来源并预测结果一直是困难的。机器学习在预测MDD治疗反应方面显示出了潜力,但其局限性在于机器学习模型的临床可解释性不足。我们利用差异原型神经网络(DPNN)分析了6个药物治疗抑郁症的临床试验数据(总样本量n = 5438),这是一种神经网络模型,它可以得出治疗相关的患者集簇,同时学习生成差异性治疗反应的概率,其中利用了辅助性临床和基本数据信息。我们使用这个模型训练了一个分类缓解的模型,并对五种一线单药和三种联合治疗进行个体缓解概率输出。根据曲线下面积(AUC)和模型引导治疗中预期的人群缓解率提高来测量模型的有效性和临床效用。后续分析利用了在训练期间学习的患者原型产生集群(亚群)。通过评估特征分布和治疗特异性结果之间的差异,评估了原型的可解释性。一个3-原型模型达到了0.66的AUC和对人口缓解率的预期绝对提高,这些结果比样本缓解率高。我们确定了三个与治疗相关的患者集群,它们在临床上是可解释的。使用机器学习模型可以生成新的与治疗相关的患者配置文件,这可能改善抑郁症的精准医学。注意:该模型当前不是任何主动临床试验的研究对象,也不是用于临床目的的。