清华大学生命科学学院江鹏课题组在《自然》发表文章报道肿瘤氨代谢异常的分子机制及功能
美国东部时间3月6日,清华大学生命科学学院江鹏课题组在《自然》(Nature)杂志上发表了题为《p53通过尿素循环调控氨代谢进而控制肿瘤细胞多胺合成》(p53 regulation of ammonia metabolism through urea cycle controls polyamine biosynthesis)的研究论文,报道了肿瘤氨代谢异常的分子调控机制和功能。
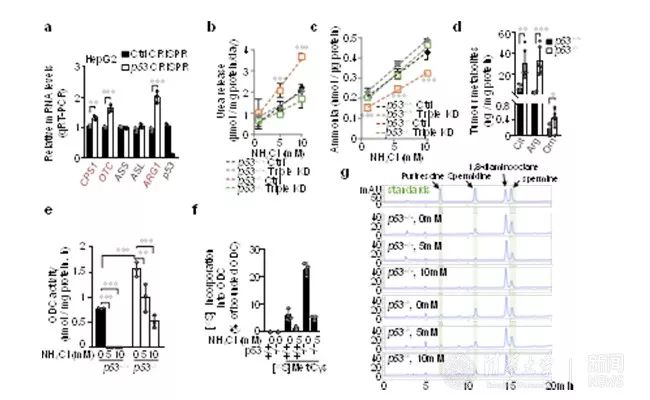
图1. (a,b),p53调控尿素循环代谢酶基因表达(a),和尿素释放(b)。(c-g),p53通过尿素循环调控了氨的生成(c),肿瘤生成(d),细胞内ODC的酶活性(e),ODC蛋白翻译(f)和多胺合成(g)。
肿瘤细胞为了满足其快速增殖或存活的需要,会改变其一些重要的代谢途径,而异常改变的、高活性的代谢过程(包括蛋白降解和含氮物质的合成代谢等)往往会伴随着氨的生成。而在这种情况下,肿瘤细胞如何处理氨的累积?以及大量氨的存在会带来怎样的后果或影响?多年来我们对此却并不清楚。
在本项研究工作中,研究者发现肿瘤细胞内介导氨代谢的尿素循环受到肿瘤抑制因子p53的调控,p53的缺失或突变的肿瘤细胞或小鼠体内表现出高水平的尿素循环代谢酶(Carbamoyl Phosphate Synthetase 1, Ornithine transcarbamylase 和 Arginase 1)的表达和氨基酸的合成。体内、体外的数据表明,p53对尿素循环的抑制导致了氨的积累和肿瘤生长的抑制。同时还发现:氨的累积反馈激活p53,而这一过程与MDM2有关。有趣的是,尿素循环的代谢酶的表达和功能具有组织依赖的特性,而p53选择调控了该循环途径中一半以上的反应步骤,在一定程度上暗示了p53对此途径的监控强度之强,以及该途径的重要性。因此,对于氨代谢的调控可能是p53影响肿瘤发生发展的一个重要的分子机制。
为了进一步弄清氨累积抑制肿瘤的原因,研究者进行了更加深入的机制挖掘。研究发现,多胺合成途径中的限速酶ODC (ornithine decarboxylase)的活性与p53的表达,尿素循环的活性,以及氨累积呈现显著的负相关。p53抑制尿素循环代谢途径导致的氨累积可直接下调ODC的mRNA翻译,进而导致细胞内总体ODC的活性降低,使得多胺合成受阻,减慢肿瘤细胞的增殖。
这项工作的发现,首次将p53与氨代谢直接联系起来;同时揭示了氨的过度积累可以被ODC的蛋白翻译过程所“感知”,具有调控多胺合成,从而影响肿瘤细胞增殖的生物学功能。
清华大学生命学院2014级博士生李乐为该论文的第一作者。清华大学生命学院江鹏研究员为论文通讯作者。本项目的研究得到了清华大学生命学院俞立教授的帮助和大力支持。该研究由国家自然科学基金委、青年千人计划项目和CLS提供了经费支持。
论文链接:https://www.nature.com/articles/s41586-019-0996-7

来源:清华新闻网
供稿:生命学院