传奇PCR:从科学狂想到普通医学检验室,这个故事里每个关键人物都手握诺奖
1993年,Kary Mullis因发明了聚合酶链式反应(PCR)获得了诺贝尔化学奖[1]。1998年,《纽约时报》一篇文章提到PCR时,不吝惜赞美地写道,“生物学以此划分为PCR前和PCR后两个时期。”[2]
这并非溢美之词。自双螺旋被阐明,人们对生命的理解进入DNA分子时代,几乎所有需要研究遗传物质的人,都无法离开PCR。
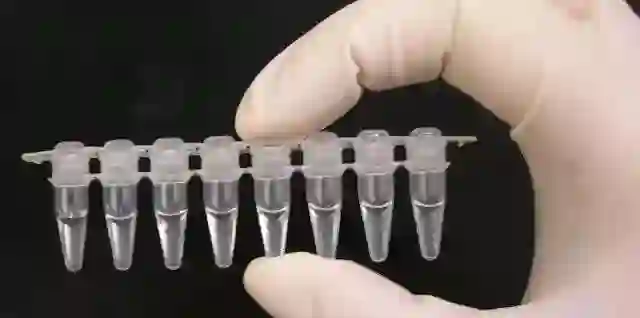
在它出现以前,扩增DNA序列需要在细菌中进行,整个过程可能需要几周;使用PCR,你只需要几个EP管,把原材料加进去丢进热循环仪,然后静静等上几个小时,就能够得到几何数级的产物。
从高中课堂到顶尖实验室、从医院到外太空,PCR默默地绽放着光芒[3]。
而在它的背后,几乎每个值得被记录下来的名字都手持诺奖。
撰文 代丝雨
来源 Dr.Why
沙之塔
说起来还真有点儿怪,PCR使用范围之广,很难让人相信它是一种出现还不到半个世纪的技术。换个角度理解,PCR也可以算是某种程度的厚积薄发,它能够取得今日的成就,还是因为站在巨人的肩膀上。
1953年4月,DNA的双螺旋结构首次与世人见面[4],人类对生命终极的认知走入了分子层面,发现者之三Waston、Crick和Wilkins因此在1962年被授予诺贝尔生理学或医学奖。
在探索DNA结构过程中做出贡献的科学家们,左一、左二、右二获得1962年诺贝尔生理学或医学奖
1957年,美国科学家Arthur Kornberg发现了第一种DNA聚合酶[5],人类了解到,DNA的复制是在引物引导下、由酶的作用、以脱氧核苷酸为材料向单一方向延伸。当然,在复制之前,还有更复杂的打开双螺旋等等过程。Kornberg在1959年获得了诺贝尔奖。
Arthur Kornberg
差不多同一时期,印度裔美国科学家H.Gobind Khorana成功破解了所有的密码子。为了完成人类功能性基因全合成的伟愿[6],他在此后的科研生涯中开创了许多合成寡核苷酸所需要的技术。1968年,他因破解遗传密码获得诺贝尔奖。
三年后,Khorana和他的学生Kleppe在《分子生物学杂志》上发表了一篇论文[7],文内首次提到了双引物系统和“修补复制”的概念,这是PCR技术的雏形。
H.Gobind Khorana漫画形象
1969年,Tomas Brock从黄石国家公园的高温温泉中鉴定到了全新的耐热细菌,Thermus aquaticus[8]。
1976年,Jhon Trela和他的学生,华人科学家钱嘉韵成功从该菌种内提取到了能够耐75℃以上高温的TaqDNA聚合酶[9]。
发现了Thermus aquaticus的热泉口
1971年,Cetus Coporation宣告成立,这家公司的创始人之一Donald Glaser是1960年诺贝尔物理学奖获奖者。顶尖的科学家、前沿的科学视角,让这家公司成为日后孕育PCR技术的摇篮。
1977年,Frederick Sanger发明了桑格测序法[10],基因组全面向人类敞开,再无秘密。他因此在1980年获得诺贝尔化学奖。
至此为止,PCR技术所需的所有基础材料都已摆上桌台,只剩耐心等待天选之人的到来。
Cetus是出现得最早的生物技术公司之一,只可惜,这家本有希望成为业界领头羊的公司只在历史上出现了短短20年。这短暂的时光里,它带来了包括白介素-2、β干扰素在内的几种重要药物,以及最关键的PCR技术。
Cetus也很关注DNA诊断,它与Perkin-Elmer共同研发了第一台热循环仪,还与柯达合作商用诊断试剂盒(对就是那个柯达)。
创始之初,Cetus致力于研究工程菌的自动化筛选方法,这些细菌可以用于生产大量的化学原料、抗生素以及疫苗的组分。
那个年代,生物学时时刻刻都在发生巨变,没过几年,DNA重组技术、单克隆抗体、基因表达这三项革命性的技术出现,新的生物技术产业即将成型。Cetus快速跟上节奏,1981年首次公开募股,便筹集了1.08亿美元。这个数字即使放到今天,也值得称上一句天价IPO。
cetus是鲸鱼座的意思
Cetus的业务中心主要都放在白介素-2上。这块竞争十分激烈,除了Cetus以外,还有Genentech、Immunex(后来成了Amgen的一部分)等颇有实力的公司,以及一位名为Tadatsugu Taniguchi的日本研究者在进行IL-2基因的克隆研究。
1982年,Taniguchi率先完成了人源IL-2的克隆,不过次年Cetus就搞定了独家的重组版本,同时用于治疗肾癌的临床试验也开始进行了[11]。
看看现在IL-2用得多广,我们就知道这块蛋糕确实美味。Cetus对它寄予厚望,几乎把全公司的资源都倾倒在IL-2的开发上,甚至在FDA还没有批准上市之前,Cetus已经为IL-2建造了两座工厂和配套的基础设施,前期的资金投入高达1.27亿美元。
值得一提的是,为了支持IL-2的研发,Cetus从1987年开始就对外授权PCR技术的使用,尽管当时很多外部人都认为PCR才是Cetus最有价值的产品。
然而很悲剧,1990年,FDA驳回了Cetus对IL-2的上市申请。实际上当时Cetus的IL-2产品,患者的响应率并不是很高,只有10%-20%的肾癌患者获得了有效治疗;与之相对的是,药物的副作用巨大,严重的液体潴留可能会危及患者生命[12]。
FDA认为还需要更多的临床试验来验证IL-2的效果,现在它还未到时候。可是Cetus等不起了。当年,Cetus年报亏损23%,CEO辞职,公司不得不通过大幅度裁员来消减成本。
然而这也没能拯救Cetus下坠的趋势。1991年,Cetus被成立于1981年的后起之秀Chiron以7亿美元的价格收购。次年,IL-2才以Prileukin之名进入市场,同时PCR技术专利被罗氏控股Hoffman公司以3亿美元全盘收购。
冠上Chiron名字的IL-2
说来遗憾,Cetus拥有当时业界顶尖的科学家、雄厚的资本、有前景的产品,但是在IL-2上过于孤注一掷。这赌博似的行为导致了全盘皆输,Cetus一夜消失在了历史的洪流里。
现在让我们回到1953年,双螺旋发现的那一年。那年Kary Mullis 8岁,正是和小伙伴们漫山遍野瞎跑的年纪。在他出生的1944年,薛定谔出版了《生命是什么》。当然了,8岁的他既看不懂这部生物学著作,也完全理解不了DNA结构的发现到底意味着什么。事实上很长一段时间里,他都对生物学毫无兴趣。
Kary Mullis
比起生物,Mullis反倒在化学领域上显得颇有天赋。十几岁的时候,他就从家里偷来糖,混上药店里买来的硝酸钾,和小伙伴们自制火箭;在乔治亚理工学院修习化学学位期间,他也常常自己合成有毒物质和爆炸物。很幸运,几乎没人管他,那段时光让Mullis掌握了不少有机化学知识。
所以到底为什么他选择了生物化学作为接下来的研究方向呢?Mullis自述只对小分子感兴趣,而PCR出现之前的DNA又长又“稳如泰山”,和他喜欢的化学合成完全搭不上边。修完硕士修博士,在加州大学伯克利分校读了六年生物化学,到1972年毕业,Mullis依旧是只懂化学,不懂生物。
好在他的导师Joe Neilands很宽容,他并不限制学生选课程,所以Mullis赫然选修了一门天体物理学。神奇的是这门课他可能学得不错,甚至在1968年时发表了一篇名为《十年逆转的宇宙学意义》的论文,发在《自然》上。多亏了这篇论文,要不然他恐怕拿不到博士学位。
Mullis此时应该没想到自己日后的成就
毕业后,Mullis没有想好要做什么,于是就先随着妻子来到堪萨斯州。起初他想当个作家(执念很深,后来确实出书了),但是遗憾的是毫无天赋。随后他在医院工作了一段时间,又因为离婚回了伯克利,做了两年餐馆的经理人。
这里要提到一位好朋友Tomas White,是这位朋友劝说他回到学校继续深造,也是White介绍他到Cetus工作,后来又在Mullis难以立足的时候拉了他一把。
Mullis来到加州大学旧金山分校,进行药物化学的博士后研究。学习期间,他了解到,DNA也可以通过化学方法来合成。Mullis对此产生了兴趣。1979年,他来到Cetus的时候,也是负责合成寡核苷酸,给公司其他部门的同事使用。
Mullis确实在化学合成上有天赋,他很快搞出了计算机自动合成程序,工作流程大大简化。1981年,他就当上了实验室的负责人。
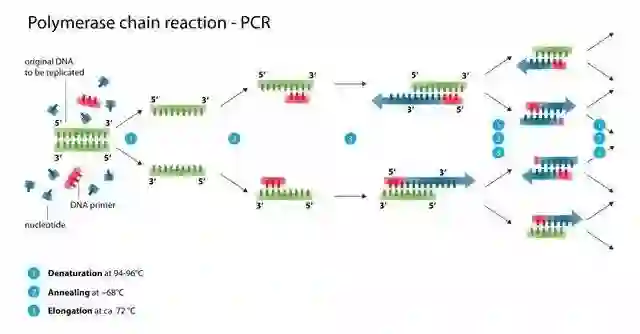
1983年春天的一个夜晚,Mullis载着当时同在Cetus工作的女友从旧金山前往乡下度过周末。汽车行驶在蜿蜒盘旋的128号公路上,此时一个念头出现在Mullis的脑海中——扩增DNA片段时,如果同时添加两条引物,分别扩增正义链和反义链,那么只要引物足够,岂不是可以无限循环地扩增下去!
Mullis马上靠边停车,掏出纸笔开始演算。这种扩增方法,每个循环得到的DNA都是上一循环的二倍,那么循环10次DNA就能扩增1000倍,循环个30次就能达到10亿倍!
这个数字太惊人了,这个思路也太简洁了,Mullis一时之间都无法相信,之前居然从未有人尝试过。他反复查阅资料之后,在Cetus内部的科研会议上分享了自己的想法。然而奇怪的是,同事们完全不觉这有什么厉害之处。
Mullis花了几个月时间寻求认同,但赞同他观点的科学家寥寥无几,这期间他与女友的感情也出现了裂缝,直到9月,他才开始第一次实验。
如果顺利,DNA将不断以倍数扩增
在诺奖致辞中,Mullis提到他不喜欢重复劳动,如果一件事需要反复做同一个流程,那么他会倾向于写个程序来解决。所以那个夜晚,他把聚合酶加入试管后就径直回家了,满心以为DNA已经在管中自己成倍增加了。
然而第二天中午,Mullis没能在凝胶中看到期望的条带。他不得不承认,反复地加热、冷却、添加聚合酶,这枯燥的工作是绕不过去的坎儿。
接下来的三个月里,Mullis磨磨蹭蹭地进行着实验,同时为了感情问题焦头烂额。终于在飘雪的圣诞节,他终于成功实现了扩增一个pBR322质粒的一个25bp长的片段,同时也失去了爱情。
事情进展并不顺利。1984年中,Mullis再次在Cetus的会议上向同事汇报了自己的成果,结果依旧无人感兴趣。也是在这个会上,Mullis和另外一位同事发生了口角,上升到了肢体冲突。这个突发事件以Mullis降职、另一人离开公司结束。
Mullis的好友White此时已经当上了Cetus的技术副总裁,他帮助Mullis拉起一支小组专门研究PCR,其中有个名为才木的日本人。不知是不是日本人天性严谨又勤劳,这支小组成立后,研究很快得到了推进,他们成功扩增了一个110bp的人源蛋白基因片段。
进行了更多的尝试之后,研究者们决定撰写两篇论文,Mullis主导的一篇介绍PCR技术理论,才木主导的另一篇介绍PCR技术的应用。
出于某些原因——笔者本人相信可能是Mullis的拖延癌又犯了——当才木的论文写好时,Mullis几乎还没动笔。
在前几节我们提过,此时Cetus正把全力投在IL-2开发上,公司急于从科研公司转型到制药公司,没有时间耗费在不知能不能变现的技术上。高层没法等Mullis完成论文,便催促才木赶快先把应用论文发表。
12月,才木的论文发表在了《科学》上,题目是《β-珠蛋白基因组序列的酶促扩增和限制性位点分析诊断镰状细胞贫血》[13]。
Mullis的论文就没那么好运了,他先后投了《自然》和《科学》,都因为内容不够“原创”被拒稿,最后不得已投了《酶学方法》,论文直到1987年才出版[14]。
同一年里,Cetus内另一组科学家也在为PCR的进化添砖加瓦。PCR最初的版本使用的是来自大肠杆菌的DNA聚合酶,这种酶不耐热,必须每个循环都重新添加,大大降低了自动化程度。
Cetus与Perkin-Elmer合作开发的热循环仪原型机,因为需要持续添加DNA聚合酶,所以采用了敞口、机械臂移动的方式
从耐热菌中分离聚合酶的想法是谁提出的不确定,最后进行这项工作的是David Gelfand和Susanna Stoffel。两位科学家在秋天从Thermus aquaticus中分离到了能够在95℃高温下依旧不失活的TaqDNA聚合酶,Taq酶马上就被应用到了PCR中。
这就是我们现在也在使用的PCR第一次完整出现。
1986年的热循环仪原型机
看起来PCR已经走过最艰难的时刻,是该享受光辉和荣耀的时候了。然而不知为什么,共过苦的伙伴,却很难同甘。
一方面,是PCR发明人的身份争议;另一方面,Cetus对PCR团队也着实不太公平,虽然Mullis获得了一万美元的奖金,但是团队里的其他人只是象征性地收到了一美元,这让他们与其他团队之间的分歧更大了。1986年,Mullis选择了离开Cetus。
1991年,Cetus折戟梦途;1992年,身价3亿美金的PCR专利去往新东家Hofmann-La Roche;1993年,Mullis登上诺贝尔领奖台,大谈童年时光与128号公路上的那个夜晚[15]。
Mullis与PCR的故事其实到这里就差不多已经全部说完了。纵观他的一生,Mullis表现出很多并不那么像个德高望重的诺奖获得者的特征。
Mullis在诺贝尔获奖致辞中反复提到分手的女友,甚至表示获奖的喜悦也抵消不了失去这个姑娘的悲伤——就算那已经是十年前的事情了——表现得像个痴心的情圣,可他50岁前就结了四次婚。据称他在男女关系上确实不那么保守,也曾因此在公司内引发问题。
White把Mullis描述为一个充满创造力,但是有些过于随心所欲的角色[16]。Mullis才华横溢,而且没有对权威的畏惧,但是另一方面他并不那么自律,实验进行得断断续续,这是他无法在Cetus内部取信于人的原因之一。他俩的友谊最后没能持续下去,但在之后的舆论纷争中White一直站在Mullis的一边。
Mullis还有些不那么登得上台面的小爱好。1938年,Albert Hofmann首次合成了LSD,这种物质在十年后被引入精神疾病治疗领域,然后在短短几年时间内成了倍受年轻人喜爱的时髦小玩意儿,成为史上最有名的致幻剂[17]。Mullis上学的时候也好这一口——这是他亲口告诉Hofmann的——并且Mullis认为LSD带来的幻觉帮助他在128号公路上找到了PCR的灵感。
Mullis还有些甚至不太像科学家的地方。比如他认为HIV病毒并非AIDS的病因、全球变暖是个伪命题;他相信占星术,相信转世,还宣称自己曾与伪装成荧光浣熊的外星人对话[18]。
还有一个有趣的细节。前文曾讲过,Kleppe1971年发在《分子生物学杂志》上的论文首次提到了修补复制的概念,也提到了双引物系统。
人类学家Paul Rainbow曾写过一本书“Making PCR:a story of biotechnology”,详细地讲了整个PCR的发现故事[11],书中提到,其实1969年的高登会议上,Kleppe就公开发表过这个观点,当时在场的科学家中有一位名为Stuart Linn。
巧了,这位科学家正是Mullis就读加州大学伯克利分校期间的一位老师,而Linn也的的确确曾在课堂上演示过Kleppe的设想,实验也成功了。所以Rainbow认为,Mullis可能只是个“追随者”,并非“开创者”。
Mullis是个“好人”吗?我们不知道。但是PCR,真真实实地改变了世界。
PCR诞生之后,科学家们迅速意识到了这门新技术的价值,Cetus内部即有学者开始尝试使用PCR测定血液中的HIV病毒循环量,并很快取得了关键的突破[19]。基于这项成果,人们得已对捐献的血液进行病毒筛查,并直接检测抗病毒药物的疗效。
这项技术在几年内得到了极大的发展。基于PCR bug一样的的扩增能力,从极微量的样本中提取遗传信息成为可能。最直观的应用就是在法医学上,例如著名的辛普森杀妻案,能够给犯人定罪就少不了PCR的功劳。
还有考古学,有了PCR就可以从几万年前的化石里获取来自远古的遗传信息用于分析,如果将来真的像《侏罗纪公园》那样重新培育出恐龙,PCR技术一定不会缺席。更近一些,最有名的故事可能是寻回英国国王理查三世遗体的故事了(就是莎士比亚那个理查三世)。
理查三世
理查三世是金雀花王朝的最后一位国王,在玫瑰战争的最后一场战役里,他与自己的士兵一起葬身战场、匆匆被埋葬,以至于之后的五个多世纪都没能找回。直到21世纪到来,通过放射性碳测年找到尸骨、与其姐姐女性后代比对线粒体DNA,这才确认了理查三世的尸骨并重新安葬[20]。
在医疗方面,PCR才是真正的改变了世界。产前检测、组织分型、癌基因突变检测、诊断传染病、鉴定微生物……有了PCR的出现,人类以前所未有的速度认识了这个世界,逐渐把生命的真相抓在手中。
结合新出现的事物,PCR还在不断地出现新的变体。2018年,PCR技术35周岁,而立之年,仍旧大有可为。
如果说PCR有什么缺点,那么可能成本是个问题。PCR最关键的过程就是热循环,为了保证精准的温度变化,昂贵而笨重的设备必不可少,这使得PCR的使用限于实验室内。
近年来有研究者试图解决这个问题。他们采用一些更加轻薄、体积更小的薄膜电阻加热器,取代传统的热电装置,其他结构也选了更加简单的部件。这种新的名为MiniPCR的系统更小更轻,而且更便宜。
这种设备很适合中等教育需求,一些野外科学家、食品公司都在使用这个系统。最令人惊喜的是,这种设备很适应太空环境,国际空间站的工程师也在使用。
还有些科学家正在试图让PCR出现在我们的手机上。Biomeme尝试把光学传感器安装到手机上,用APP监控实时定量PCR(RT-qPCR),能够在线分析数据,并且在手机上实时检查实验进度。
用PCR进行微生物检测也有了新的进展。日本一家乳品公司的科学家正在开发一种基于钯的试剂,这是一种DNA交联剂,能够特异性进入死亡的细菌,防止其DNA的扩增。使用这种技术,PCR可以快速检测生产的食品中是否含有未被杀死的致病菌[21]。
还有我们最关注的癌症。液滴数字PCR(ddPCR)出现了,它的特点在于PCR反应是在上千个纳米级别的液滴中进行的,每个液滴都是单独的反应池,通过荧光标记来检测靶序列的含量。这种技术精度更高、需要的样品量更少,在液体活检领域可以大显身手。
而且或许在不久之后,使用PCR可能不需要再重复加热、退火这个过程了。科学家们已经发现了能够在恒定温度下进行DNA复制循环的酶。等温扩增(LAMP)除了不需使用热循环仪进行操作,还能够直接分析新鲜或冷冻血液样本中的点突变,甚至是纸张上面的干血斑也行,再也不用提取DNA了[22]。
令人激动的时代,令人激动的技术。期待它的下一个35年。
参考资料:
[1] Shampo, M. A.; Kyle, R. A. (2002). "Kary B. Mullis — Nobel Laureate for procedure to replicate DNA". Proceedings. Mayo Clinic. 77 (7): 606. doi:10.4065/77.7.606. PMID 12108595.
[2]https://www.nytimes.com/1998/09/15/science/scientist-at-work-kary-mullis-after-the-eureka-a-nobelist-drops-out.html
[3]http://www.sciencemag.org/features/2018/05/pcr-thirty-five-years-and-counting?_ga=2.214061143.1757775300.1531552304-1663670973.1526261271
[4] Watson JD, Crick FHC, "structure of DNA", natural volume. 171, pp.737-738 (1953).
[5] Lehman, IR, Bessman MJ, Simms ES, Kornberg A "Enzymatic Synthesis of Deoxyribonucleic Acid. I. Preparation of Substrates and Partial Purification of an Enzyme from Escherichia coli" J. Biol. Chem. vol. 233(1) pp. 163–170 (1958).
[6] Khorana HG et al. "Total synthesis of the structural gene for the precursor of a tyrosine suppressor transfer RNA from Escherichia coli. 1. General introduction" J. Biol. Chem. vol. 251(3) pp. 565–70 (1976).
[7] Kleppe K, Ohtsuka E, Kleppe R, Molineux I, Khorana HG "Studies on polynucleotides. XCVI. Repair replications of short synthetic DNA's as catalyzed by DNA polymerases." J. Molec. Biol. vol. 56, pp. 341–61 (1971).
[8] Brock TD, Freeze H "Thermus aquaticus, a Nonsporulating Extreme Thermophile" J. Bacteriol. vol. 98(1) pp. 289–297 (1969).
[9]Chien A, Edgar DB, Trela JM "Deoxyribonucleic acid polymerase from the extreme thermophile Thermus aquaticus" J. Bacteriol. vol. 174 pp. 1550–1557 (1976).
[10] Sanger F, Nicklen S, Coulson AR "DNA sequencing with chain-terminating inhibitors" Proc Natl Acad Sci vol. 74(12) pp. 5463–7 (1977).
[11] Paul Rabinow. Making PCR: A Story of Biotechnology. University of Chicago Press, 1996 ISBN 978-0226701479
[12]https://www.nytimes.com/1990/07/31/business/cetus-drug-is-blocked-by-fda.html
[13] Saiki RK et al. "Enzymatic Amplification of β-globin Genomic Sequences and Restriction Site Analysis for Diagnosis of Sickle Cell Anemia" Science vol. 230 pp. 1350–54 (1985).
[14] Mullis KB and Faloona FA "Specific Synthesis of DNA in vitro via a Polymerase-Catalyzed Chain Reaction." Methods in Enzymology vol. 155(F) pp. 335–50 (1987).
[15]https://www.nobelprize.org/nobel_prizes/chemistry/laureates/1993/mullis-lecture.html
[16]https://www.nytimes.com/1998/09/15/science/scientist-at-work-kary-mullis-after-the-eureka-a-nobelist-drops-out.html
[17] "Hallucinogenic effects of LSD discovered". The History Channel. Archived from the original on March 11, 2014.
[18] Dancing Naked in the Mind Field. 1998, Vintage Books.
[19] Kwok S, etc. "HIV sequences were identified by in vitro enzymatic amplification and oligomeric cleavage." J. Virol. The first volume. 61 (5) pp.1690-4 (1987).
[20] https://en.wikipedia.org/wiki/Richard_III_of_England
[21] T. Soejima, K. Iwatsuki, Appl. Environ. Microbiol. 82, 6930–6941 (2016).
[22] L. Detemmerman, S. Olivier, V. Bours, F. Boemer, Hematology 23, 181–186 (2018).
[23]http://www.sciencemag.org/features/2018/05/pcr-thirty-five-years-and-counting?_ga=2.214061143.1757775300.1531552304-1663670973.1526261271
本文转载自公众号“Dr.Why”(ID: DoctorWhy-Geekheal)