又是海马体,这次发在Cell!科学家发现:海马体中新神经元的来源
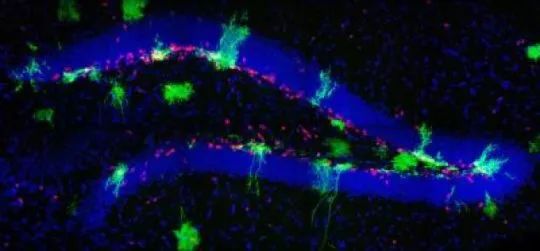
曾经有人认为,哺乳动物出生时会有一生所有的神经元供应。 然而,在过去的几十年中,神经科学家已经发现,大脑至少有两个区域——嗅觉中心和海马体——在整个生命中能生长出新的神经元。近期发表在Cell上的一篇研究不仅证实了这一观点,而且对大脑海马体中新神经元的来源进行了探究。
(DOI:https://doi.org/10.1016/j.cell.2019.02.010)
宾夕法尼亚大学的研究人员通过小鼠实验发现,海马体内新生神经元来源于一种制造成年神经元的干细胞。这些发现将有助于神经学家弄清楚如何保持年轻态的学习和记忆条件,以及大脑在受伤和衰老后如何修复和再生。
研究人员说,这是第一次在哺乳动物中证明了海马齿状回中的神经元在整个生命周期中都是由单个干细胞群生长发育而来的。与成熟神经元相比,新的、未成熟神经元在海马体中建立联系方面更加灵活,而这对于学习、记忆和调节情绪至关重要。
研究人员从胚胎期开始标记神经干细胞,并且从出生到成年持续追踪。结果发现在胚胎发育的第11.5天,小鼠齿状神经上皮中的Hopx+前体在原始齿状区产生增殖的Hopx+神经祖细胞,它们在发育过程中产生颗粒神经元,而不是其他神经元,然后在出生后早期转变为Hopx+静止的径向胶质神经祖细胞。通过RNA-seq和ATAC-seq分析表明,Hopx+胚胎、产后早期和成年齿状神经祖细胞具有共同的分子、表观遗传特征以及发育学特性。他们的研究揭示了带有前体标记的新神经干细胞在动物的一生中不断地制造神经元。
“这个过程在大脑中是独一无二的,”此研究合作者、神经科学教授、医学博士郭立明说,“在海马体中,这些细胞不停的进行复制,保持哺乳动物大脑的灵活性。”
这种能力被称为可塑性,即大脑在一生中具有形成新链接的能力,以补偿损伤和疾病,并根据环境做出调整。对此,郭教授做了一个有趣的比喻——海马体中新的神经元生长过程就像是在大脑主板的电路中添加新的电路单元。
研究小组透露,他们下一步的研究计划是在其他哺乳动物中寻找相同的神经干细胞,当然最重要的还是在人类的脑组织中找到相关的证据,预计将在遗体脑组织中展开研究,并研究这些神经干细胞群是如何调控的。
最后忍不住啰嗦一句,众所周知,海马体与阿尔兹海默症相关,看完这些研究小编不经怀疑,这些科学家们也看《都挺好》吧,而且是原著党,要不怎么蹭着热点都在最近集中发了呢?
End
参考资料:
2) Daniel A. Berg, Yijing Su, Dennisse Jimenez-Cyrus, Aneek Patel, Nancy Huang, David Morizet, Stephanie Lee, Reeti Shah, Francisca Rojas Ringeling, Rajan Jain, Jonathan A. Epstein, Qing-Feng Wu, Stefan Canzar, Guo-Li Ming, Hongjun Song, Allison M. Bond. A Common Embryonic Origin of Stem Cells Drives Developmental and Adult Neurogenesis. Cell, 2019; DOI: 10.1016/j.cell.2019.02.010
本文系生物探索原创,欢迎个人转发分享。其他任何媒体、网站如需转载,须在正文前注明来源生物探索。







