害羞的抗生素先锋 | 走近科学

青霉素对于今天的大众来说并不陌生,我们大多数人在日常生活中或多或少地都使用过青霉素类药物治疗细菌感染类疾病。现在大大小小的医院、诊所、药店里都备有各种类型和剂型的青霉素类药物,这类药物已经成为对抗细菌感染类疾病的一线用药。而在青霉素普及以前,哪怕是在20世纪四五十年代,一些现在看来不是十分严重的疾病,如肺炎、肺结核、猩红热、白喉、脑膜炎、淋病、梅毒等,仍然严重地威胁着人们的生命。由于没有针对性的药物,一旦感染上这些疾病,人们只能眼睁睁地看着病人一个个悲惨地死去。随着青霉素的发现与生产,相关药物结构与治疗效果研究的不断深入,人类对抗细菌性疾病的能力不断增强,许多原来的不治之症现在都能轻易地被青霉素类药物治愈。毋庸置疑,青霉素类药物推动世界现代医疗革命进入了一个全新的时期。

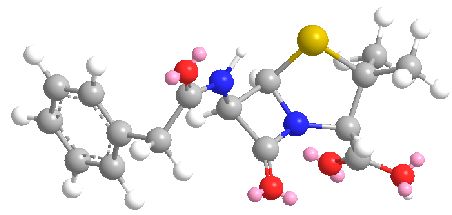
青霉素(英文名:benzylpenicillin/penicillin,音译为:盘尼西林,图1),性状:无定形白色粉末,溶解性:微溶于水,溶于甲醇、乙醇和苯。
图1 青霉素G三维分子结构式
青霉素的发现源于苏格兰微生物学家Alexander Fleming(图2)一次幸运的失误。早在20世纪20年代,Fleming就从眼泪中发现了具有杀菌作用的溶菌酶,这一对人体无害但却能杀灭有害细菌的物质,引起了Fleming对抗菌物质的强烈兴趣,但遗憾的是这一蛋白质杀菌物的杀菌能力不足以用于治疗疾病。为了寻找更为有力的杀菌剂,Fleming在实验室中培养了多种致病细菌,其中就包括致病性最高的细菌之一——金黄色葡萄球菌。1928年夏秋之交,Fleming在外出度假时忘记了把一个培养金黄色葡萄球菌的培养皿盖上盖子。3周后当他回到实验室,开始整理相关培养皿时,不由地注意到这个与空气意外接触过的金黄色葡萄球菌培养基中长出了一团青绿色的霉菌。出于他良好的观察习惯,Fleming并没有放过这一微生物培养过程中常见的误操作现象,通过仔细观察研究,他发现在这一丛霉菌的周围出现了一圈金黄色葡萄球菌停止生长的“抑菌圈”。进一步观察研究表明,当正常的金黄色葡萄球菌一旦接触到这种霉菌及其代谢产物时也会出现细胞溶解而死亡。这就意味着青霉菌的分泌物有明显的杀菌作用。通过接下来的鉴定,Fleming得知上述霉菌为点青霉菌(Penicillum notatum),于是将其产生的抑菌物质称为青霉素(penicillin)。为了获得这种神秘的抑菌物质,Fleming尝试了当时能够使用的各种分离方法,但在多年的努力之后,Fleming并未找到有效提纯青霉素的方法,而只能将点青霉菌菌株进行一代代地培养。1929年他发表了研究成果,但未引起科学界广泛的关注。
图2 Alexander Fleming
为了进一步推进这一十分有意义的研究成果,Fleming于20世纪30年代初将菌种提供给了牛津大学的Howard Walter Florey(图3)和Ernst Boris Chain(图4)团队,团队中还包括Norman Heatley,Edward Abraham,Arthur Duncan Gardner,M. Jennings,J. Orr-Ewing和G. Sanders等科学家。但是由于青霉素结构的高度不稳定性,直到40年代初,Chain和Florey才逐步优化了培养和分离青霉菌提取物的手段,获得了少量可以用于动物实验和临床实验的青霉素。一旦被投入人体或是特定动物的体内实验,青霉素马上就表现出了优异的杀菌作用。而且十分有意义的是,在有效杀灭致病细菌的同时,青霉素对大多数实验动物和人体均表现出了良好的安全性。和磺胺等其他化学药物相比较,青霉素的毒副作用要小得多。
图3 Howard Walter Florey
图4 Ernst Boris Chain
更让人惊喜的是,青霉素具有比磺胺类药物广的杀菌谱,这就意味着一种药物可以对抗多种致病细菌,对于战场外伤等复杂的细菌感染情况具有特别的疗效。此后一系列临床实验不断证实了青霉素对链球菌、白喉杆菌、金黄色葡萄球菌等多种细菌感染的治疗有效。这些令人振奋的结果出现于第二次世界大战的初期,战争时期的特殊情况进一步推动了对于抗菌药物的特殊需求。英国和美国政府都充分意识到了这一药物对于战争的重要意义,因而制定了包括限制发表青霉素相关研究成果等一系列的措施,加之战争阴云笼罩之下的英国科学家的研究环境不断恶化,两国政府为了更快地推进青霉素的研发与应用进程,开展了史称“青霉素计划”的宏大合作项目。Florey和Heatley来到了美国,与美国农业部的首席微生物学家Charles Thom展开了合作。为了尽快地实现青霉素的大规模生产,在当时的研究基础和物质条件下,有两条途径可以进行尝试。第一条是寻找青霉素产率更高的微生物菌种,优化发酵条件从而实现大规模的生产;第二条是尽快确定青霉素的化学结构,寻找合适的合成路线实现化学合成。历史最终证明,第一条路线首先解决了青霉素大规模生产的问题。
位于美国伊利诺伊州皮奥里亚的美国农业部北部地区研究实验室(Northern Regional Research Laboratory,USDA)是青霉素菌种筛选和发酵工程的研发中心。非常凑巧的是,高产率的青霉素发酵菌种(Penicillum chrysogenum)正是从该实验室的一名工作人员Mary Hunt所提供的一个发霉的甜瓜上找到的。以这一菌种为基础,在英、美两国的相关多家研究机构、包括默克(Merck)、辉瑞(Pfizer)、施贵宝(Squibb)和雅培(Abbott)等药物生产企业的合作之下,随后才发展出了以当地大量产出的玉米浆为主要原料的深罐(deep-tank)大规模生产发酵工艺,使大规模生产青霉素成为可能。在这些研究成果的推动下,美国多家制药企业于1942年开始对青霉素进行大批量生产。到了1944年6月6日的诺曼底登陆日,盟军指挥官Dwight Eisenhower将军已经拥有了近300剂青霉素的后备支持。整个1944年,青霉素的供应量已经足够治疗第二次世界大战期间所有参战的盟军士兵。由此作为起点,青霉素开始不断得到更加广泛、深入的应用,拯救了无数人的生命。因为这项伟大的发明,Fleming,Florey和Chain共同荣获了1945年度诺贝尔生理学或医学奖。
然而这一美好的结果却只是刚刚掀开了青霉素类化合物研究的大幕,一幕幕精彩好戏随之不断展开。首先是青霉素结构的确定。因为天然青霉素结构中包含酸性的羧基结构,可以和碱性物质生成盐类,所以随着青霉素分离、纯化方法的不断改进,首先获得的是青霉素的钠盐、钾盐以及相应的晶体。但是在20世纪三四十年代,化合物的结构鉴定虽然取得了长足的进步,但仍然不像现在这样可以依赖各种大型光谱仪器和数据库实现较为快速的结构鉴定,而只能通过大量烦琐的元素分析以及反应性质推断等传统方法获得相关的结构信息。在获得了青霉素盐类的纯净物后,英美两国的科学家都对这一物质的分子结构做出了大量的研究和推测。
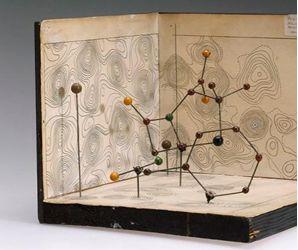
围绕青霉素的核心结构,当时顶尖的化学家们分为了两大派,一派以Robert Robinson(1947年诺贝尔化学奖得主)、John Cornforth(1975年诺贝尔化学奖得主)为主,他们认为青霉素的核心结构属于唑酮联噻唑环结构类型;另一派则以牛津团队中的Abraham、Chain以及美国Merck公司的化学家为主,他们认为青霉素的核心结构属于β-内酰胺并噻唑环结构类型。Robinson等化学家反对β-内酰胺结构的主要原因在于:β-内酰胺环是一个四元环,几何上要求环的内角都是90°,但是构成环的羰基碳原子正常的成键角度是120°,其他几个原子的正常成键角度都是109°,因此这个环的所有成环原子的键角都负向偏离了正常角度,相当于是被挤压着成环,具有明显的“张力”,所以不稳定。这一化学发展历史上著名的争议,最终被英国杰出的晶体化学家Dorothy Crowfoot Hodgkin(图5)于1945年通过X射线晶体衍射法确定了青霉素的三维晶体结构而解决(图6)。实验结果表明,青霉素的实际结构属于β-内酰胺并噻唑环的结构类型。回顾青霉素的整个发现过程,正是这一高活性的结构特点使青霉素在常见的分离条件下容易分解,因此,从1928年Fleming发现青霉素的活性开始直到20世纪40年代初,科学家才获得了足够进行生理活性研究和结构研究的纯青霉素。后续研究表明,青霉素对特定致病细菌的选择性抑制作用也来自于这一高活性的结构特点。
图5 Dorothy Crowfoot Hodgkin
图6 Hodgkin解析的青霉素晶体结构
而Hodgkin女士在复杂化合物结构解析方面的惊人工作远远不止青霉素。1955年她再次破解了一个看似无法破解的复杂分子——维生素B12的三维空间结构。基于这些漂亮的结构解析工作及她对X射线晶体衍射结构解析方法的巨大贡献,她于1964年成为了世界上第三位获得诺贝尔化学奖的女性;1965年,她又成为第二位获得英国功绩勋章的女性。更让人钦佩的是,Hodgkin女士在获得了世界范围内的广泛认可和尊敬后并没有停止她在科学高峰上的攀登。1969年她又成为世界上第一个完成对胰岛素三维结构分析的科学家。
在确定了青霉素的结构以后,通过化学方法合成这一分子成了青霉素研究的下一个重大目标。有意思的是,在分离、纯化和结构解析中带来过巨大困难的β-内酰胺结构再次成为青霉素全合成过程中的最大障碍。众多的化学家在合成青霉素的过程中都跌倒在形成β -内酰胺环这一难以逾越的最后一步上。大多数化学家经过一段时间的实验后,都停止了尝试。直到1957年,这一四元环的形成才被麻省理工学院的John Sheehan所完成,在此基础上他也成为世界上第一个完成青霉素类化合物全合成的科学家。正是因为Sheehan创造性地使用了一个刚发现的超强有机脱水剂DCC才使构成β-内酰胺环的氨基和羧基之间完成了脱水缩合反应形成四元环。为了完成青霉素的全合成,Sheehan领导他的课题组在青霉素的合成方法探索上寂寞地坚持了十余年。他们对DCC的使用也不是偶然的发现,而是在大量失败实验的基础上,针对反应特点进行目标性的试剂筛选和方案设计的必然结果。在这一合成方法的基础上,DCC这一试剂也开始逐渐在酯合成、蛋白质合成等领域崭露头角。在当今广泛应用的蛋白质固相合成方法中,DCC就起着不可替代的作用。随着全合成的完成,青霉素化学工作方面的障碍基本都被克服,青霉素的相关研究也随之进入了快速发展的时期。
1944年9月5日,中国第一批国产青霉素诞生,揭开了中国生产抗生素的历史。目前,我国的青霉素的年产量稳居世界首位。从20世纪九十年代初开始,我国青霉素盐的产量在世界总产量中的占比逐步从三分之一增加到目前的90%以上,青霉素工业盐产能已达10万吨/年。因此,如何改进我国青霉素生产的格局,从世界级的原料药物生产地转变为优势药品的生产基地是值得每一位相关药物研发工作者思考的问题。
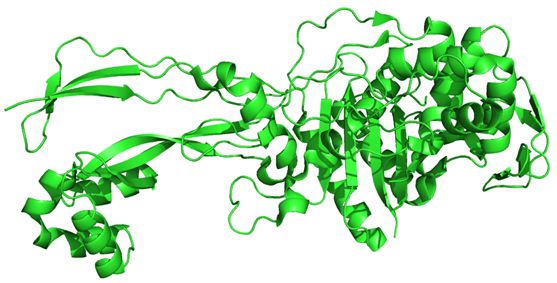
在与青霉素相关的众多研究结果中,最有意思的结论再次与青霉素的β-内酰胺环结构联系在一起。从前面的故事中我们已经了解到,青霉素和其他具有体内抑菌作用的药物比较起来,最突出的优势就是它对致病细菌具有强烈的抑制作用,而对人体却影响很小。这一神奇的生物种属作用差异其实来源于青霉素的作用机制。它之所以能够抑制人体内的致病细菌,是因为它可以不可逆地与细菌体内的青霉素结合蛋白(penicillin binding proteins,PBPs)(图7)结合。青霉素结合蛋白是细菌细胞壁合成过程中不可或缺的催化活性蛋白质,如转肽酶、羧肽酶、肽链内切酶等,它们在细菌生长过程中起着无法替代的重要作用。不同细菌PBPs种类及数量有很大差异,例如:金黄色葡萄球菌有4种PBPs,大肠杆菌则至少有7种。
图7 绿脓杆菌(Pseudomonasaeruginosa)的青霉素结合蛋白(PBPs)
细菌细胞壁具有保护和维持细菌正常形态和隔离细胞内外环境的功能,主要成分是胞壁黏肽(mucopeptide, 也称肽聚糖,peptidoglycan)。它由两条氨基酰化的线型多糖链(N-乙酰葡萄糖胺,N-acetylglucosamine, NAG;N-乙酰胞壁酸,N-acetylmuramic acid, NAM)通过肽链交联而成。细菌细胞壁的生物合成可分为3个阶段:①胞质内黏肽前体的形成。②胞质膜上为乙酰胞壁五肽与乙酰葡萄糖胺连接。③在细胞膜外,通过转肽作用完成交叉连接过程。
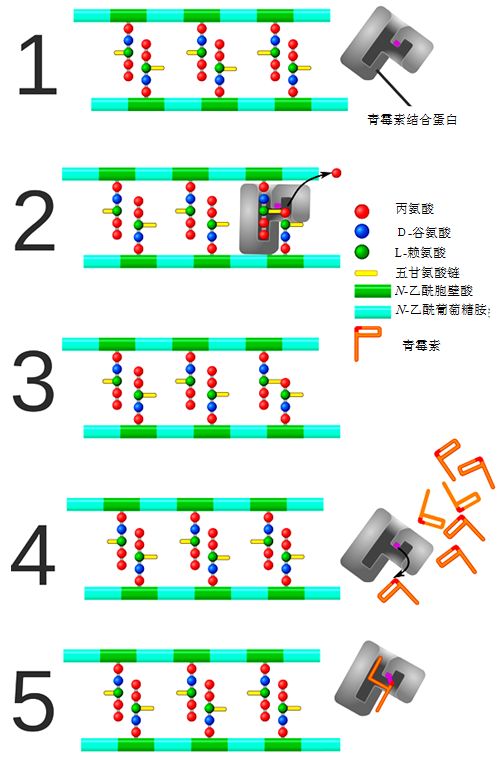
青霉素结合蛋白是合成细菌细胞壁表面结构肽聚糖(peptidoglycan)的关键催化剂,一旦青霉素结合蛋白的活性中心与青霉素结合就失去了催化肽聚糖合成的活性,就会使细胞壁合成终止,从而导致细菌的死亡(图8)。
图8 PBPs在细菌细胞壁生成交联中发挥作用及其与青霉素等结合产生永久抑制的作用1~3为转肽酶正常作用时对肽聚糖的催化联结作用;4~5则是青霉素抑制转肽酶后,肽聚糖片段无法联结的情况
青霉素能与青霉素结合蛋白形成不可逆结合主要有两个原因,第一:青霉素的整个分子结构从空间形态上来说,与转肽酶正常的结合对象——肽聚糖的末端二肽D-丙氨酰-D-丙氨酸具有足够的相似度,可以进入酶的活性中心;第二:β-内酰胺四元环的巨大张力使其容易接受转肽酶中羟基的进攻而发生不可逆的酰化反应而使酶失活。也就是说青霉素β-内酰胺环的高度反应活性体现在与酶活性中心中的羟基的不可逆酰化反应中;相比较而言,该活性中心与糖蛋白的肽链反应则是活性适中,表现为可逆反应,可以不断地催化细胞壁的合成。一旦转肽作用不能进行,肽聚糖交叉连接就会受阻,致使细胞壁缺损,失去保护屏障。由于菌体内渗透压高,环境中水分就会不断渗入,使细胞肿胀、变形,在自溶酶激活影响下,细菌破裂溶解而死亡。
显而易见,使用青霉素的优点在于:与细菌相比,人与动物的细胞就没有细胞壁这一结构,也就是说没有肽聚糖结构。人体细胞的最外层是磷脂双分子细胞膜,所以人与动物的细胞中就没有细胞壁合成相关的转肽酶等青霉素结合蛋白,自然也就不会被青霉素所毒害。
青霉素因其高效、低毒的特点,被广泛应用于临床治疗。经过数十年时间的完善,青霉素针剂和口服剂已经能够根据不同需要治疗肺炎、肺结核、脑膜炎、心内膜炎、白喉、炭疽等细菌感染性疾病。继它之后,链霉素、氯霉素、土霉素、四环素等一大批针对性各不相同的抗生素不断被发现并生产,极大地增强了人类治疗细菌性疾病的能力。
常言道“道高一尺,魔高一丈”,一部分病菌的抗药性也随着抗生素的使用而不断进化、变异和增强。对青霉素而言,抗药性的本质就是细菌通过变异作用在细胞内部产生出了对青霉素类化合物具有破坏作用的β-内酰胺水解酶。这种酶在青霉素接触转肽酶之前就能把它的β-内酰胺环结构水解开环,这样分解掉的青霉素就不再会对细菌产生毒害作用,从而产生抗药性。细菌一旦产生了抗药性,其危害自然是不言而喻的。
针对这一严重威胁人类健康的细菌变异作用,我们能够采用的手段并不是十分多,下面简单地介绍几种思路。
第一种思路是改变药物分子的结构。从上面的青霉素结构研究结果中,我们已经了解到:青霉素的分子由二部分组成,一部分是由四元β-内酰胺环与五元噻唑环并在一起形成的“母核”——青霉胺,它是青霉素抗菌的活性中心,一旦四元β-内酰胺环被破坏,青霉素就失去抗菌活性;另一部分则是与青霉胺相连的侧链。显而易见,针对化合物结构的改造也只能从这两部分结构入手。就侧链改造而言:由于青霉素的侧链与母核青霉胺之间是通过酰胺键连接的,因此可以利用已经十分成熟的青霉素生产工艺,大量生产青霉素,然后通过酶水解其固有侧链来进行改造。研究发现,改变侧链结构,一方面可以使母核的结构更加稳定,增强药物的耐酸性,使之可以口服,增加对耐药性致病菌的破坏和打击能力;另一方面,还可以扩大青霉素的抗菌谱,并在一定程度上降低过敏性。这类侧链经过改造的青霉素药物被称为半合成青霉素,现在已经广泛用于临床。例如,很多人都使用过的安必仙(氨苄青霉素)和阿莫西林(羟氨苄青霉素)就是其中的典型代表。这类青霉素就具有一定耐抗药性,效果较青霉素好,可以作为口服剂型使用。
过去病人打一针普通青霉素需要80~100万单位,现在使用半合成青霉素,如氨苄青霉素、羟氨苄青霉素,只需要20万单位就可以达到同样的治疗效果。化合物甲氧西林(methicillin)值得额外地介绍一下,这个化合物虽然具有比其他青霉素更好的抗耐药性,但是由于它引起间质性肾病的比例高于其他青霉素类药物,而且已经有了更好的替代药物,现在已经基本退出了临床使用。因此被用作衡量青霉素类药物抗药性的标准物质,即对甲氧西林有抗药性的致病细菌就可以认为所有青霉素类抗菌药物都对其无效。其中最为有名的抗药性致病菌是耐甲氧西林金黄色葡萄球菌(MERSA),这类细菌感染就只能使用其他类型的抗生素进行治疗,例如利奈唑胺(linezolid)和万古霉素(vancomycin),而且治愈率和预后不是十分理想。
相比较而言,针对母核的结构改造不如侧链改造那么方便,主要就是因为母核中的β -内酰胺结构不能耐受剧烈的反应条件。因此更为实际的途径就是寻找其他微生物发酵来源以获得不同的母核结构。就具有与青霉素类似的β-内酰胺结构的化合物而言,最有代表性的就是从冠头孢菌(Cephalosporium acremonium)中培养得到的天然头孢菌素C(cephalosporinC),以此化合物为基础,通过类似于青霉素的研发方法,发展出了几乎和青霉素同等重要的头孢类抗生素。
第二种思路是从抗药性产生的源头开始防止抗药性的产生。从前面的讨论可以看出:抗药性的产生是由于致病细菌针对抗生素的结构弱点,产生相应的生物化学破坏机制而形成的药物失效作用。理论上说,只要长期使用某种抗生素治疗细菌感染就有可能产生相应的抗药性。目前,形势逐日严重的抗药性感染,很大程度上都要归因于青霉素类抗生素的滥用。很多人都有得了类似于感冒、咳嗽的小毛病就懒得上医院,而是去药店随便买点安必仙、阿莫西林之类的药物吃上几天,如果症状稍有减轻就停药,症状加重后再次服药的经历。殊不知,这样不规范地使用抗生素,特别容易产生抗药性,这也是社会上大范围产生抗生素类药物抗药性的重要根源之一。因此,合理、规范地使用抗生素是防止产生抗药性的根本。如果觉得病情严重,需要使用抗生素,那就应该在执业医师的指导下,按时、按量、足量的使用抗生素,才能达到较好的治疗作用,防止抗药性的出现。
作为社会的一分子,我们既有享受社会医疗发展带来的各种便利的权利,也有为社会节约资源防止不良现象产生的义务。
本文摘编自《奥妙化学》编委会编《奥妙化学》一书,内容有删节。标题为编者所加。
《奥妙化学》
《奥妙化学》编委会编
北京: 科学出版社,2018.6
ISBN 978-7-03-057346-9
责任编辑:张 析
云南大学化学科学与工程学院•药学院和自然资源药物化学教育部重点实验室的多位一线教师在长期教学科研实践的基础上,汲取国内外同类教材和书籍的特点,以“有趣的化学,有用的分子”为主线,从化学分子的角度,感悟化学的真谛,并编写成一本综合性的化学通识素质教育教材。全书主要包括天然产物、药物、食品、新能源、高分子材料、毒物、日用保健品和化学品等领域的代表分子共七部分内容,49个分子的相关知识,旨在通过对社会发展和人们生活产生重要影响的分子的精彩介绍,以纵横捭阖的风格,揭开化学的神秘面纱,展现化学知识、化学的奥妙和魅力。
本书可供化学爱好者和其他专业人员作为扩充化学知识阅读,也可供从事化学研究和相关工作的人员扩充专业背景知识参考。
(本期编辑:王芳)
一起阅读科学!
科学出版社│微信ID:sciencepress-cspm
专业品质 学术价值
原创好读 科学品味
更多好素材,期待你的来稿
点击“阅读原文”可购买本书