会议名称:
创建儿童癌症精准医疗体系
在过去的十年中,基于基因组学的研究成果揭示了儿童癌症的分子基础。这些机制与在成人癌症基因组中的发现形成了鲜明的对比,并在基因组学诊断和罕见病护理中形成了一系列的挑战。目前很多正在进行的工作包括针对儿童病例中的复发或难治病例,应用基因组学技术和先进的分析方法进行研究和诊断。本次报告主要针对其中遇到的困难,现行方法,成功和失败的经验进行总结,并对未来的趋势进行展望。
Frontiers in Cancer Research, October 2018, Heidelberg, Germany
会议简介:
在过去的几十年中,随着现代社会面临重大挑战,人们预期寿命的延长和生活方式的根本变化导致癌症发病率不断增加。以优秀的基础研究的持续交流作为推动力,跨学科研究方法揭示了癌症发展和进展的机制,实现从实验室到病床边(from bench to bedside) 的创新转化。本次Frontiers in Cancer Research会议概述了当前跨学科癌症研究中最激动人心的领域,国际知名的专家们从6 个方面介绍他们最近的成果:
干细胞和癌症
癌症分子机制
系统生物学
肿瘤免疫学
转化医学研究
预防癌症
本次会议旨在为杰出的科学家提供一个论坛,尤其是女性科学家,意在促进学术研究各方面的性别平等来增强科学卓越性。约有80%的受邀来宾是女性。
主讲人:
Elaine Mardis教授,俄亥俄州哥伦布市全国儿童医院(Nationwide Children’s Hospital, Columbus, OH, USA),基因组医学研究所联合执行主任,现任美国癌症研究学会(AACR)主席
基于亚马逊云服务的基因组分析(AWS-based genome analysis)
目前Nationwide Children’s Hospital的分子诊断平台(GenomeNext’s Platform)使用Amazon Web Service(AWS)云服务器,可每天分析1000个基因组。其中80%的病人样本来自于冰冻组织(fresh frozen samples),20%的病人样本来源于福尔马林固定的石蜡包埋组织(FFPE samples)。在病人签署同意书之后进行全基因组(WGS, 深度60x)、全外显子组(WES, 深度250x)的肿瘤和对照正常组织测序和肿瘤组织的RNA测序(RNAseq); 还有一部分病例在病患孩子家长同意之后会对家长或者其他家庭成员进行采血后测序。这种体系可以充分涵盖体细胞突变及可遗传突变(somatic mutations & germline mutations)。
二代测序(NGS)分析的临床应用
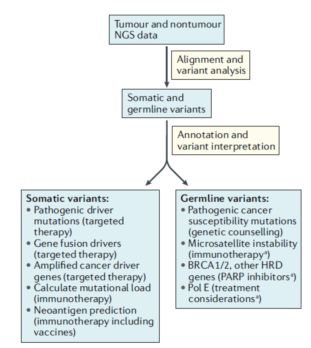
通过肿瘤细胞和正常体细胞的对比,建立变异分析检测标准流程(图1)。和用药相关的体细胞突变分析主要包括有靶向药针对的致病驱动基因、融合基因、扩增基因,免疫疗法相关的突变量计算和新抗原预测。而可遗传突变主要针对与癌症相关性高的多态性位点(SNP),微卫星序列(microsatellite),和PARP抑制剂相关的突变,如:BRCA1/2, 同源DNA重组修复缺陷(HRD),DNA聚合酶ε (如:Pol E基因突变的患者肠癌复发的机率显着减少)。其他分析包括临床意义不明确的突变、扩增、删除、小片段插入以及缺失(Indel)、染色体结构变化、肿瘤内异质性(intratumoral heterogeneity)等等。
图1. 基因组测序的临床应用流程。引自Berger MF and Mardis ER. The emerging clinical relevance of genomics in cancer medicine. Nat.Rev. Clinical Oncology,15:353–365 (2018)
树屋儿童癌症公共数据(The Treehouse Childhood Cancer Initiative)
加州大学圣克鲁兹分校基因组学研究所(UCSC Genomics Institute)的树屋儿童癌症倡议使用共享数据分析儿童肿瘤和成人肿瘤(网站链接见后)。该数据库共收集了来自11000多个肿瘤样本的数据,并可供所有研究人员免费下载和进行可视化。 该基因表达数据与患者隐私保护的临床数据一起可用,包括年龄,性别和疾病类型等。最近发布的数据版本8 (发布于2018年7月)包含11427个poly-A 筛选-核糖体去除的RNA样本的RNAseq数据及临床数据,以器官系统排序,相同种类的肿瘤可以进行比较,结果包括差异基因表达,信号通路富集,基因融合等。其中融合基因全部由PCR二次确认,并包含表达量排序。
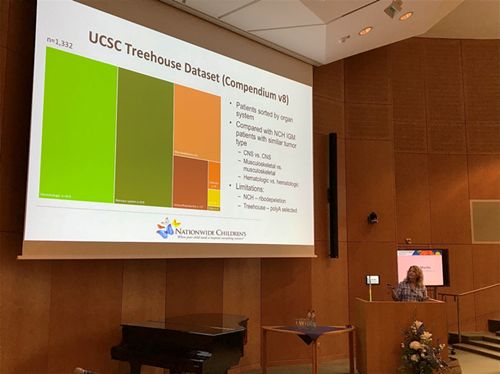
病人1患有FGFR1:TACC1融合基因的胶质母细胞瘤(glioblastoma) ,后应用FGFR抑制剂治疗;
病人2患有MET-RBPMSLP融合基因的梭形细胞肉瘤 (spindle cell sarcoma), 后应用MET抑制剂治疗;
病人3青少年复发性脑瘤患者(relapsed childhood CNS tumor),家族性遗传NF-1基因突变,基因组改变复杂,经过信号通路富集分析和癌症免疫微环境分析发现该病人巨噬细胞增多,PD1表达较其他glioblastoma病人增高,酪氨酸激酶表达量增高等,后决定将其纳入anti-PD1和MEK抑制剂联合应用的成人临床试验。
临床应用NGS的挑战
二代测序在临床上应用的挑战大体可以从测序技术本身、病人样本、数据分析和临床解释几个方面来说。随着测序数据的复杂化和方法的多样化,对测序结果的临床意义解释成为这个领域中最大的难点。一种癌症中有哪些驱动基因、相同突变在不同癌症中意义不同、什么样的变化可以算作可治疗的突变(targetable genomic alterations)等等很多问题仍然有待基础科研去解决。病人样本的采集方式和对应的分析方法有很多种,哪种既能准确地反映不同时期的肿瘤特性,又能简单易行。病人的样本通常是稀缺资源,数量非常有限,生物检材在日常处理中不容易保证样品处理的一致性,极易降解和污染,这些都会直接影响测序数据的结果。数据分析方面,由于不同种类的改变需要不同的算法来计算,检测的灵敏度会受到测序深度的影响,因此NGS分子诊断通常需要保证高深度测序和一定广度的覆盖范围。另外由于全基因组数据量巨大,分析时间往往较长,不足以满足临床快速诊断的需要,优化出高效且精准的标准分析流程成为必须。在当前条件下即便有很大的云计算服务器,全基因组(WGS)和全外显子组(WES)数据依然需要较长时间和大量人力去分析解读,不同平台和工作流程之间产生结果的可重复性仍需提高。还有大数据产出之后的储存和访问等等,都是分子诊断中的挑战。
数据和软件共享(Data and software sharing):
由于儿童癌症相对罕见,所以共享数据和临床资料对了解疾病十分重要。整合多平台数据,从聚焦单一驱动基因到信号通路,可以更好地了解每个病人的癌症基因组。建立更多方便下载的整合工具包和基于网络的数据库,增加专职基因数据分析人员和提高病人数据访问权限,将构成未来的主要工作内容。
结论:
1) 虽然面临诸多挑战,针对儿童癌症的临床基因组学检验依然可以为治疗计划,诊断和预告提供重要的临床证据。
2) 结合DNA和RNA的数据可以很有效地提供癌症驱动基因(driver genes),新抗原(neoantigens)和免疫微环境(immune microenvironment)的信息,但是需要评估各类治疗方案的临床获益(clinical benefit)和分子水平变化上的关系。
3) 分享数据和软件,包括分享治疗信息和临床结果对儿童癌症来说至关重要,甚至只发表一小部分针对和治疗相关的分子特性的探索性研究都十分重要。
4) 对患者群体的教育会促进这些诊断和检测方法的信息透明化, 但是需要更多创新方法和开源数据库的支持。
旅德华人医师学者协会(SCDSG) 简介:
旅德华人医师学者协会(微信公众号”龙一族”)是以医学及生物学博士为主体,以学术交流为主要目的的非盈利团体。协会于2016年正式成立,目前包括在德会员和归国会员230余人,非正式会员近100人。在德会员主要来自海德堡大学及附属医院和德国癌症研究中心(DKFZ),国内部成员主要就职于全国各大城市的大型医院各个科室及科研院所。协会致力于构建中德医学、生物及相关领域的学术交流合作平台,普及医学科学知识,推动生命科学创新,服务留德及归国华人。联系方式:scdsg.heidelberg@gmail.com
更多信息请访问:
Nationwide Children’s Hospital:https://www.nationwidechildrens.org/
The Treehouse childhood cancer initiative: https://treehousegenomics.soe.ucsc.edu/
41本肿瘤患者指南丛书
点击下方图片即可免费阅读
70个肿瘤相关临床试验招募患者
点击下方图片或识别图片二维码即可查看详情