有“芙”共享丨生命之托,有“氟”所依
病例分享:张明坤 空军军医大学附属西京医院
病例指导:张聚良 空军军医大学附属西京医院
点评专家:刘红 天津医科大学附属肿瘤医院

术前新辅助治疗是指通过手术前的化疗、内分泌治疗等手段,使乳腺癌患者能够快速达到缩瘤、降期、保腋窝的目的,为进一步的手术创造机会和条件。术前新辅助内分泌治疗用于HER2阴性、激素受体阳性的乳腺癌患者,已逐渐进入公众视野。对于因合并其他系统疾病而不能耐受化疗的激素受体阳性老年女性患者,持续更久的新辅助内分泌治疗也是可选策略。
陕西省抗癌协会青年专业委员会委员
2011年7月本科毕业于哈尔滨医科大学临床医学系,2014年7月硕士毕业于哈尔滨医科大学外科学专业,毕业后于空军军医大学附属西京医院甲乳血管外科工作至今。
参与省级自然基金课题两项,国内外杂志发表论文5篇,参编著作1部。
中华医学会肿瘤学分会乳腺学组青年委员
中国医师协会乳腺疾病专业委员会委员
中国医药教育协会乳腺专业委员会委员
中国研究型医院学会乳腺疾病专业委员会委员
陕西省抗癌协会青年委员会副主任委员
陕西省保健协会肿瘤防治专业委员会常委
陕西省保健协会乳腺癌MDT学组副组长
基本情况
患者女性,65岁,已绝经。2018年5月主因“发现右乳腺肿物1月余”就诊于我院。既往否认慢性病、传染病、家族病史。
现病史及穿刺
患者入院后查体:双侧乳房对称,双侧乳头无内陷,无异常分泌物,表面皮肤无红肿,右侧乳腺外下象限可触及一3cm×3cm大小包块(约7点方向,距乳头约5cm),无压痛,质地硬,边界不清,活动度差,与胸壁粘连固定,右侧腋窝可触及肿大淋巴结,左侧乳腺及左腋下未触及异常。相关影像学和实验室检查示:①乳腺超声:右侧乳腺8点方向距乳头约5cm可见大小约2.9cm×1.6cm×2.5cm低回声,边缘不清,形态不规则,内可见丰富血流信号,BI-RADS 4类。右侧腋窝可见肿大淋巴结,皮髓质界限不清。②乳腺MRI(图1)示:右乳外下象限胸壁前方见一个不规则团块状稍长T2信号,周围环绕片状长T2信号,TIC呈流出型,大小约2.6 cm×2.6 cm×2.9cm,BI-RADS 4类,肿块后缘与右侧胸壁界限不清。③超声心动示:左房、左室大,左室舒张、收缩功能减低,二尖瓣返流(中-重度),双平面法估测EF:32%。④脑利钠肽(brain natriuretic peptide,BNP)2132pg/L。④余胸部CT、腹部B超、骨扫描、血肿瘤标志物等检查未见明显异常。
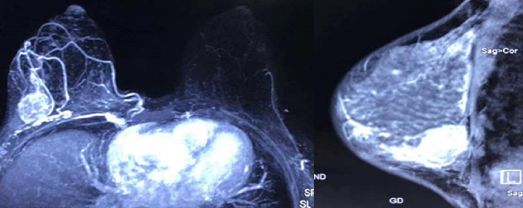
图1 乳腺MRI(入院后)
后排除明显禁忌,行超声引导下右乳腺肿物穿刺活检术,病理示:右侧乳腺浸润性癌(invasive ductal carcinoma,IDC),非特殊类型,SBR Ⅱ级。右侧腋窝纤维组织内查见癌组织。免疫组化(immunohistochemistry,IHC)示:ER(3+,85%),PR(3+,90%),HER-2(-),Ki-67(约30%)。结合患者病史及病理结果,目前诊断明确为:右侧乳腺浸润性癌( cT4N1M0 ⅢB期,分子分型Luminal B型)。
治疗及手术
结合患者疾病的病理类型及患者本身体质状况不佳,与患者及家属反复商议,于2018年6月起采用术前新辅助内分泌治疗方案,具体方法为:氟维司群 500mg 肌注每28天同时联合阿那曲唑口服1mg qd。在新辅助内分泌治疗期间患者就诊于我院心血管内科积极对症处理以改善心脏功能,并行心脏瓣膜置换术。2018年12月完成内分泌治疗,综合疗效评估为完全缓解(complete response,CR,图2)。
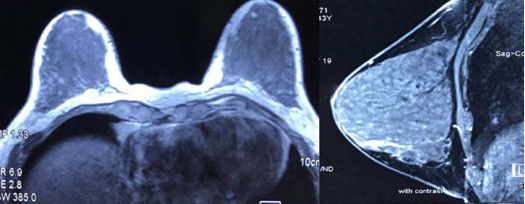
图2 新辅助内分泌治疗后
患者于2019年1月行右乳腺癌改良根治术(breast cancer modified radical mastectomy),手术过程顺利,术后病理示:新辅助治疗后,左侧乳腺导管及纤维组织增生,部分导管扩张,局部泡沫细胞聚集,可见钙化,同侧腋窝淋巴结(0/17)未查见转移癌。结合术后病理结果,认为患者术前内分泌治疗已达病理学完全缓解(pathological complete remission,pCR)。后患者于2019年2月起口服阿那曲唑至今,期间定期复查未见明显转移与复发征象。
总结
患者2018年5月主因“发现右乳肿物1月余”就诊,右乳肿物穿刺示:IDC,非特殊类型,SBR Ⅱ级。右腋窝查见癌组织。IHC示:ER(3+,85%),PR(3+,90%),HER-2(-),Ki-67(约30%)。诊断明确为:右侧乳腺浸润性癌( cT4N1M0 ⅢB期,分子分型Luminal B型)。因患者机体耐受欠佳,给予术前氟维司群+阿那曲唑内分泌治疗6月,综合疗效为CR。后行右乳腺癌改良根治术病理示:新辅助化疗后,左侧乳腺导管及纤维组织增生,同侧腋窝淋巴结(0/17)未查见转移癌,达pCR。后于2019年2月起口服阿那曲唑至今。
天津医科大学附属肿瘤医院乳腺中心
先后师从我国著名肿瘤学专家李树玲教授和郝希山院士,获得肿瘤学硕士和博士学位
分别于1999年和2007年公派赴日本久留米大学和美国M.D.Anderson Cancer Center进修学习
中国抗癌协会乳腺癌专业委员会常委兼青年委员会主任委员
中国抗癌协会学术部副部长
中国医师协会外科医师分会乳腺外科医师委员会常委
北京乳腺疾病防治学会外科专委会常委
专家点评
患者老年女性,已绝经。分析患者的既往内分泌治疗和手术病理等情况,结合美国国立综合癌症网络指南(national comprehensive cancer network guidelines,NCCN)2019 V1乳腺癌指南和《中国临床肿瘤学会(CSCO)乳腺癌诊疗指南》2019 V1版分析:
HR+乳腺癌内分泌治疗,不可或缺
临床上常常根据乳腺癌的患者病理组织切片中雌激素受体(estrogen receptor,ER)、孕激素受体(progesterone receptor,PR)和人表皮生长因子受体(human epidermal growth factor receptor,HER2)基因表达及蛋白水平将乳腺癌大致分成四类:Luminal A型, Luminal B型、HER2+乳腺癌和三阴性乳腺癌(triple negative breast cancer,TNBC)。针对不同的分子分型,开展相对个体化的手术、化疗、靶向治疗、放疗、内分泌治疗等多种治疗手段。
对于激素受体阳性的乳腺癌而言,由于乳腺癌细胞的生长部分依赖于雌激素的存在,通过降低雌激素的水平或者干扰雌激素与受体的结合可以达到治疗目的。第三代芳香化酶抑制剂(aromatase inhibitor,AI)如阿那曲唑、来曲唑、依西美坦等,结构上与该酶的自然底物雄烯二酮相似,为芳香化酶的伪底物,可通过与该酶的活性位点结合而使其失活,从而明显降低绝经后妇女血液循环中雌激素水平。而氟维司群(fulvestrant)是一类雌激素受体下调剂,一方面可以与雌激素受体竞争性结合,亲和力与雌二醇相似,另一方面还可以抑制雌激素的与受体结合并激发受体发生形态改变,降低ER水平。相较于化疗,内分泌治疗还具有安全性高,易于维持等特点,在辅助及晚期乳腺癌的治疗中发挥重要作用,而在新辅助领域,近年也逐渐引起大家关注。
HR+乳腺癌新辅助内分泌治疗,获益良多
既往一些小规模临床试验如GEICAM/2006-03、NEOCENT和回顾性研究表明,接受新辅助化疗和新辅助内分泌治疗(neoadjuvant endocrine therapy,NET)的ER阳性、HER-2阴性乳腺癌患者有相似的局部控制率和总生存期(overall survival,OS),化疗能够带来较高的pCR率,而内分泌治疗的优势在于提高了保乳率[1~4]。2015年St Gallen专家共识认为相比新辅助化疗,绝经后Luminal A型患者更适宜行新辅助内分泌治疗,治疗持续时间建议为4~8个月或达到最大缓解[5]。
本例患者属于局部晚期,具备新辅助化疗的指征,但相关检查提示患者心功能及体质状况较差,不能耐受短期高强度化疗带来的毒副作用,特别是心脏毒性。山重水复疑无路,患者穿刺提示为Luminal B型乳腺癌,这就为她提供了另一种可能——新辅助内分泌治疗,适宜人群主要是需要术前治疗而又无法适应化疗的、暂时不可手术或无需即刻手术的激素依赖型患者。通过6个月的新辅助内分泌治疗,患者的病灶得到了良好的控制,术后病理提示通过NET达到了病理完全缓解(pCR),与术前新辅助化疗所追求的目的一致。
对于新辅助内分泌治疗的早期疗效判定仍处于探索阶段,Ki67的下降水平、PEPI评分等均在不同的临床试验中用于疗效评估,显示出一定的价值,但由于往往需要二次穿刺,不同实验室的检测标准并不统一等,限制了这些指标的应用,有待进一步证实。新辅助内分泌的时长尚不明确,现有的试验证据大多支持3~6个月,个别的临床试验中时长可达1年。由于新辅助内分泌治疗不良反应较小,在肿瘤持续缓解的情况下,延长内分泌治疗的时间而达到肿瘤最大缓解可能不失为一个良策。但延长内分泌治疗的时间有可能增加疾病进展的风险,因此内分泌治疗期间需要进行严密随访,并在适当的时机进行手术干预[6]。
氟维司群+AI新辅助强强联合,值得期待
本例患者新辅助内分泌治疗方案选择了氟维司群联合AI,是基于新辅助治疗更适合强化这一理念,也确实取到了良好的治疗效果。一项晚期的随机对照临床研究SWOG S0226[7]结果显示,在激素受体阳性的349例LR/MBC患者中氟维司群联合阿那曲唑延长中位PFS(联合治疗组为15.0个月,阿那曲唑单药组为13.5个月;HR=0.80,P=0.007)。两组严重毒性反应的发生率相似,几乎所有患者都能接受治疗。此外,中位随访7年的OS结果表明接受联合治疗的患者OS延长,阿那曲唑单药组的中位OS为42个月,联合治疗组的中位OS为49.8个月。生存曲线存在显著差异 (HR=0.83;95%CI,0.69~0.98;P=0.03)。研究结果表明氟维司群和AI阿那曲唑的组合作为绝经后激素受体阳性LR/MBC患者的一线内分泌治疗,对比阿那曲唑单药,能够显著延长PFS和OS,且前期未经内分泌治疗的患者更应选择氟维司群和阿那曲唑的联合方案。当然,还有一些类似的研究并不支持这一结论,如FACT及SoFEA研究中,氟维司群与AI的联用并未显示出优势。因此,如何选择合适的新辅助内分泌治疗方案有待证实,一些临床试验显示,CDK4/6的抑制剂与AI或氟维司群的联用可能具有更好的缓解率,期待这些临床试验的生存数据带给我们更多地选择。
总而言之,NET 用于激素受体阳性的术前新辅助治疗的乳腺癌的方法 已逐渐进入公众视野,特别是对于因合并其他系统疾病而不能耐受短期高强度化疗的激素受体阳性老年女性患者,持续更久的NET 是较为优选的可选策略。尽管NET 具有能够降低TNM 分期、降低手术难度并减少复发风险等上述优点,但仍有许多问题有待回答,如:NET 的最适宜人群、最佳疗程、最佳药物选择及耐药等一系列问题,期待相关循证医学证据的的支持和完善。该病例基于指南规范,又结合临床现实合理治疗的成功病例,给患者带来临床获益,对我们很有启发,值得借鉴和学习。
[1] Semiglazov V F , Semiglazov V V , Dashyan G A , et al. Phase 2 randomized trial of primary endocrine therapy versus chemotherapy in postmenopausal patients with estrogen receptor-positive breast cancer[J]. Cancer, 2007, 110(2):244-254.
[2] Alba E , Calvo L , Albanell J , et al. Chemotherapy (CT) and hormonotherapy (HT) as neoadjuvant treatment in luminal breast cancer patients: results from the GEICAM/2006-03, a multicenter, randomized, phase-II study[J]. Annals of Oncology, 2012, 23(12):3069-3074.
[3] Palmieri C,Cleator S,Kilburn L S et al. NEOCENT: a randomised feasibility and translational study comparing neoadjuvant endocrine therapy with chemotherapy in ER-rich postmenopausal primary breast cancer.[J] .Breast Cancer Res. Treat., 2014, 148: 581-90.
[4] Wright J L , Saigal K , Reis I M , et al. Locoregional and Overall Recurrence After Neaodjuvant Endocrine Therapy Versus Chemotherapy in Postmenopausal Women With Estrogen Receptor+ HER2- Breast Cancer.[J]. American Journal of Clinical Oncology, 2015, 330(2):398–411.
[5] Goldhirsch A, Ingle J N, Gelber R D, et al. Thresholds for therapies: highlights of the St Gallen International Expert Consensus on the Primary Therapy of Early Breast Cancer 2009[J]. Annals of Oncology, 2009, 20(8):1319-1329.
[6] Carpenter R , Doughty J C , Cordiner C , et al. Optimum duration of neoadjuvant letrozole to permit breast conserving surgery[J]. Breast Cancer Research and Treatment, 2014, 144(3):569-576.
[7] Mehta RS, Barlow WE, Albain KS, et al. Overall Survival with Fulvestrant plus Anastrozole in Metastatic Breast Cancer[J]. N Engl J Med. 2019;380(13):1226-1234.