Cell:一个新的“免疫检查点”,有望与癌症疫苗联合抗癌
免疫检查点抑制剂是癌症免疫治疗的热门方向,通过阻断T细胞表面的PD-1、CTLA-4等“刹车分子”与配体结合,从而消除其对T细胞活性的抑制,最终释放免疫系统消灭肿瘤的能力。
近日,《Cell》期刊上最新一篇文章,揭示了免疫细胞上一个新的“检查点”,有望应用于抗癌治疗中。改善治疗性癌症疫苗的临床反应。
DOI:https://doi.org/10.1016/j.cell.2018.10.028
在最新的研究中,来自于范德堡大学的科学家们着重研究了自然杀伤(NK)细胞,试图寻找在肿瘤发生过程中,抑制这些天然免疫细胞不能正常运作的关键蛋白。
他们发现,NKG2A蛋白是唯一的抑制性受体,在头颈部肿瘤中的NK细胞上表达增加。然而,在血液中循环的NK细胞同样也表达NKG2A蛋白,而且只比肿瘤中NK细胞的表达量略低。
很显然,对于NK细胞而言,NKG2A蛋白的“刹车效果”并不明显。
当他们进一步观察CD8+T细胞(杀伤性T细胞)时,意外发现了NKG2A的“跳跃”。“因为NKG2A通常与NK细胞有关,”文章作者Michael Korrer解释道,“但是最新研究却显示,在头颈部肿瘤样本中,CD8+T细胞表面NKG2A表达显著,且在血液中不表达。”
杀伤性T细胞同样可以消灭入侵病毒感染的细胞以及癌细胞,但是它们首先必须通过识别特异性抗原来激活。随后,Michael Korrer和团队发现了NKG2A的“配体”——肿瘤细胞表面表达的HLA-E蛋白。他们证实,NKG2A表达会抑制CD8+T细胞的活性。这也是为什么头颈部肿瘤NKG2A表达会与较差的临床响应有关了。
Young J. Kim, MD, PhD, left, Michael Korrer, PhD, and colleagues are studying a potential new cancer immunotherapy option. Credit: Anne Rayner
于是,Michael Korrer团队与荷兰莱顿大学医学中心的Thorbald van Hall实验室合作,对HLA-E进行了深入研究,并与法国Marseille的一家生物医药公司Innate Pharma建立合作。该公司已经研发了一种NKG2A抗体,被称为monalizumab。
基于小鼠肿瘤模型,科学家们发现,单独使用monalizumab抑制NKG2A的治疗效果较差。但是,将monalizumab与旨在刺激抗肿瘤免疫应答的癌症疫苗相结合,可以减少肿瘤生长并延长无进展生存时间。
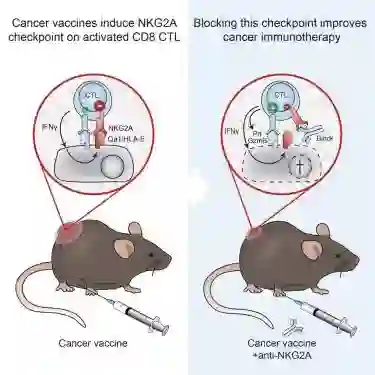
“结果似乎显示,NKG2A靶向治疗必须与引起肿瘤炎症的因素相结合,例如癌症疫苗。” Michael Korrer表示道。这是为什么呢?研究显示,癌症疫苗可以刺激NKG2A的表达。这时候,通过NKG2A抗体阻断NKG2A与HLA-E的结合可以提供癌症免疫疗法。
图片来源:Cell
在一项单独的研究中,Innate Pharma的研究人员报告了一项II期临床试验的中期结果,该试验是monalizumab联合西妥昔单抗(一种抗EGF受体的抗体)治疗头颈癌患者。结果显示,30%的患者在联合治疗后肿瘤负荷减轻。
“现在,NKG2A看起来有望成为有潜力的免疫治疗检查点,靶向NKG2A的抗体可以增强由癌症疫苗诱导的免疫疗法。” Michael Korrer总结道。
责编:探索君
End
参考资料:1)NKG2A Blockade Potentiates CD8 T Cell Immunity Induced by Cancer Vaccines
2)Discovery of new 'checkpoint' points to new cancer immunotherapy option
本文系生物探索原创,欢迎个人转发分享。其他任何媒体、网站如需转载,须在正文前注明来源生物探索。