致敬PROTAC技术!破解“不可成药”蛋白靶点密码,下一代重磅疗法在路上
2019年7月12至13日,由药时代主办的“新靶点 新技术 新机遇 助力新跨越!—— 2019中国抗肿瘤药高峰论坛”在上海成功举办,在这场业界最前沿的会议上,各位专家精心准备的报告可谓是让人“听君一席话,胜读十年书”,精彩纷呈的内容也获得全场一致好评。
来自清华大学药学院的饶燏博士在论坛大会上所带来的报告《小分子靶向蛋白质降解——生物医药最前沿》引起了全场最热烈的掌声与讨论。他所研究的蛋白降解靶向嵌合体(PROteolysis TArgeting Chimeria, PROTAC)技术也引起了众人的强烈关注。
饶燏教授 图片来源:药时代
目前,这一技术已然在国际悄悄“走红”。《Nature》杂志在今年3月20日发文对此进行评价:”基于PROTAC技术的蛋白降解剂或许会成为下一个重磅药物。”那么,这么重要的信息,我们怎么能错过呢?下面,让我们走近 PROTACs的前世今生,提前了解这个即将到来的抗肿瘤药界的“重磅炸弹”吧。
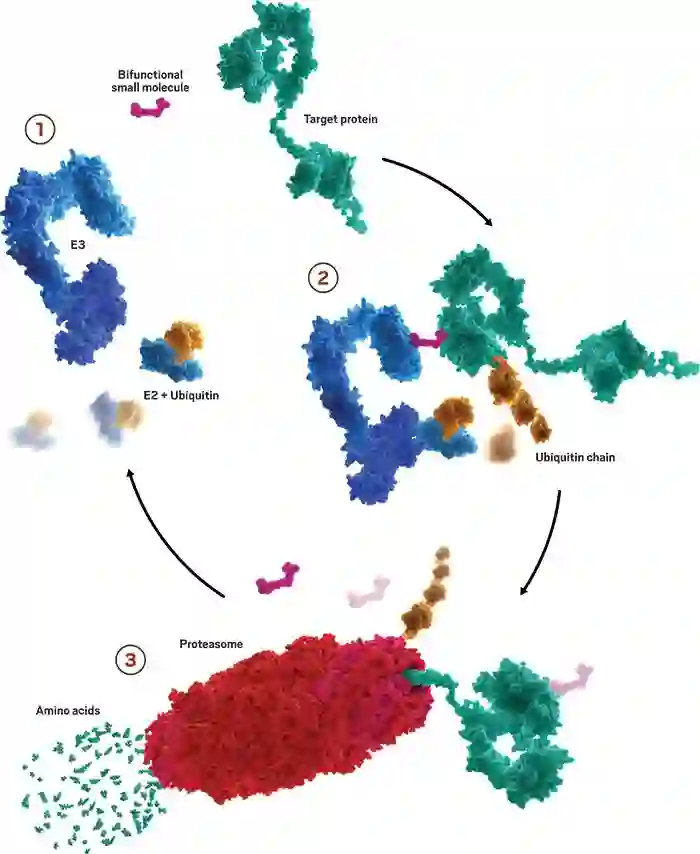
PROTAC技术:蛋白质降解剂通过劫持细胞的天然系统处理用过的或错误折叠的蛋白质来解决棘手的药物靶点。这些分子将引起疾病的蛋白质连接到E3泛素连接酶(1),募集E2蛋白并标记蛋白质以进行泛素化(2)并随后分解成蛋白酶体中的氨基酸(3)。然后分子继续重复该过程。图片来源:Kymera Therapeutics【参考资料1】
2018年2月19日,发表在《C&EN News》杂志上的一篇由Lisa Jarvis撰写的PROTAC技术综述,第一次系统介绍了这一技术20年来的发展。作者评价到:自从人类基因组被解读以来,研究人员就在试图靶向成千上万导致疾病的蛋白。但目前可知的仅有10%的蛋白能作用于小分子调控,10%能作用于大分子调控,而剩下80%的蛋白质靶标在现有技术面前几乎“无药可用”。蛋白靶向降解 (Targeted protein degradation) 或许能够成为挽救这一惨淡局面的新兴药物研发方向。【参考资料1】
追溯其起源,蛋白降解靶向嵌合体(PROTAC),可以说是一项源于诺贝尔化学奖的技术。2004年10月6日, 以色列科学家Aaron Ciechanover、Avram Hershko和美国科学家Irwin Rose, 因共同发现了泛素(Ubiquitin, Ub)调节蛋白的降解过程被授予诺贝尔化学奖。基于这一机制,Raymond J. Deshaies(美国两院院士)和Craig M. Crews(Arvinas公司创始人)等人在2001年最早提出了PROTAC这个概念,并成功地设计和合成了第一代PROTACs双功能分子用于降解甲硫氨酰氨肽酶2(MetAP-2)。但由于这些基于大而笨重的肽而起连接作用的化合物很难以进入细胞,第一代PROTACs宣告失败。
DOI: 10.1038/nchembio.1858【参考资料2】
直到2008年,Crews教授及其同事设计出了第二代PROTACs:基于E3的泛素蛋白连接酶MDM2, 是一种可用于降解雄激素受体(AR)的小分子蛋白降解剂。2015年是小分子PROTACs研究成果丰硕的一年,Crews教授及其团队开发出一种结合VHL的PROTACs,使用该技术可使多种蛋白的水平降低超过90%基于CRBN配体的PROTACs开发。此时,研究人员才开始相信,PROTAC技术或许能够变成药物。
与传统小分子药物阻断蛋白质功能不同的是,蛋白靶向降解药物力图将小分子设计成为新型药物,通过蛋白酶(proteasome) 的自然降解作用能将药效发挥的更完整。
DOI:10.1038 / d41586-019-00879-3【参考资料3】
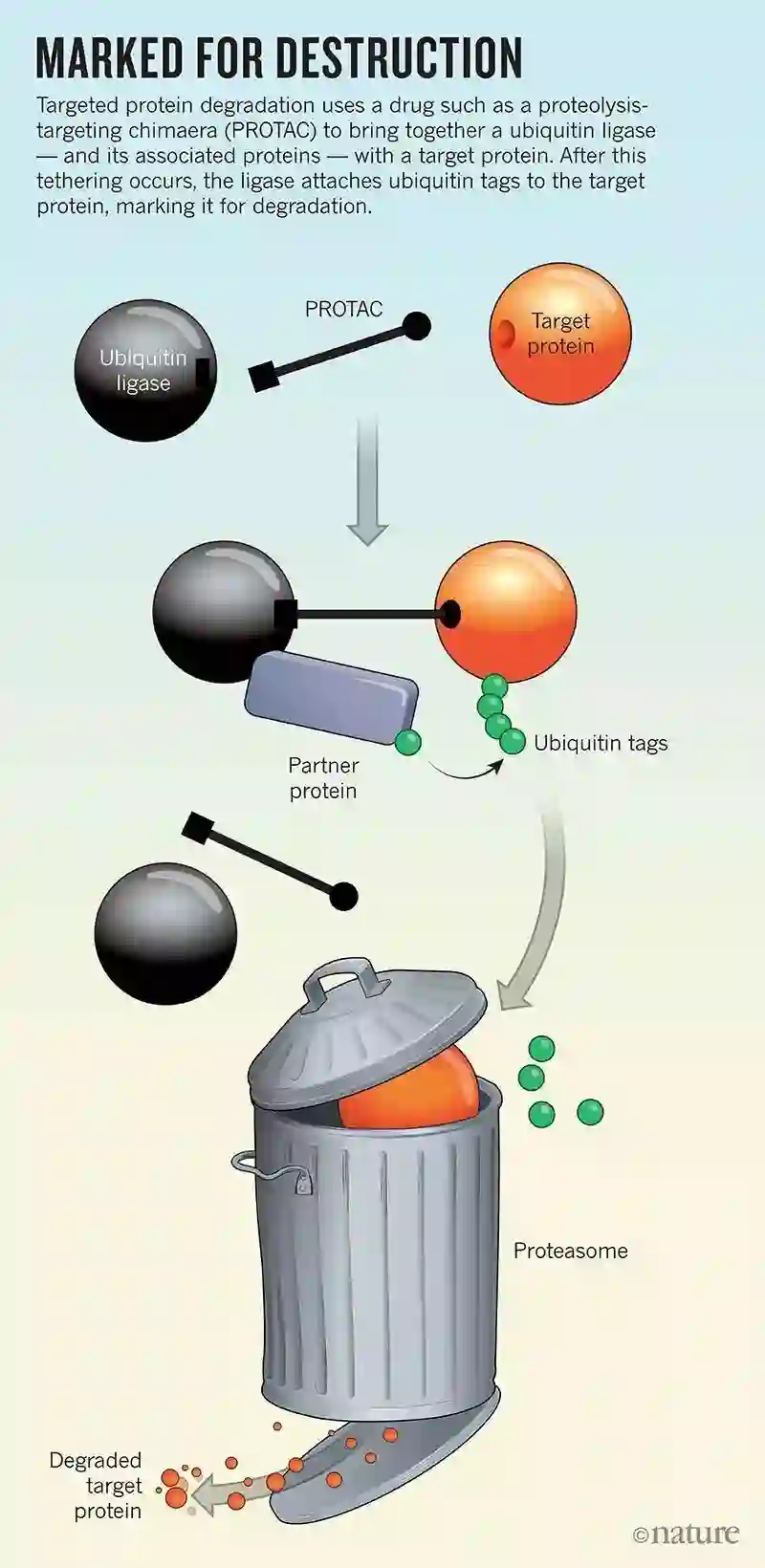
蛋白降解靶向嵌合体 (PROTAC)是一种特殊的蛋白降解技术, 使用一个Linker,一端连接目标蛋白的抑制剂,另一端连接泛素连接酶E3的结合配体分子。PROTACs代表了一种化学敲降策略,泛素连接酶作为细胞天然处理垃圾系统的一部分,将“泛素“这个标签标记到有缺陷或受损的蛋白质上。之后,细胞蛋白酶便自动识别这个标签,从而有效规避传统小分子药物的短板,有着巨大的应用潜力。(具体过程如下图)
DOI:10.1038 / d41586-019-00879-3【参考资料3】
随着时间慢慢推移,近几年来PROTAC技术进入前所未有的发展阶段。科学家们逐渐看到了该技术绝对的优势,不仅可以让非药物靶点(undruggable)转变为可行的药物靶点(druggable),还能化解现有靶点耐药性的问题。或许新型抗肿瘤重磅药物已悄然来临。
DOI:10.1038 / s41422-018-0055-1【参考资料4】
2018年6月6日,清华大学药学院饶燏教授及其团队在《Cell Research》杂志上发表了一篇论文在体外实验中证实:针对B细胞恶性肿瘤临床一线药物依鲁替尼(全球首个获批上市的BTK抑制剂) 的耐药性,可借助PROTAC技术通过 BTK蛋白降解剂靶向降解C481S突变的BTK蛋白来有效克服。
DOI:10.1038 / s41375-019-0440-X【参考资料5】
3月11日,饶燏教授及其团队又在Nature子刊《Leukemia》杂志上发表了最新体内实验的结果。结果表明,利用PROTAC技术降解多种突变型BTK蛋白,能够有效抑制对依鲁替尼耐药的非霍奇金淋巴瘤(B细胞恶性肿瘤的一种)发展。研究人员们也表示,或许PROTACs策略(蛋白质降解而不是抑制)可以作为未来耐药性癌症的强有力的治疗方法。
在此次论坛大会上,饶燏教授表示,之所以会选择BTK作为研究靶点,一方面是因为它是一个与B细胞恶性肿瘤相关的十分重要的靶点,另一方面是由于患者对依鲁替尼的临床耐药性日渐严重, 需要一种新的药物来帮助患者获得生机。因此,他和团队借助PROTAC技术,探究明星抗癌药真实的临床耐药问题。接下来,他们也将进一步深入开展关于小分子蛋白降解剂在多数靶点上的应用,以求解决更多耐药性问题或开发出新的抗肿瘤重磅药物。
Amgen全球研究高级副总裁Raymond Deshaies作为Crews教授的早期合作者,对此技术表现出极大的兴趣。在一次采访中,他说到,如今这个技术不仅吸引着来自包括罗氏,辉瑞,默克,诺华和葛兰素史克等巨头制药公司数十亿美元的投资,还推断几乎每家公司都有PROTAC技术所适用的潜在项目存在。
Craig M. Crews教授 图片来源:Chem-Station
就在5月29日,由Crews教授创立的基于目标蛋白质降解创造了新型药物Arvinas公司终于获得美国食品和药物管理局 (FDA)首个批准,允许其用于治疗选择性靶向和降解雄激素受体(AR)蛋白的患有转移性去势抵抗性前列腺癌(mCRPC)的口服蛋白降解剂ARV-110招募1期临床试验男性患者。
在6月25日,Arvinas公司再次获得FDA批准其用于选择性地靶向ER治疗的局部晚期或转移性ER阳性/ HER2阴性乳腺癌癌症的口服蛋白降解剂ARV-471于2019年第三季度开始1期临床试验。
正如饶燏教授所说的那样:未来,将是PROTACs的时代,2019年到2021年将是这一领域爆发的时期。这项技术不仅吸引了包括Arvinas,C4 Therapeutics和Kymera Therapeutics等公司专注于改良靶向降解剂的化学特性,也将给我们带来了无限的可能。这可能是药物开发领域最具颠覆性的技术,也请我们共同瞩目这一技术的盛大到来!
往期精选
围观
热文
热文
热文
热文
End
参考资料:
[1] Targeted protein degraders are redefining how small molecules look and act
[2] Catalytic in vivo protein knockdown by small-molecule PROTACs
[3] Protein-slaying drugs could be the next blockbuster therapies
[4] PROTAC-induced BTK degradation as a novel therapy for mutated BTK C481S induced ibrutinib-resistant B-cell malignancies
[5] Degradation of Bruton’s tyrosine kinase mutants by PROTACs for potential treatment of ibrutinib-resistant non-Hodgkin lymphomas
[6] Small-molecule PROTACs: An emerging and promising approach for the development of targeted therapy drugs
[7] 【PROTACs】新药开发系列
[8] 颠覆性PROTACs技术迎来突破 蛋白降解剂将成下一个重磅药物?
本文系生物探索原创,欢迎个人转发分享。其他任何媒体、网站如需转载,须在正文前注明来源生物探索。