光照就会性高潮!最新研究:奖励机制让果蝇深陷“红灯区”
用奖惩机制驯化自然生物是人类智慧的一大表现,但也许你并没有意识到,在人类漫长的生存和演化中,也存在着自我奖励机制(Reward Mechanism)和自我“驯化”的痕迹。
奖励系统是一系列强化生物特定行为的神经回路,这些神经回路所控制的行为恰恰是生物生存所必须的,比如交配、食物摄取、社交行为等。研究者发现,人脑中可以分泌多种让人感到快乐、安全和成就感的物质,如多巴胺、内啡肽等,对特定的行为通过奖赏机制加以鼓励,使人类体验到满足和喜悦,因而更愿意完成某些适应生存环境的艰难任务。
图 | 研究对象果蝇
鉴于交配对于生物繁衍的重要意义,毫无疑问,促进交配成功的行为应该使生物得到奖励,即精神愉悦,获得快感高潮。一直以来,研究者都对于人以外的生物是否存在“性趣”持怀疑态度。而今,来自以色列巴伊兰大学(Bar-Ilan University)的研究团队以果蝇为研究对象,对其在交配过程的奖励机制进行研究。有趣的是,研究者发现在漫长的演化中,雄性果蝇可以从交配过程,或者更严格意义上来说,射精行为中获得快感,且这一奖励机制一直获得保留。
该项研究首次证明了自然界中无论是果蝇或是哺乳动物,射精所带来的快感(奖励机制)都是高度保守的,即高度一致,在演化的过程中没有发生变化。同时,该研究也证实了生物内在状态的改变会对外来药物或事物感知产生影响。研究者可通过操纵果蝇的性经验,使果蝇对摄入酒精的兴趣明显下降。
图 | Galit Shohat-Ophir
“大脑中的奖励过程对于所有生物都高度保守,这是生物生存的基础,” 该研究的研究组长 Galit Shohat-Ophir 说到,“而大脑在滥用药物的过程中经历了相同的奖励机制。该项研究结果的证实,将有助于我们建立更简单的生物模型,用于药物成瘾的多方面研究,包括对自然奖励与药物奖励的区别、以及药物成瘾的危害等。”该研究发表在 Cell 子刊 Current Biology 上。
感情不顺?果蝇也会借酒浇愁
黑腹果蝇(Drosophila melanogaster),又称黑尾果蝇,因为其易在实验室饲养、繁殖迅速、产卵众多,且只有四对染色体,被人类广泛的应用于遗传学、生理学、微生物致病机理及生物演化史等方面的研究,是人类应用最多的模式生物之一。直到 2017 年,已有 8 个诺贝尔奖颁给使用果蝇的相关研究。
果蝇在演化过程中,保留了因社交行为而获得兴奋的奖励机制,为了验证性交与饮酒之间的关系,即社交活动对随后行为的影响,2012年,本文的研究者 Galit Shohat-Ophir 联合加州大学旧金山分校的研究团队开展了一个非常有趣的实验,其研究结果发表在 Science 杂志上。
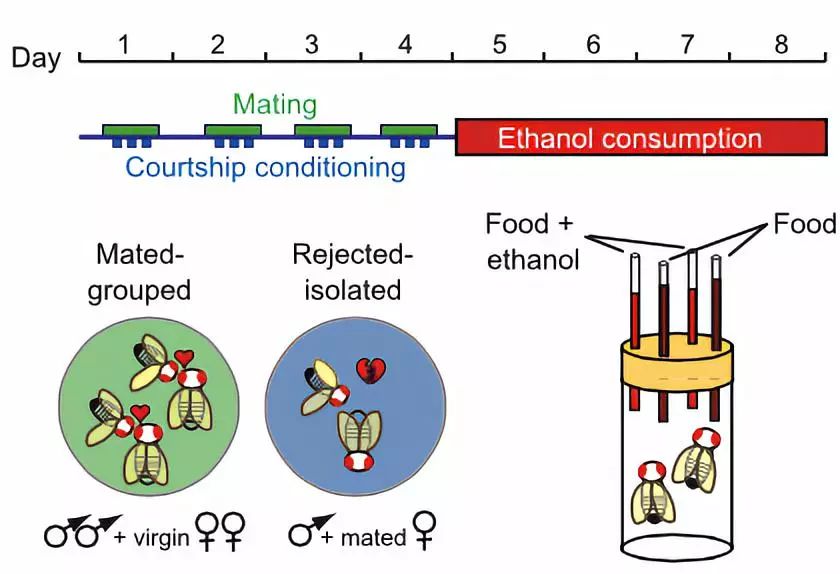
图 | 果蝇社交活动研究实验流程
研究中,他们将雄性果蝇分为两组,一组以1:5的比例与未交配过的雌性果蝇放在一起,每天6小时,持续处理4天,因而每只雄性果蝇每天都有多次机会与多个雌性进行交配;另一组则恰恰相反,12只未交配过的雄性果蝇与已经交配过的雌性果蝇放在一起,雌性果蝇由于已经交配过,因而对于同一容器内雄性果蝇的求爱视若无睹,因而在每天3次、每次1小时、持续4天的处理中,这一组雄性果蝇不停的遭遇求爱被拒。
在经历了4天差距悬殊的“待遇”之后,两组雄性果蝇被移入新的容器中,容器内分别装有添加酒精和不含酒精的糊状的食物,每只果蝇都可以选择要喝哪个毛细管上的食物,随后研究人员会测量果蝇的进食量。
结果差异十分显著,被多次拒绝的果蝇对添加酒精食物的摄入量是另一组果蝇的4倍,很显然,被拒绝的雄性果蝇借酒浇愁,甚至以“酗酒”的方式弥补糟糕的心情。
图 | 果蝇借酒浇愁
那么“酗酒”所能带来的精神奖励究竟是什么呢?一直以来,研究者都怀疑果蝇大脑中的神经肽F(neuropeptide F,NPF)是驱使生物摄取酒精、获得快感的原因。因而研究团队分别测量了两组雄性果蝇脑部神经肽F,惊喜的发现,被拒绝的果蝇,脑部神经肽F的含量只有对照组的一半。为了进一步验证,研究者通过抑制脑部的神经肽F受体,发现即使成功交配的果蝇也会摄入更多的酒精,其行为与求爱被拒的果蝇并无差异。
毫无疑问,在果蝇酗酒和交配过程中充当“快感源泉”的化合物就是神经肽F.那么,在复杂的交配过程中以及众多的外界因素影响下,究竟是哪个感官刺激,或是行为激发了奖励机制呢?
果蝇也爱“红灯区”
为简化研究,排除众多外界因素的影响,研究者将果蝇的整个性交过程简化为最后也是最重要的阶段:射精。
在雄性果蝇的腹部有一种特殊的神经元——黑化诱导神经肽表达神经元(corazonin-expressing neurons, 简称Crz神经元),他们可以通过分泌黑化诱导神经肽(corazonin,Crz)控制昆虫的心跳,刺激雄性果蝇射精。通常情况下,只有在一系列的复杂的求偶行为下,黑化诱导神经肽才能得以分泌。
图 | 光遗传学技术的应用帮助研究者“点亮”大脑
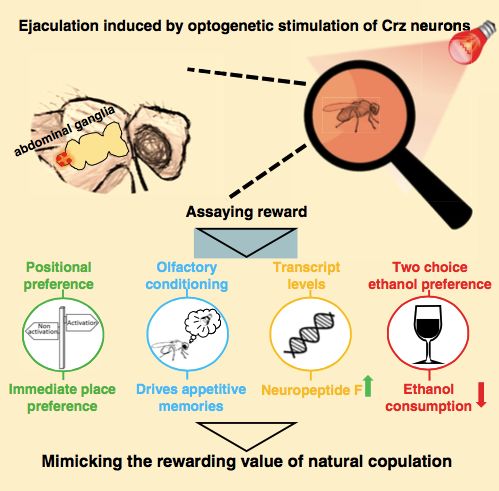
可如何绕过复杂的求爱、交配过程直接到达结果呢?聪明的研究者使用了光遗传学技术,通过一种对红光敏感的光敏蛋白“劫持”了这类细胞。在红光的照射下,Crz神经元表达被激活,不断分泌的黑化诱导神经肽促使雄性果蝇不停的射精。
光遗传学(optogenetics),又称光刺激基因工程(optical stimulation plus genetic engineering),是通过将微生物学、现代遗传学、神经科学等各项技术结合起来,通过给特定的细胞装上开关,使微生物光敏蛋白能够精确地在某一类神经元中表达,保证该类神经细胞在光照下的准确激活或抑制。
研究中,科学家们将经过光遗传学基因编辑的果蝇放入有红光照射和没红光照射的空间内。在红光下,基因编辑的雄性果蝇Crz神经表达会被激活并不停射精,而无红光情况下则表现正常,在实验中果蝇可以自由选择所处的位置。
结果令人惊喜,一旦进入“红灯区”,雄性果蝇便“流连忘返”,简直可以说是乐不思蜀。由于果蝇无法识别红色,因而选择在“红灯区”逗留的解释只能是因为射精可以给果蝇带来难以自拔的精神奖励。
对上述结果,研究者又进一步进行了验证。研究者对果蝇的神经肽F的转录表达水平及含有酒精的食物摄入进行了对比研究,结果发现,红灯下的雄性果蝇神经肽F表达量更高,同时对酒精的兴趣大大减弱。
图 | 光遗传学促进Crz神经表达刺激果蝇射精过程
雄性果蝇视交配为一种自然奖励,成功射精的雄性果蝇脑内有较高水平的神经肽F,显然,由Crz信号通路诱导的射精过程正是这一自然奖励最重要的一部分,这也是人类首次看到大脑以外的神经元可以诱导奖励行为。
蜂喜蜜,蚊喜血,一切生物的行为都趋向于自我取悦。除了排除万难完成任务达到满足,自我愉悦也有其他捷径,酗酒、吸烟、毒品、游戏等都可以为人类带来精神上的愉悦,也容易成瘾。
此项研究首次证明了射精的快感可以替代其他奖励行为,在生物漫长的演化过程中,奖励机制的高度保守更使其在未来人类酗酒或药物滥用的治疗上具有重要的借鉴意义。
正如 Shohat-Ophir 所说的,“在某些方面,6 条腿的与 2 条腿的并没有什么差别”。
-End-
编辑:Sha
参考:
https://www.cell.com/current-biology/fulltext/S0960-9822(18)30368-3
http://science.sciencemag.org/content/335/6074/1351.long
https://www.sciencenews.org/article/male-fruit-flies-enjoy-ejaculation
https://www.theatlantic.com/science/archive/2018/04/scientists-genetically-engineered-flies-to-ejaculate-under-red-light/558320/