另辟蹊径!CD4+T细胞谱写肿瘤免疫新篇章!

作者:Ruthy
导语
2010年以来,肿瘤免疫治疗发展迅速,以免疫检查点抑制剂为主的疗法已被证实可产生显著的抗原特异性免疫反应,决定该疗法成败的关键之一是提高T细胞的初始激活水平。目前治疗靶点的研究主要集中于CD8+T细胞,而CD4+T细胞在肿瘤免疫中扮演的角色逐渐受到重视,但其激活机制尚未得到准确诠释。

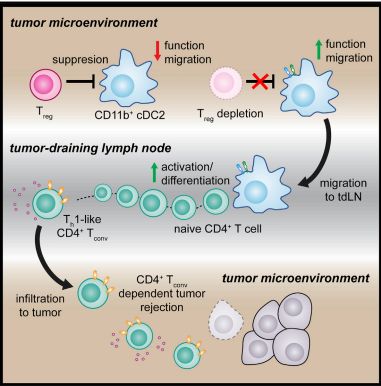
近日,加州大学的研究人员完整描述了肿瘤免疫中CD4+T细胞激活的过程,揭示了决定CD4+T细胞激活水平的关键——肿瘤微环境中的cDC2亚群,为提高CD4+T细胞的抗肿瘤免疫功能提供了宝贵意见。
CD4+T细胞——
肿瘤免疫不可或缺的重要角色
CD4+T细胞是人体免疫系统中的一种重要免疫细胞,CD4 主要表达于辅助T(Th)细胞,可与MHCⅡ类分子的非多肽区结合,参与T细胞抗原受体(TCR)识别抗原的信号转导。研究发现,在肿瘤免疫中,CD4+T细胞启动后可以通过多种机制激活CD8+T细胞,使其分化为细胞毒性T淋巴细胞(CTL),同时维持并加强CTL的抗肿瘤反应。另一方面,即使在没有CD8+T细胞的情况下,CD4+T细胞同样可以以IFN-γ机制直接杀死肿瘤细胞,这就说明CD4+T细胞是肿瘤免疫不可或缺的重要角色。因此,其有效激活也成为了肿瘤免疫治疗的必须关注的重点之一。
cDC2——
CD4+T细胞有效激活的关键
说到CD4+T细胞的激活,就必须提及机体功能最强的专职抗原递呈细胞——树突状细胞(DC),其能高效地摄取、加工处理和递呈抗原,未成熟DC具有较强的迁移能力,成熟DC能有效激活初始T细胞,其处于启动、调控、并维持免疫应答的中心环节。对不同组织来源DC的深入研究指出经典DC(cDC)的主要作用是诱导针对入侵抗原的特异性免疫应答并维持自身耐受,可通过分泌细胞因子与共刺激分子共同激活初始T细胞。我们知道,cDC有cDC1和cDC2两个亚群,这二者谁是CD4+T细胞有效激活的决定者呢?
研究人员对接种B16肿瘤的小鼠淋巴结中的髓系细胞进行了单细胞测序,发现迁移性cDC2亚群可以根据CD301b分子的有无分为两个不同亚群。后续增殖实验则证实了CD301b+/- cDC2亚群引发了初始CD4+T细胞的增殖。也就是说,cDC2是CD4+T细胞有效激活的关键。那是否意味着提高肿瘤微环境中的cDC2的比例,就能有效提高CD4+T细胞的抗肿瘤免疫效果?实验结果显示,如果仅仅提高cDC2比例,cDC2无法迁移至肿瘤区域,而且激活的CD4+T细胞并没有因此分化增加!抗肿瘤反应也停滞不前!这就意味着,应该还存在着可以“抗衡”cDC2的另一要素,是什么呢?
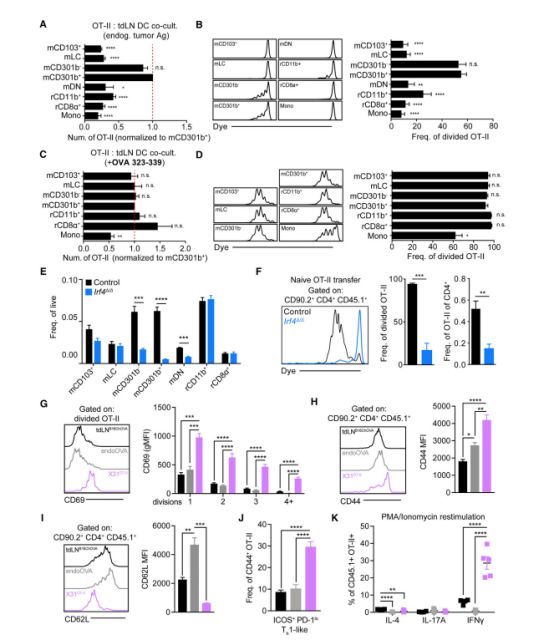
cDC2是CD4+T细胞有效激活的关键
Treg细胞——
阻滞CD4+T细胞激活的元凶
我们知道,肿瘤患者的外周血及肿瘤局部往往可以找到调节性T细胞(Treg细胞)的踪迹,有研究证实Treg细胞能够抑制免疫应答,因此研究人员猜想Treg细胞或许正是阻滞CD4+T细胞激活的元凶。研究人员去除了实验肿瘤小鼠体内的Treg细胞,发现cDC2可顺利迁移至肿瘤区域,同时小鼠的抗肿瘤免疫反应明显加强,而且他们证实这种免疫反应是依赖于CD4+T细胞产生的Treg细胞。
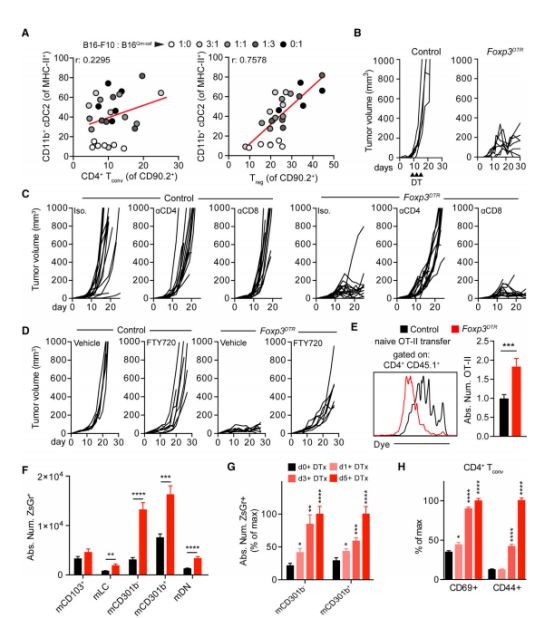
去除Treg细胞增加CD4+T细胞抗肿瘤活性
研究人员指出,去除Treg细胞后可增加cDC2共刺激因子和其它炎症因子的表达,同时促进初始CD4+T细胞激活分子的表达,推动初始CD4+T细胞向Th1样效应T细胞的分化,最终提高其抗肿瘤免疫反应。也就是说,cDC2正是Treg抑制剂的有效靶标,这为肿瘤免疫治疗的发展提供了一个新方向。
这项研究深入诠释了CD4+T细胞激活机制,为肿瘤免疫治疗研究开辟了一条新道路,有望谱写免疫治疗的新篇章。但这仅仅是临床前实验的结果,目前仍需更多数据证据加以佐证,这一切都需要充足的时间和精力,我们拭目以待。
参考文献:
Mikhail Binnewies,et al.Unleashing Type-2 Dendritic Cells to Drive Protective Antitumor CD4+ T Cell Immunity.Cell.
推荐内容



