江苏大学钱晖、许文荣团队又出新作:p53缺失的小鼠骨髓MSC外泌体富含UBR2通过Wnt/β-Catenin途径胃癌的进展
近日,国内外泌体领域研究高产的钱晖、许文荣团队又出新成果,在国际知名干细胞领域杂志Stem Cells上发表题为“p53缺失的小鼠骨髓MSC外泌体富含UBR2通过Wnt/β-Catenin途径胃癌的进展”的文章,介绍了p53缺失的间充质干细胞分泌的外泌体富含一种蛋白UBR2,该蛋白可以以外泌体为载体转移到小鼠前胃癌细胞,从而促进胃癌的进展。
p53的缺失或突变与几种类型的癌症有关。间充质干细胞(MSC)是肿瘤微环境中的重要组成部分,MSCs分泌的外泌体可将生物活性分子(包括蛋白质和核酸)转移到肿瘤微环境中的其他细胞中,影响肿瘤的进展。然而,MSCs中p53的状态是否会影响外泌体的生物活性分子分泌以促进癌症发展、其调控机制是什么仍然不清楚。该研究旨在探究p53缺陷小鼠骨髓MSC(p53-/- mBMMSC)分泌的富含泛素蛋白连接酶E3组件n-recognin 2(UBR2)的外泌体在体内和体外对胃癌进展的影响。研究发现p53-/- mBMMSC中外泌体的浓度显著高于p53野生型mBMMSC(p53 +/+ mBMMSC)。尤其是UBR2在p53-/- mBMMSC细胞和外泌体中高表达。P53-/- mBMMSC外泌体富集的UBR2可以内化到p53+/+ mBMMSC和小鼠前胃癌细胞(murine foregastric carcinoma, MFC)中,诱导UBR2在这些细胞中过度表达,从而促进细胞的增殖、迁移和干性相关基因的表达。从机制上看,UBR2在p53-/- mBMMSC外泌体中的下调可以逆转这些行为。此外,大多数Wnt家族成员β-连环蛋白及其下游基因(CD44,CyclinD1,CyclinD3和C-myc)在UBR2敲低和β-连环蛋白敲除的MFC中显著降低,UBR2敲除没有造成Nanog、OCT4、Vimentin和E-cadherin的显著表达差异。总之,这些研究结果表明,p53-/- mBMMSC外泌体可以通过调控Wnt/β-连环蛋白途径将UBR2递送至靶细胞并促进胃癌生长和转移。
该研究的重要意义:
胃癌仍然是全球癌症死亡的主要原因。探索参与胃癌发生发展的新型分子和分子机制至关重要。越来越多的证据表明,间充质干细胞(MSCs)在调节胃癌发展中起重要作用。先前的蛋白质组学分析已经证实MSC外泌体富含泛素蛋白连接酶E3组分N-识别蛋白2(UBR2)。然而,p53缺失型小鼠骨髓MSC的外泌体(p53-/- mBMMSC-外泌体)是否可以将UBR2转移至p53+/+ mBMMSC和小鼠前胃癌(MFC)细胞来促进胃癌生长和转移,其潜在的机制仍然不清楚。这篇论文证明富含p53-/- mBMMSC的外泌体的UBR2可以重新编程p53+/+ mBMMSC和MFC细胞,促进胃癌的体外和体内进展。UBR2在p53-/- mBMMSC细胞和外泌体中高表达,可以转移到p53+/+ mBMMSC和MFC细胞中,提高细胞的增殖、迁移和p53+/+ mBMMSC和MFC细胞干性相关基因的表达。UBR2在MFC中的敲低可能影响Wnt/β-catenin通路的活性。该研究为p53-/- mBMMSC-外泌体UBR2参与胃癌进展提供了新的机制,为胃癌的诊断和治疗开辟了新的途径。
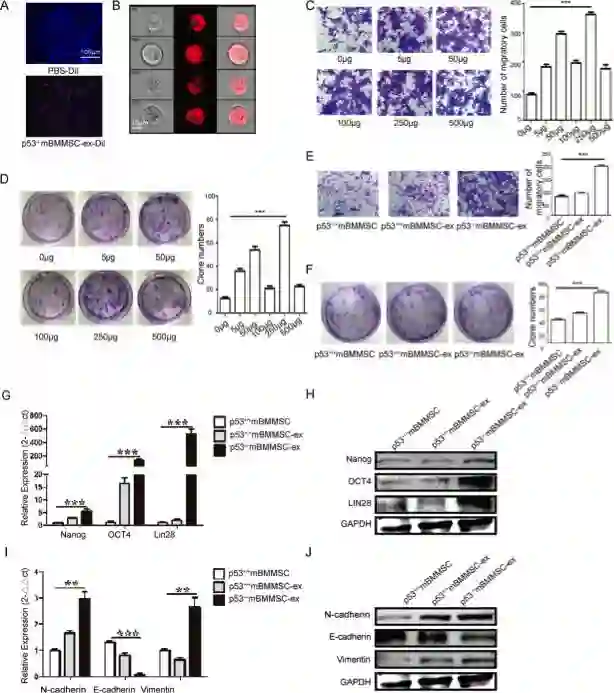
p53–/–mBMMSC外泌体可转移到 (p53+/+mBMMSC) 和MFC,敲除UBR2可抑制p53–/–mBMMSC的增殖、迁移和干性
参考文献:
Jiahui Mao, Zhaofeng Liang, Bin Zhang, Huan Yang, Xia Li, Hailong Fu, Xu Zhang, Yongmin Yan, Wenrong Xu, Hui Qian. UBR2 Enriched in p53 Deficient Mouse Bone Marrow Mesenchymal Stem Cell-Exosome Promoted Gastric Cancer Progression via Wnt/β-Catenin Pathway. Stem Cells 2017;35:2267–2279 DOI: 10.1002/stem.2702
科研学习班推荐 (点击详细了解):