恒瑞与Incyte终止合作开发PD-1单抗SHR-1210
2月14日,恒瑞医药公告称,经与Incyte协商,双方签订了终止合作开发 PD-1 单克隆抗体SHR-1210的协议。
本文转自医药魔方数据微信,发布已获医药魔方授权,如需转载,请与医药魔方联系。
恒瑞与Incyte是在2015年9月2日签订了SHR-1210的合作开发协议,恒瑞将SHR-1210除中国大陆、香港、澳门和台湾地区以外的全球独家临床开发和市场销售权利许可给Incyte。该笔交易总额合计7.95亿美元,协议签订后30天内Incyte需要向恒瑞支付2500万美元首付款。
双方此次终止SHR-1210的合作开发并不算太意外。
一方面,SHR-1210的海外开发进展在Incyte的2017Q1季报中曾显示试验招募暂停。另一方面,Incyte在2017年10月又以9亿美元从MacroGenis引进了另一款PD-1单抗药物MGA012所有适应症的全球开发和商业权利,包括支付1.5亿美元首付款,4.2亿美元的临床开发和注册里程金,3.3亿美元的商业开发里程金。如果MGA012获批上市并实现商业销售,Incyte还需向MacroGenics支付15%~24%的分层销售收入分成。
Incyte虽然此前一直未明确透露SHR-1210的合作开发动向,但花了更大代价的首付款再引进一款PD-1药物之后,业内已有猜测Incyte可能会终止开发SHR-1210。
Incyte已经在澳大利亚开展了SHR-1210 的 I期临床试验研究。恒瑞在公告中表示:“收回海外权益后,恒瑞将自主继续推动澳洲临床开发并开展包括美国在内的国际多中心临床试验。恒瑞认为自主开发SHR-1210有利于该产品利益最大化且符合股东长期的利益。”
目前,恒瑞 SHR-1210 在国内针对多个瘤种、适应症的 II、III 期 临床试验正顺利进行中。此外,恒瑞的PD-L1单抗SHR-1316也已经在国内获批临床,并于2018/1/24登记了第1项临床研究(CTR20180040),主要评估SHR-1316在晚期恶性肿瘤患者中的安全性和耐受性。
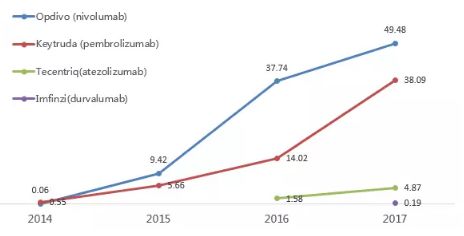
全球目前共批准上市了5个PD-1/PD-L1单抗药物,2017年全球PD-1/PD-L1药物的市场规模达到100亿美元左右。中国是肿瘤大国,PD-1药物的竞争十分激烈,目前已经有百时美施贵宝Opdivo、信达生物信迪单抗、默沙东Keytruda陆续申请上市。
PD-1/PD-L1药物全球销售额(亿美元)
注:Tecentriq销售额单位为亿瑞士法郎
End