J Lipid Res杂志连发两篇外泌体脂质相关综述 阐述磷脂和鞘脂在外泌体发生和应用中的作用
5月31日,脂类研究期刊TheJournal of Lipid Research连发两篇细胞外囊泡及外泌体领域的文章,着重介绍了外泌体中磷脂酶、磷脂酸、鞘脂、鞘磷脂酶等脂质在外泌体发生和功能应用中的作用,研究外泌体脂质以及代谢组学的同仁可以下载一读。
1. 磷脂酶D和磷脂酸在细胞外囊泡的生物发生和货物装载中的应用
Egea-JimenezAL, Zimmermann P. Phospholipase D and phosphatidic acid in the biogenesis andcargo loading of extracellular vesicles. J Lipid Res. 2018 May 31.
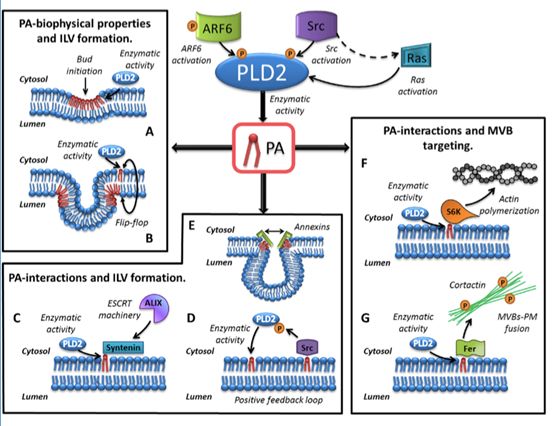
摘要:活细胞释放的细胞外囊泡(包括外泌体和微泡)已经成为支持细胞间通讯的重要细胞成分。由于它们潜在的治疗意义,研究人员正在努力表征这些囊泡的内容和研究控制其生物发生的机制。最近研究证实,脂质修饰酶磷脂酶D2(PLD2)参与外泌体生成并且在GTP酶ARF6的下游起作用。这篇综述旨在重述我们对PLD2及其产物磷脂酸(PA)在外泌体生物发生中的作用的现有知识,并提出进一步研究这些分子在这些外泌体中的生物学中可能的中心作用。
下图:磷脂酶D和磷脂酸在细胞中多泡体(MVB)的形成和向细胞膜移动产生外泌体过程中的作用。
2. 鞘脂在细胞外囊泡的生物合成和生物学活性中的作用
VerderioC, Gabrielli M, Giussani P. Role of sphingolipids in the biogenesis andbiological activity of extracellular vesicles. J Lipid Res. 2018 May 31.
细胞外囊泡(EV)是由真核细胞和原核细胞释放的囊泡。它们不仅具有独特的生理功能,如处理细胞成分和细胞废物,而且在炎症和退行性疾病中发挥病理生理作用。 EV的生物发生的共同分子机制在真核生物的不同病理细胞生物学环境中是很明显的,并且抑制EV的生物发生可能为治疗研究提供了途径。鞘脂类及相关酶在EV生物发生和释放中的研究中尚未得到很多关注。这篇综述通过塑造膜曲率以及靶细胞中细胞外囊泡作用研究来回顾鞘脂类如何参与细胞外囊泡生物发生。首先,作者描述了酸性和中性鞘磷脂酶如何通过产生组成型鞘脂神经酰胺促进胞质囊泡在胞质膜和胞内体的生物发生。然后讨论其他鞘脂如神经鞘氨醇磷酸盐和半乳糖神经鞘氨醇在细胞外囊泡形成和货物分选中的参与情况。最后,展望由受体细胞中鞘脂水平变化介导的细胞外囊泡的一系列的生物效应。
在过去的10年中已经取得了进展,阐明了EV是如何形成的,并且在形成膜负曲率(远离细胞质方向)的过程中神经酰胺(Cer)的基本作用已经建立,这对于外泌体和微泡生物发生都是必需的。这篇综述讨论的EV生物发生的例子中,已经广泛研究了n-和a-SMase(中性和酸性鞘磷脂酶)并分别介导外泌体和MV的释放。特别地,a-SMase的明确作用已经在通过刺激各种表面受体或在压力条件下发生的MV释放中得到证实。然而,n-SMase抑制剂GW4869是一种更为复杂的情况,它通过阻断外泌体释放,成为增强而不是阻断上皮细胞表面MV产生的常用工具。
综合证据表明,鞘脂(SL)及其酶在EV中有重要作用,尽管SL含量较少,SL种类仍不确定。SL除了作为癌症和炎性疾病中潜在疾病生物标志物外,囊泡SL和它们的代谢酶已显示通过影响受体细胞中的SL水平而促进EV的作用。有趣的是,EV也可能通过转移靶向SL代谢的miRNA来影响SL在受体细胞中的活性,比如原核细胞产生的EV的转录组分析中的结果证实了这一点。我们预计未来在不同细胞生理学中表征EV将有助于理解这些高度保守的哺乳动物细胞间通讯传递者,它们的生物发生和信号传导功能的探究也将产生广泛影响。
科研学习班了解一下~ ~(点击详细了解):
MATLAB高级编程及机器学习技术应用研讨班
关注 外泌体之家 公众号
回复“外泌体” 阅读外泌体最新科研进展及动态
回复“EV” 阅读 2016-2018年This Week in Extracellular Vesicles
回复“盘点” 阅读 外泌体领域十大前沿进展盘点